გართულებები
ინტენსიური თერაპიის განყოფილებაში ნამკურნალებ COVID-19-ის მქონე პაციენტებს შესაძლოა გამოუვლინდეთ ინტენსიური მკრუნალობის შემდგომი სინდრომი, რომელიც ხასიათდება ფსიქიატრიული, კოგნიტიური და/ან ფიზიკური ქმედუუნარობის სპექტრით (მაგ. კუნთების სისუსტე, კოგნიტური დისფუნქცია, ინსომნია, დეპრესია, შფოთვა, ტრავმის შემდგომი სტრესული აშლილობა, დელირიუმი, ენცეფალოპათია). სინდრომი გვხვდება კრიტიკულ პაციენტებში მკურნალობის შემდგომ და გრძელდება ინტენსიური განყოფილებიდან პაციენტის გაწერის შემდეგაც. რისკის მაქსიმალურად შემცირება შესაძლებელია მედიკამენტური მართვით, ფიზიკური რეაბილიტაციით, ოჯახის მხარდაჭერითა და შემდგომი მეთვალყურეობის კლინიკების ჩართულობით. ფიზიკური, გონებრივი ან კოგნიტური სიმპტომები ხშირად აღინიშნა პაციენტებში, რომლებიც გადარჩნენ ინტენსიური თერაპიის განყოფილებაში მოთავსებიდან 1 წლის განმავლობაში.[940]
ჰიპერკოაგულაციური მდგომარეობა დაავადების ერთ-ერთი დამახასიათებელი ნიშანია, განსაკუთრებით მძიმედ დაავადებულ პაციენტებში, რაც ხშირად ვლინდება ვენური და არტერიული თრომბოემბოლიის სახით. კოაგულოპათიას COVID-19-ში აქვს პროთრომბოზული ხასიათი, D-დიმერის, ფიბრინის, ფიბრინის დეგრადაციის პროდუქტებისა და ფიბრინოგენის მატებით.[941] მძიმე და კრიტიკული დაავადების მქონე პაციენტებში გამოვლინდა ანტიფოსფოლიპიდური ანტისხეულები; თუმცა, ამჟამად არ ჩანს რაიმე კავშირი ამ აღმოჩენასა და დაავადების შედეგებს შორის (მაგ., თრომბოზი, სიკვდილობა).[942]
ეპიდემიოლოგია: ვენური თრომბოემბოლიის, ღრმა ვენების თრომბოზისა და ფილტვის ემბოლიის ინციდენტობა ჰოსპიტალიზებულ პაციენტებში შეადგენდა 14.7%-ს, 11.2%-ს და 7.8%-ს (იმავე რიგითობით). თრომბოპროფილაქტიკის მიუხედავად, პრევალენტობა მნიშვნელოვნად მაღალი იყო რეანიმაციულ განყოფილებაში მოთავსებულ პაციენტებში. არტერიული თრომბოემბოლიის პრევალენტობა უფრო დაბალია- 3.9%; თუმცა, მტკიცებულებები მწირია.[943] თრომბოემბოლიური მოვლენები იშვიათია ბავშვებში.[944] ვენური თრომბოემბოლიის პროგნოზირების ყველაზე ძლიერი რისკფაქტორებია ხანდაზმული ასაკი და D-დიმერის დონის მატება.[945] მამრობითი სქესი, სიმსუქნე, მექანიკური ვენტილაცია, მოთავსება ინტენსიურ განყოფილებაში, მძიმე პარენქიმული ცვლილებები და მომატებული ლეიკოციტები ასევე განსაზღვრულია, როგორც რისკფაქტორები.[946] ფილტვის მწვავე ემბოლიის და ღრმა ვენების თრომბოზის კუმულაციური სიხშირე გამოჯანმრთელებულ პაციენტებში საავადმყოფოდან გაწერის შემდეგ იყო 1.2% და 2.3%, შესაბამისად, რაც გაცილებით დაბალია საავადმყოფოში დაფიქსირებულ სიხშირესთან შედარებით.[947] არაჰოსპიტალიზებულ პაციენტებს ასევე შეიძლება ჰქონდეთ თრომბოემბოლიური მოვლენების მომატებული რისკი.[948]
ეტიოლოგია: პათოგენეზი სრულად არ არის ცნობილი. ვარაუდობენ, რომ ადგილობრივი თრომბები წარმოიქმნება ადგილობრივი ანთებითი პროცესის გამო, შედარებით კლასიკურ ემბოლიასთან, რომელიც მოდის სხეულის სხვა ნაწილიდან.[949][950] პაციენტები შესაძლოა მიდრეკილნი იყვნენ თრომბოემბოლიის განვითარებისადმი ინფექციის როგორც პირდაპირი, ასევე არაპირდაპირი ეფექტების (მაგ., მძიმე ანთებითი რეაქცია, კრიტიკული მდგომარეობა, ტრადიციული რისკფაქტორები) გამო.[951] თრომბოზული მოვლენების მიზეზი შეიძლება იყოს ციტოკინების შტორმი, ჰიპოქსიური დაზიანება, ენდოთელიუმის დისფუნქცია, ჰიპერკოაგულაცია და/ან თრომბოციტების გაძლიერებული აქტივობა.[952]
დიაგნოსტიკა: დააკვირდით პაციენტებს ვენური ან არტერიული თრომბოემბოლიის დამახასიათებელ ნიშნებსა და სიმპტომებზე და გააგრძელეთ მართვა ადგილობრივი პროტოკოლების მიხედვით.[85] ჰოსპიტალიზაციისას განსაზღვრული D-დიმერის დონე დაკავშირებულია ვენური თრომბოემბოლიის დიაგნოზთან ჰოსპიტალიზაციის დროს; თუმცა, არ არსებობს ოპტიმალური ზღვრები პროფილაქტიკური ზომების წარმართვისთვის.[953] შეაფასეთ ჰოსპიტალიზებული პაციენტები, რომლებსაც აღენიშნებათ ფილტვის, გულის ან ნევროლოგიური ფუნქციის სწრაფი გაუარესება, ან პერიფერიული პერფუზიის უეცარი ლოკალიზებული დაქვეითება თრომბოემბოლიური დაავადების გამო.
მართვა: თრომბოემბოლიური მოვლენის შემთხვევაში (ან თრომბოემბოლიური დაავადების მაღალი რისკის დროს, როდესაც ხელმისაწვდომი არ არის ვიზუალიზაცია) უმკურნალეთ პაციენტებს ანტიკოაგულანტის თერაპიული დოზებით. მიყევით ადგილობრივ ინსტიტუციურ პროტოკოლებს.
მონიტორინგი: ჰემატოლოგიური და კოაგულაციის პარამეტრები ჩვეულებრივ იზომება ჰოსპიტალიზებულ პაციენტებში; თუმცა, ამჟამად არ არის საკმარისი მტკიცებულება, რომ რეკომენდაცია გაუწიოს ამ მონაცემების გამოყენებას მართვის გადაწყვეტილებების წარმართვის მიზნით. D-დიმერის ძალიან მაღალი დონის მქონე პაციენტებს აქვთ თრომბოზის მომატებული რისკი, ამიტომ მნიშვნელოვანია მათი აქტიური მონიტორინგი.[616][617]
პროგნოზი: პაციენტები, რომლებსაც თრომბოემბოლიური გართულებები აღენიშნებათ, ექვემდებარებიან გარდაცვალების 1.93-ჯერ მეტ ალბათობას, ვიდრე პაციენტები ვენური თრომბოემბოლიების გარეშე.[954]
ასევე იხილეთ დისემინირებული ინტრავასკულური კოაგულაცია ქვემოთ.
გულ-სისხლძარღვთა გართულებები მოიცავს არითმიებს, მიოკარდიუმის დაზიანებას, მწვავე კორონარული სინდრომს და გულის უკმარისობას.[955] მიუხედავად იმისა, რომ მწვავე ინფექცია ასოცირებული იყო საერთო ჯამში გულ-სისხლძარღვთა დიაგნოზების ექვსჯერ ზრდასთან, რისკი მცირდება ინფექციიდან 5 კვირის შემდეგ და უბრუნდება საწყის დონეს ან ნაკლებს 12 კვირიდან 1 წლამდე პერიოდში.[956]
ეპიდემიოლოგია: გულ-სისხლძარღვთა გართულებები დაფიქსირდა პაციენტების 14.1%-ში ჰოსპიტალიზაციის დროს.[955] მიოკარდიუმის მწვავე ინფარქტის, გულის უკმარისობის, არითმიების, გულის გაჩერების და მწვავე კორონარული სინდრომის საერთო გაერთიანებული ინციდენტობა იყო 21%, 14%, 16%, 3.45% და 1.3%, შესაბამისად.[957] მიოკარდიუმის დაზიანების უფრო მაღალი მაჩვენებელი დაფიქსირდა შეერთებულ შტატებში (9%-დან 52%-მდე), ჩინეთთან შედარებით (7%-დან 28%-მდე).[958] კოხრეინის მიმოხილვამ აჩვენა, რომ გულ-სისხლძარღვთა სისტემის ყველაზე ხშირი გართულებები იყო გულის არითმიები, გულის უკმარისობა და არტერიული და ვენური ოკლუზიური მოვლენები.[175] უფრო იშვიათად, აღინიშნა ელვისებრი (ფულმინანტური) მიოკარდიტის, პერიკარდიტის, გულის ტამპონადის, ფილტვისმიერი გულის და ტაკოცუბოს სინდრომის შემთხვევები.[959] რისკის ფაქტორები მოიცავს ხანდაზმულ ასაკს, ჰიპერტენზიას, გულ-სისხლძარღვთა დაავადებებს და თირკმელების ქრონიკულ დაავადებას.[958]
ეტიოლოგია: COVID-19 ასოცირდება მაღალი ანთებითი დატვირთვით. მიოკარდიუმის ანთებამ შესაძლოა გამოიწვიოს მიოკარდიტი, გულის უკმარისობა, არითმიები, მწვავე კორონარული სინდრომი, მდგომარეობის სწრაფი გაუარესება და უეცარი სიკვდილი.[960][961]
დიაგნოზი: მიოკარდიუმის მწვავე დაზიანებაზე მიმანიშნებელი ნიშნებისა და სიმპტომების მქონე პაციენტებში, დიაგნოზის დასადგენად, ჩაატარეთ ეკგ და მაღალი მგრძნობელობის ტროპონინი I (hs-cTnI) ან T (hs-cTnT) და N-ტერმინალის პრო-თავის ტვინის ნატრიურეზული პეპტიდის (NT-proBNP) ტესტები. ჩამოთვლილი ტესტები შეიძლება დაგეხმაროთ დიაგნოსტიკაში: ეკგ ცვლილებები, რომლებიც მიუთითებს მიოკარდიუმის იშემიაზე; NT-proBNP დონე >400 ნანოგრამი/ლ; hs-cTnI ან hs-cTnT მაღალი დონე, განსაკუთრებით თუ დროთა განმავლობაში იმატებს. მომატებული ტროპონინი შეიძლება მიუთითებდეს გულის ანთებით რეაქციაზე მძიმე დაავადების დროს, და არა მწვავე კორონარულ სინდრომზე. მიიღეთ სპეციალისტი კარდიოლოგის რჩევები შემდგომი ტესტებისა და რადიოლოგიური კვლევების შესახებ.[397]
მართვა: მიმართეთ კარდიოლოგს მკურნალობის შესახებ რჩევებისთვის და მიჰყევით მკურნალობის ადგილობრივ პროტოკოლებს.[397] ამ ტიპის პაციენტებში სპეციფიკური მედიკამენტური მკურნალობისთვის რეკომენდაციის გასაწევად საკმარისი მონაცემები არ არსებობს. პაციენტის მართვაში ჩართული უნდა იყოს მულტიდისციპლინური გუნდი, მათ შორის ინტენსიური თერაპიის სპეციალისტები, კარდიოლოგები და ინფექციური დაავადებების სპეციალისტები.[962]
მონიტორინგი: მიოკარდიუმის საეჭვო ან დადასტურებული მწვავე დაზიანების მქონე ნებისმიერ პაციენტში საჭიროა არტერიული სისხლის წნევის, გულისცემის სიხშირისა და სითხეების ბალანსის მონიტორინგი, ასევე მუდმივი ეკგ მეთვალყურეობა. რეკომენდებულია მონიტორინგი ისეთ გარემოში, სადაც კარდიოლოგიური ან რესპირატორული გაუარესება სწრაფად დიაგნოსტირდება.[397] ლაბორატორიული ბიომარკერები შეიძლება დაგეხმაროთ გულ-სისხლძარღვთა გართულებების უფრო მაღალი რისკის მქონე პაციენტების გამოსავლენად. გულის ბიომარკერების მომატება და ახალი არითმიები შეიძლება დაკავშირებული იყო მძიმე დაავადებასთან და ინტენსიური მოვლის საჭიროებასთან.[963]
პროგნოზი: მიოკარდიუმის დაზიანება დაკავშირებულია არასასურველ კლინიკურ შედეგებთან და გადარჩენადობასთან. მომატებული ტროპონინი წარმოადგენს არასასურველ პროგნოზულ მაჩვენებელს და დაკაშირებულია სიკვდილობის მაღალ რისკთან.[958] დაფიქსირებული საერთო ლეტალობის მაჩვენებელი 9.6%.[955] ინფექციას შეიძლება ჰქონდეს გრძელვადიანი გავლენა ზოგად გულ-სისხლძარღვთა ჯანმრთელობაზე.[964] გულ-სისხლძარღვთა პრობლემები დაფიქსირდა ინფიცირებიდან 1 წლის განმავლობაში, მათ შორის, ვინც არ იყო ჰოსპიტალიზებული მწვავე ინფექციის გამო.[965]
თირკმელების მწვავე დაზიანება ხშირია, განსაკუთრებით კრიტიკულად დაავადებულ პაციენტებში. შეიძლება ნებისმიერ დროს განვითარდეს, ჰოსპიტალიზაციამდე, განმავლობაში და შემდეგაც.[397] COVID-19-ით კრიტიკულად დაავადებულ პაციენტებში რისკი უფრო დაბალია, გრიპის მქონე პაციენტებთან შედარებით.[966]
ეპიდემიოლოგია: თირკმლის მწვავე დაზიანების ჯამური ინციდენტობა შეფასებული იყო 19.45%-მდე; თუმცა, ინციდენტობა განსხვავდება კვლევების მიხედვით. პაციენტებს აქვთ მნიშვნელოვნად გაზრდილი ჰოსპიტალური სიკვდილობის რისკი (54.2%).[967] დამოუკიდებელი რისკფაქტორები: მამრობითი სქესი, ხანდაზმული ასაკი, მწეველობის ისტორია, სიმსუქნე, ჰიპერტენზია, დიაბეტი, პნევმოპათია, გულ-სისხლძარღვთა დაავადება, კიბო, თირკმელების ქრონიკული დაავადება, მექანიკური ვენტილაცია და ვაზოპრესორების გამოყენება.[968]
ეტიოლოგია: შესაძლო მიზეზებია ჰემოდინამიკური ცვლილებები, ჰიპოვოლემია, ვირუსული ინფექციები, რომლებიც თირკმლის მილაკოვან დაზიანებას იწვევს, თრომბოზული სისხლძარღვოვანი პროცესები, გორგლოვანი პათოლოგია ან რაბდომიოლიზი. შეიძლება უკავშირდებოდეს ჰემატურიას, პროტეინურიას, შრატში ელექტროლიტების დონის ცვლილებას (მაგ. კალიუმი, ნატრიუმი).[397]
დიაგნოზი: დააკვირდით პაციენტებს თირკმლის მწვავე დაზიანების დამახასიათებელ ნიშნებსა და სიმპტომებზე და გააგრძელეთ მართვა ადგილობრივი პროტოკოლების მიხედვით.
მართვა: მიჰყევით ადგილობრივ გაიდლაინებს თირკმლის მწვავე დაზიანების სამართავად. საჭიროა დამხმარე ზომები და სითხით მართვა.[967] კალიუმთან შემკავშირებლები შეიძლება გამოყენებული იყოს, როგორც ვარიანტები სტანდარტული მოვლასთან ერთად, მწვავე სიცოცხლისთვის საშიში ჰიპერკალიემიის გადაუდებელი მართვისთვის.[397] შეიძლება საჭირო გახდეს თირკმლის ჩანაცვლებითი თერაპია.
მონიტორინგი: თირკმლის მწვავე დაზიანების შემდეგ თირკმლის ქრონიკული დაავადების მქონე პაციენტის მონიტორინგი, სულ მცირე, 2 წელიწადის განმავლობაშია საჭირო.[397]
სიმპტომების გახანგრძლივება ხშირია მრავალი ვირუსული თუ ბაქტერიული ინფექციის, მათ შორის SARS-CoV-2 დროს.[969] შემთხვევის განსაზღვრებები განსხვავდება. ჯანმრთელობის მსოფლიო ორგანიზაცია განსაზღვრას ხანგრძლივ კოვიდს, როგორც მდგომარეობას, რომელიც გვხვდება SARS-CoV-2-ის შესაძლო ან დადასტურებული ინფექციის ანამნეზის მქონე ზრდასრულებში. იგი ჩვეულებრივ იწყება სიმპტომების გამოვლენიდან 3 თვეში და გრძელდება, სულ მცირე, 2 თვის განმავლობაში და ვერ იხსნება ალტერნატიული დიაგნოზით.[970] აშშ დაავადებათა კონტროლის და პრევენციის ცენტრების თანახმად, პოსტ-COVID მდგომარეობა არის ქოლგისებრი ტერმინი, რომელიც ჯანმრთელობის სხვადასხვა პრობლემებს მოიცავს, რაც მწვავე ინფექციიდან 4 კვირის განმავლობაში ვლინდება.[971]
სიმპტომები მრავალფეროვანია, შეიძლება გამოვლინდეს რეციდივი, რემისია და არაპროგნოზირებადი მიმდინარეობა. შეიძლება მსუბუქ შემთხვევებშიც გამოვლინდეს. ხშირი გრძელვადიანი სიმპტომები შეიძლება იყოს: მუდმივი ხველა, დაბალი ხარისხის ცხელება, ქოშინი, დაღლილობა, გულმკერდის ტკივილი/შებოჭილობა, პალპიტაცია, მიალგია, ართრალგია, თავის ტკივილი, მხედველობის ცვლილებები, სმენის დაქვეითება, ტინიტუსი, ყელის ტკივილი, გემოვნების/სუნის დაკარგვა, პერიფერიული ნეიროპათია, თავბრუსხვევა, ტრემორი, განწყობის ცვლილებები, კანის გამონაყარი, თმის ცვენა, სექსუალური დისფუნქცია, კუჭ-ნაწლავის სიმპტომები, ნეიროკოგნიტური სირთულეები, ძილის დარღვევა, დელირიუმი (ხანდაზმული ადამიანები) და ფსიქიკური ჯანმრთელობის პრობლემები.[972][973][974] 1-წლიანი მეთვალყურეობის შემდგომ ყველაზე ხშირი სიმპტომები იყო დაღლილობა, ოფლიანობა, დაჭიმულობა გულმკერდის არეში, შფოთვა და მიალგია.[975] გამოკვლევები მორგებული იუნდა იყოს კლინიკურ სურათზე. მათი საშუალებით უნდა გამოირიცხოს ნებისმიერი მწვავე ან სიცოცხლისთვის საშიში გართულება და ალტერნატიული დიაგნოზები.
ფარმაკოლოგიური ჩარევის მტკიცებულებები მწირია. მართვის მნიშვნელოვან ნაწილს წარმოადგენს პერსონალიზებული, მულტიდსციპლინური რეაბილიტაციის გეგმა, რომელიც მოიცავს რეაბილიტაციის ფიზიკურ, ფსიქოლოგიურ და ფსიქიატრიულ ასპექტებს. მიეცით რჩევები და ინფორმაცია თვითმართვის შესახებ, სიმპტომების თვითმართვის გზების ჩათვლით. შესაძლოა საჭირო გახდეს სპეციალისტთან მიმართვა იმ პაციენტებში, სადაც არის კლინიკური შეშფოთება.[973] ჯანმრთელობის მსოფლიო ორგანიზაცია რამდენიმე რეკომენდაციას იძლევა პოსტ-COVID-19 სინდრომის მქონე ზრდასრულების რეაბილიტაციისთვის.[85] კონსენსუსის გაიდლაინები ასევე ხელმისაწვდომია ფიზიკური მედიცინისა და რეაბილიტაციის ამერიკული აკადემიისგან.[976] მკურნალობის დროს პაციენტები უნდა იყვნენ დაკვირვების ქვეშ. გამოჯანმრთელების დრო განსხვავებულია, მაგრამ სიმპტომები, როგორც წესი, ქრება 12 კვირაში.
მიოკარდიტი ან პერიკარდიტი შეიძლება განვითარდეს მესენჯერული რნმ-ის ვაქცინებით აცრის შემდეგ.[977] ვარაუდობენ, რომ მესენჯერული რნმ-ის ვაქცინამ შეიძლება გააძლიეროს ანთება ენდოთელიუმზე, ასევე გულის კუნთის T- უჯრედების ინფილტრაცია; თუმცა საჭიროა შემდგომი კვლევა, რადგან სხვადასხვა მექანიზმებია ნავარაუდები.[978][979] არსებობს მიზეზობრივი კავშირის მაღალი ალბათობა, აუტოფსიის კვლევების მიხედვით.[980] შემთხვევები ასევე დაფიქსირდა ადენოვირუსული ვექტორული ვაქცინების და ცილის ქვეერთეულოვანი ვაქცინების გამოყენებისას, თუმცა უფრო იშვიათად.[981][982]
ეპიდემიოლოგია: მიოკარდიტის სიხშირე შეიძლება იყოს 140 შემთხვევა მილიონ დოზაზე, ასაკისა და სქესის მიხედვით. ყველაზე მაღალი რისკის ქვეშ არიან მამრობითი სქესის მოზარდები და ახალგაზრდები; სიხშირე ყველაზე მაღალია 12-დან 29 წლამდე ასაკის მამაკაცებში. მიოკარდიტი უფრო ხშირია Moderna ვაქცინის გამოყენებისას, ვიდრე Pfizer/BioNTech ვაქცინის შემდეგ. უფრო ხშირად ვითარდება მეორე დოზის შემდეგ (მესამე დოზის შემდეგ სიხშირის მონაცემები შეზღუდულია, თუმცა მწარმოებელი აცხადებს, რომ რისკის პროფილი მსგავსია მეორე დოზის შემდეგ არსებული რისკისა). საშუალოდ, სიმპტომები იწყებოდა ვაქცინის მიღებიდან 2-დან 4 დღის შემდეგ, თუმცა დაფიქსირდა 20 დღემდე (ან მეტი) ინტერვალიც. სიხშირე მეორე დოზის შემდეგ შეიძლება იყოს უფრო დაბალი, როცა მეორე დოზა კეთდება პირველი დოზის მიღებიდან ≥31 დღის შემდეგ, ვიდრე ≤30 დღის შემდეგ ახალგაზრდა ასაკობრივ ჯგუფებში. პერიკარდიტის შესახებ მონაცემები მწირი იყო, მაგრამ დაფიქსირდა პაციენტის ასაკის, სქესის, დაწყების დროის და ჰოსპიტალიზაციის სიხშირის უფრო მეტი ვარიაბელობა, ვიდრე მიოკარდიტის შემთხვევაში.[979] რეალური, საზოგადოებრივი მონაცემებით, 5-დან 11 წლამდე ასაკის ბავშვებში მიოკარდიტის გაზრდილი რისკი ჯერჯერობით არ გამოვლენილა.[983][984] დაფიქსირებული მაჩვენებლები იმუნოკომპრომისის მქონე ადამიანებში მსგავსი იყო საერთო პოპულაციისა.[985] ვაქცინირებულ პირებს მიოკარდიტი/პერიკარდიტის განვითარების ორჯერ მეტი რისკი ჰქონდათ SARS-CoV-2 ინფექციის არარსებობის შემთხვევაში, ვიდრე არავაქცინირებულ პირებს 30-დღიანი შემდგომი პერიოდის განმავლობაში.[986]
დიაგნოზი: განიხილეთ ეს დიაგნოზი ბავშვებში, მოზარდებში ან ზრდასრულებში, რომლებსაც აღენიშნებათ ახალი, აუხსნელი ტკივილი გულმკერდის არეში, ტაქიკარდია ან ტაქიპნოე, დისპნოე, გულის ფრიალი, თავბრუსხვევა ან სინკოპე, ან ზოგადი სიმპტომები, ვაქცინაციიდან 10 დღის განმავლობაში (შენიშვნა: მდგომარეობა შეიძლება განვითარდეს აცრიდან 10 ან მეტი დღის შემდეგაც).[987] ყველაზე ხშირი პირველი სიმპტომი იყო გულმკერდის არეში ტკივილი (34.5%).[988]
გამოკვლევები: შეუკვეთეთ 12-განხრიანი ეკგ, ანთებითი სისხლის მარკერები, სისხლის საერთო ანალიზი და ტროპონინი. თუ ეკგ ან ტროპონინი ნორმაში არ არის, განიხილეთ მართვის გეგმა კარდიოლოგებთან. შემდგომი გამოკვლევები (მაგ., გულის რადიოლოგიური კვლევები და რიტმის მონიტორინგი) და შემდგომი დაკვირვება უნდა ჩატარდეს კარდიოლოგთა ჯგუფის მიერ.[987] ყველაზე ხშირი მიგნებები იყო ST ინტერვალთან დაკავშირებული ცვლილებები ელექტროკარდიოგრამაზე (58.7%) და ჰიპოკინეზია გულის მაგნიტურ-რეზონანსულ ტომოგრაფიაზე ან ექოკარდიოგრაფიაზე (50.7%). ლაბორატორიული შედეგები მოიცავდა ტროპონინ I-ის მომატებულ დონეს (81.7%) და მომატებულ C-რეაქტიულ პროტეინს (71.5%).[988]
მართვა: მძიმე ფიზიკური აქტივობა თავიდან უნდა იქნას აცილებული სიმპტომების გაუმჯობესებამდე.[987] პაციენტებმა უნდა მიმართონ კარდიოლოგს, რადგან მკურნალობა დამოკიდებულია კლინიკურ სურათზე.
პროგნოზი: მოზარდებისა და ახალგაზრდების 93%-მდე საჭიროებს ჰოსპიტალიზაციას. ინტენსიური თერაპიის განყოფილებაში მართვას საჭიროებს პაციენტების 25%-მდე. მედიანური ინტერვალი დაწყებიდან ფიზიკური აქტივობის გაგრძელებამდე იყო 98 დღე. პაციენტების დაახლოებით 81%, რომლებმაც დაასრულეს შემდგომი გამოკითხვა, ჩაითვალა გამოჯანმრთელებულად დაკვირვების დაწყებიდან არაუმეტეს 90 დღის განმავლობაში. თუმცა, პაციენტების დაახლოებით ნახევარი აგრძელებდა სიმპტომების აღნიშვნას (მაგ. გულმკერდის არეში ტკივილი) და 25%-ს ენიშნებოდა ყოველდღიური მედიკამენტები.[989] მძიმე და პოტენციურად ფატალური მიოკარდიტი დაფიქსირდა ვაქცინასთან დაკავშირებული მიოკარდიტის ყველა შემთხვევის 19.8%-ში ერთ კორეულ კვლევაში. ზოგიერთ პაციენტს დასჭირდა ინტენსიური თერაპიის განყოფილებაში გადაყვანა, ექსტრაკორპორალური მემბრანული ოქსიგენაცია და გულის ტრანსპლანტაცია.[990]
მიმართეთ თქვენს ადგილობრივ საზოგადოებრივი ჯანდაცვის ორგანოს COVID-19 ვაქცინის შემდგომი დოზების ადმინისტრირების შესახებ მითითებისთვის. ზოგიერთმა ქვეყანამ დანერგა ასაკთან დაკავშირებული შეზღუდვები მესენჯერული რნმ ვაქცინებისთვის მიოკარდიტის/პერიკარდიტის რისკის გამო. მესენჯერული რნმ ვაქცინის პროგრამების მოდიფიკაციამ, რომელიც ითვალისწინებს პროდუქტის ასაკზე დაფუძნებულ საკითხებს და ხანგრძლივ დოზებს შორის ინტერვალებს, შეიძლება შეამციროს მიოკარდიტის/პერიკარდიტის რისკი.[991]
ღვიძლის დაზიანება შეიძლება ასოცირებული იყოს ღვიძლის უკვე არსებულ დაავადებათან, ვირუსულ ინფექციასთან, წამლის ტოქსიკურობასთან, სისტემურ ანთებასთან, ჰიპოქსიასთან ან ჰემოდინამიკურ პრობლემებთან; თუმცა, გაურკვეველია ძირითადი მექანიზმი. ჯამური პრევალენტობა არის 25%, თუმცა ამ პაციენტებში არ არსებობს ღვიძლის დაზიანების ერთიანი განმარტება და პრევალენტობა დამოკიდებულია კვლევებში გამოყენებულ განსაზღვრებაზე. დიაგნოზის მკაცრი კრიტერიუმების გამოყენებისას, ჯამური პრევალენტობა შეიძლება იყოს 9% -მდეც. მომატებული ალანინამინოტრანსფერაზას და ასპარტატ ამინოტრანსფერაზას პრევალენტობაა, შესაბამისად, 19% და 22%. ჰიპერტრანსამინაზემიის პრევალენტობა უფრო მაღალია მძიმე დაავადების მქონე პაციენტებში, ვიდრე არამძიმე დაავადების მქონე პაციენტებში.[992] ღვიძლის ფუნქციის პათოლოგიური ტესტები დაკავშირებულია მნიშვნელოვნად მაღალ სიკვდილობასთან, ინტენსიური თერაპიის განყოფილებაში გადაყვანასა და მექანიკურ ვენტილაციასთან.[993] კიდევ ერთი მეტა-ანალიზის დასკვნის თანახმად, დღემდე არსებული ობსერვაციული კვლევების და შემთხვევების ანგარიშების მონაცემების საფუძველზე, ტრანსამინაზების და საერთო ბილირუბინის დონე არ ახდენს მნიშვნელოვან გავლენას COVID-19-ის მქონე პაციენტების მდგოამრეობაზე.[994]
ღვიძლის მძიმე დაზიანების რისკფაქტორებია: ხანდაზმული ასაკი, ღვიძლის ფონური დაავადება, მძიმე დაავადება.[995] COVID-19-ის სამკურნალო მედიკამენტებს (მაგ., რემდესივირი, ტოცილიზუმაბი) შესაძლოა ჰქონდეთ მავნე ეფექტი ღვიძლის დაზიანებაზე.[996] გამოქვეყნებულია ღვიძლის დაზიანების მართვის გაიდლაინები COVID-19-ის მქონე პაციენტებში.[997]
ნევროლოგიური გართულებები მოიცავს მწვავე ცერებროვასკულურ დაავადებას, ცნობიერების დაქვეითებას, ატაქსიას, კრუნჩხვებს, ეპილეფსიის სტატუსს, ენცეფალოპათიას, ენცეფალიტს და მენინგოენცეფალიტს, მწვავე დისემინირებულ ენცეფალომიელიტს, კორტიკოსპინალური ტრაქტის ნიშნებს, მადემიელინიზებელ დაზიანებებს, ცერებრალურ ნეიროპათიებს, პარკინსონიზმს, ცერებრული ვენური სინუსის თრომბოზს, მიოპათიას, გიენ-ბარეს სინდრომს, დემენციას და ტვინის მაგნიტურ-რეზონანსული ტომოგრაფიის პათოლოგიურ შედეგებს.[998][999] დაფიქსირდა პირის წვის სინდრომი და თვალის წვის სინდრომი.[1000]
პაციენტებში ხშირია ცენტრალური ან პერიფერიული ნევროლოგიური გართულებები, რაც სავარაუდოდ უკავშირდება ცენტრალურ ნერვულ სისტემაში ვირუსის ინვაზიას, ანთებით რეაქციას ან იმუნურ დისრეგულაციას.[1001] ნევროლოგიური გართულებები გვხვდება მთელი სიცოცხლის განმავლობაში ინფექციის კონტექსტში, ცნობილი თანმხლები დაავადებებით და მის გარეშე, და დაავადების ყველა სიმძიმის ფონზე (უსიმპტომო პაციენტების ჩათვლით).[1002] პაციენტებმა კლინიკას შეიძლება ამ სიმპტომებით მიმართონ, ან დაავადების მოგვიანებით ეტაპზე გამოუვლინდეთ. ნევროლოგიური გართულებები, როგორც წესი, ვითარდება რესპირატორული დაავადების გამოვლენიდან 1-2 კვირაში.[1003] წინმსწრები ნევროლოგიური დაავადებების მქონე პაციენტებს შესაძლოა განუვითარდეთ ნევროლოგიური სიმპტომების გამწვავება.[1004] შესაძლებელია გახანგრძლივებული შედეგების არსებობა.[1005][1006]
ეპიდემიოლოგია: დაფიქსირებულია პაციენტების 22%-35%-ში. ცენტრალური ნერვული სისტემის გამოვლინებები უფრო გავრცელებული იყო, ვიდრე პერიფერიული ნერვული სისტემის მანიფესტაციები.[998] ნევროლოგიური ჩართულობა ხშირია ბავშვებსა და მოზარდებში (21 წლამდე ასაკის პაციენტებში 22%).[1007]
მწვავე ცერებროვასკულური დაავადება: (მოიცავს იშემიურ ინსულტს, ჰემორაგიულ ინსულტს, ცერებრულ ვენურ თრომბოზს და გარდამავალ იშემიურ შეტევას) აღწერილია პაციენტების 0.5-5.9%-ში. ყველაზე გავრცელებული ტიპი იყო იშემიური ინსულტი (0.4% -დან 4.9%-მდე).[1001] თუმცა, ინსულტის საერთო აბსოლუტური ინციდენტობა სტაციონარში იყო 0.175%, უფრო დაბალი, ვიდრე წინა ობსერვაციულ კვლევებში.[1008] დაავადების მძიმე ფორმის მქონე პაციენტებში უფრო მაღალია იშემიური ინსულტის რისკი, ვიდრე შედარებით მსუბუქი ფორმის დაავადების მქონე პირებში.[1009] ინსულტი შედარებით ხშირია ჰოსპიტალიზებულ პაციენტებში სხვა რესპირატორულ ვირუსულ ინფქეციებთან შედარებით და ახასიათებს ჰოსპიტალური სიკვდილობის მაღალი რისკი. რისკფაქტორებია ხანდაზმულობა და მამრობითი სქესი. COVID-19-ის სიმპტომების დაწყებიდან ინსულტის განვითარებამდე საშუალო დრო შეადგენდა 8 დღეს.[1010][1011] ინსულტი დაავადების მძიმე ფორმის გვიანდელ, ხოლო მსუბუქი და საშუალო ფორმის დაავადების ადრეულ ეტაპზე გვხვდება.[1012] პაციენტებს შეიძლება ჰქონდეთ იშემიური ინსულტი ინფექციის გამოჯანმრთელების ეტაპის დროს, მათ შორის უფრო ახალგაზრდა ასაკშიც (<50), უსიმპტომო ან ნაკლებ-სიმპტომური COVID-19-ის შემთხვევებშიც.[1013] როგორც ჩანს, იშემიური ინსულტი უფრო მძიმეა და უარეს გამოსავალთანაა დაკავშირებული (მძიმე უნარშეზღუდვა) COVID-19-ის მქონე პაციენტებში. NIH-ის ინსულტის ქულის მედიანა უფრო მაღალია COVID-19 პაციენტებში, ვიდრე ინფექციის არმქონე ჯგუფებში.[1014] გამოქვეყნებულია მწვავე იშემიური ინსულტის მართვის გაიდლაინები COVID-19-ის მქონე პაციენტებში.[1015]
აღწერილია გიენ-ბარეს სინდრომი:დაფიქსირებულია როგორც პოსტინფექციური, ასევე ინფექციამდელი ფორმები.[1001] ჯამური პრევალენტობა ჰოსპიტალიზებულ და არა-ჰოსპიტალიზებულ პაციენტებში იყო 0.15%.[1016] გიენ-ბარეს სინდრომის დაწყების საშუალო ასაკი იყო 55 წელი. პაციენტების უმეტესობას ჰქონდა COVID-19-ის მძიმე რესპირატორული სიმპტომები, თუმცა უსიმპტომო პაციენტებშიც აღიწერა. ხშირია კლასიკური სენსორიმოტორული ფორმის მაღალი პრევალენტობა და მწვავე ანთებითი დემიელინიზაციური პოლინეიროპათია, თუმცა იშვიათი ფორმებიც შეიძლება გამოვლინდეს.[1017] პაციენტებს აღენიშნებოდათ დემიელინიზაციით მიმდინარე ქვეტიპების განვითარების მომატებული რისკის. კლინიკური შედეგები მსგავსია იმავე დროს ან წარსულში შერჩეული კონტროლის შედეგებთან, რომლებიც არ არიან/იყვნენ ინფიცირებული SARS-CoV-2-ით.[1016] გიენ-ბარეს სინდრომი ასევე დაკავშირებულია COVID-19 ვაქცინების გამოყენებასთან.[1018]
ენცეფალიტი: ფიქსირდება პაციენტთა <1%-ში, თუმცა კრიტიკულ პაციენტებში მაჩვენებელი 6.7%-ს აღწევს. ენცეფალიტი იწვევს არასასურველი კლინიკური შედეგების რისკის მატებას, მათ შორის ჰოსპიტალზიაციას ინტენსიურ განყოფილებაში, მექანიკური ვენტილაციის საჭიროებას, სიკვდილობის ზრდას (13.4%) COVID-19 პაციენტების ზოგად პოპულაციასთან შედარებით.[1019] აღწერილია აუტოიმუნური ენცეფალიტის იშვიათი შემთხვევები.[1020]
ნევროლოგიური გართულებების მართვის ამოსავალი წერტილი არის დეტალური ანამნეზი და გასინჯვა, ლაბორატორიული და რადიოლოგიური მონაცემების შესაბამისი ინტერპრეტაციით. უმეტეს შემთხვევაში, ამ მდგომარეობების მართვა უნდა შეესაბამებოდეს COVID-19-მდე არსებულ გაიდლაინებს.[1021]
ჰოსპიტალური გულის გაჩერება ხშირია კრიტიკულ პაციენტებში და ხასიათდება ცუდი გადარჩენადობით, განსაკუთრებით ხანდაზმულ პაციენტებში. 5019 კრიტიკულად დაავადებულ COVID-19 მქონე პაციენტს შორის, 14%-ს განუვითარდა გულის გაჩერება. რისკფაქტორებია ხანდაზმული ასაკი, მამრობითი სქესი, თანმხლები დაავადებების არსებობა და ჰოსპიტალიზაცია კლინიკაში, სადაც ინტენსიური განყოფილების საწოლების რიცხვი დაბალია. პაციენტთა დაახლოებით 57%-ს ჩაუტარდა გულ-ფილტვის რეანიმაცია. რეანიმაციის დროს ყველაზე ხშირად ფიქსირდებოდა უპულსო ელექტრული აქტივობა (49.8%) და ასისტოლია (23.8%). რეანიმაციის შემდეგ პაციენტთ 12% გაიწერა კლინიკიდან, მათ შორის უმრავლესობა 45 წელზე უმცროსი ასაკის იყო.[1022]
[Figure caption and citation for the preceding image starts]: გულის გაჩერება COVID-19-ის დროსBMJ. 2020;371:m3513 [Citation ends].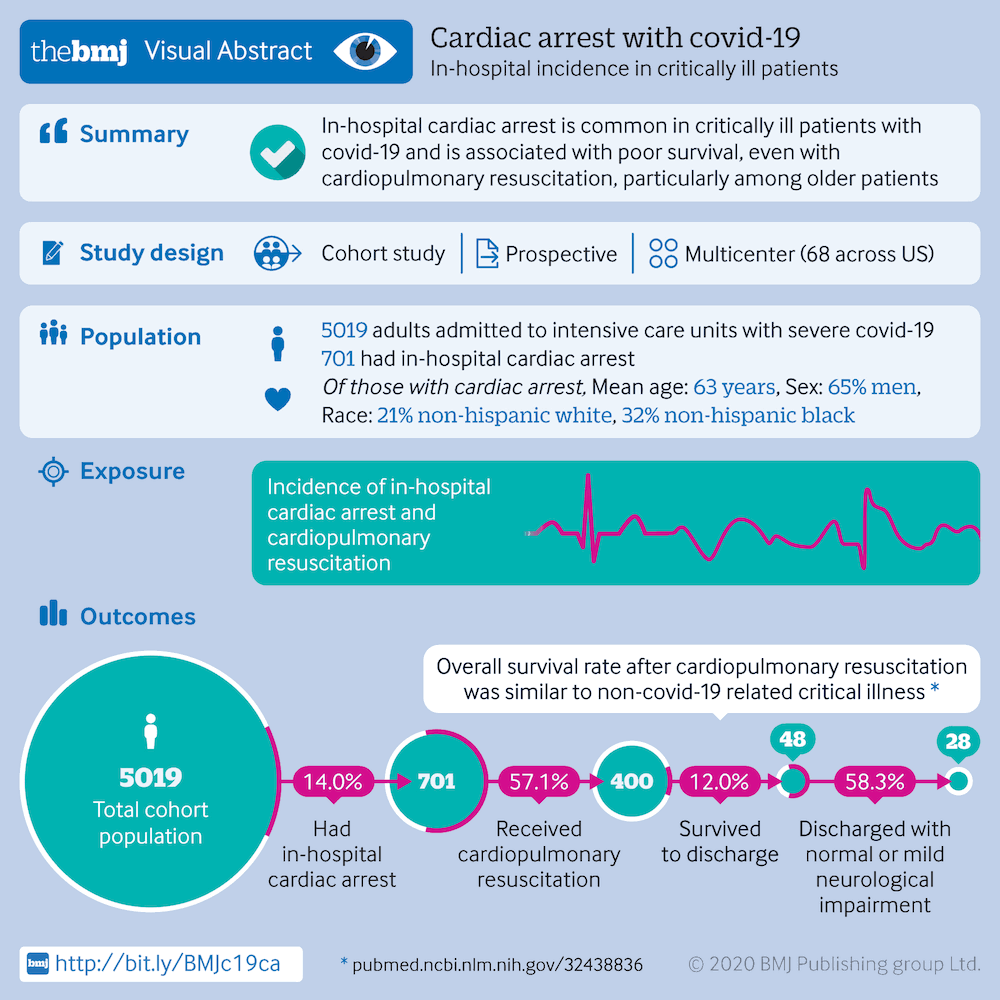
ორსულობის შედეგი, როგორც წესი, კეთილსაიმედოა, თუმცა მონაცემები არასაკმარისია ვირუსთნ ორსულობის ადრეულ ეტაპზე ექსპოზიციასთან დაკავშირებით.[220] გართულებების რისკი უფრო მაღალი იყო ორსულ ქალებში, რომლებიც იყვნენ სიმპტომატურნი.[1023] როგორც ჩანს, დედასა და ახალშობილებში გართულებების რისკი არსებითად ნაკლები იყო ომიკრონის დომინანტური პერიოდის განმავლობაში, ვიდრე ომიკრონამდე პერიოდში.[1024] უფრო დაბალი შემოსავლის მქონე ქვეყნებმა დააფიქსირეს დედების ინტენსიური თერაპიის განყოფილებაში მიღების და სიკვდილობის და მკვდრადშობადობის უფრო მაღალი მაჩვენებლები, ვიდრე უფრო მაღალი შემოსავლის მქონე ქვეყნებმა.[1025]
დედის კლინიკური შედეგები: ინტენსიური თერაპიის განყოფილებაში მოთავსების, ინვაზიური ვენტილაციისა და ექსტრაკორპორალური მემბრანის ჟანგბადის საჭიროება უფრო მაღალი იყო ორსულ და ახლახანს ნამშობიარებ ქალებში, ვიდრე არაორსულ, რეპროდუქციული ასაკის ქალებში. ორსულ ქალებში გარდაცვალების რისკი შეიძლება იყოს უფრო მაღალი. სერიოზული გართულებების რისკფაქტორებში შედის არსებული თანმხლები დაავადებები (მაგ., ქრონიკული ჰიპერტენზია, დიაბეტი), დედის უფროსი ასაკი, არა-თეთრკანიანი ეთნიკურობა, ორსულობის სპეციფიკური მდგომარეობების არსებობა (მაგ., გესტაციური დიაბეტი, პრეეკლამფსია) და სხეულის მასის მაღალი ინდექსი.[218][219][1026] გესტაციური დიაბეტის, გესტაციური ჰიპერტენზიის, ნაყოფის არასასურველი ზრდისა და პრეეკლამფსიის სტატისტიკურად მნიშვნელოვანი მაღალი რისკი დაფიქსირდა ორსულ ქალებში პანდემიის პერიოდში პანდემიამდელ პერიოდთან შედარებით.[1027]
სპონტანური აბორტი:არ არსებობს მტკიცებულება იმისა, რომ ინფექცია პირველ ან მეორე ტრიმესტრში ზრდის აბორტის რისკს. თუმცა, აუცილებელია შემდგომი კვლევების ჩატარება.[1028]
ნაადრევი მშობიარობა:COVID-19-ის მქონე ორსულებში, არაინფიცირებულ ორსულებთან შედარებით, ნაადრევი მშობიარობა უფრო ხშირია. თუმცა, ჯამში სპონტანური ნაადრევი მშობიარობის სიხშირე COVID-19-ის მქონე ორსულებში პრე-პანდემიური სიხშირის მსგავსია, ანუ ეს შემთხვევები შეიძლება არ იყოს ინფექციით განპირობებული.[218][219][1026]
სპონტანური აბორტი ან ნეონატალური სიკვდილი: მკვდრადშობადობის და ახალშობილთა სიკვდილობის საერთო მაჩვენებლები, როგორც ჩანს, არ არის უფრო მაღალი, ვიდრე ფონური მაჩვენებლები.[218][219][1029][1030] თუმცა, მონაცემები წინააღმდეგობრივია. ინლისში, წინა წლის იმავე თვეებთან შედარებით, არ ფიქსირდება სპონტანური აბორტის მომატებული შემთხვევები რეგიონულად თუ ეროვნული მასშტაბით, მსხვადასხვა რეგიონში საზოგადოებრივი ინფექციის ვარიაბელური სიხშირის მიუხედავად.[1031] 2020 წლის მარტიდან 2021 წლის სექტემბრამდე პერიოდში ,თუმცა, აშშ-ში, COVID-19-ით დაავადებულ ქალებს ჰქონდათ მკვდრადშობადობის გაზრდილი რისკი COVID-19-ის არმქონე ქალებთან შედარებით, კავშირი უფრო ძლიერი იყო დელტას ვარიანტის დომინირების დროს.[1032] სკანდინავიურმა რეესტრის კვლევამ ასევე აჩვენა მკვდრადშობადობის მომატებული რისკი გესტაციის 22 კვირის შემდეგ, განსაკუთრებით ქალებში, რომლებიც ინფიცირებულნი არიან დელტას ვარიანტით.[1033] ინდივიდუალური მონაწილეების მონაცემების მეტა-ანალიზმა ვერ დაადგინა კავშირი ორსულობის დროს ინფექციას და მკვდრადშობადობის მომატებულ რისკს შორის გესტაციის 28 კვირაში ან მის შემდეგ. კავშირი არ დადასტურდა არც საშვილოსნოსშიდა ზრდის შეზღუდვასთან.[1034] სხვა მეტა-ანალიზმა აღმოაჩინა მკვდრადშობადობის მომატებული რისკი.[1035]
ნეონატალური ინფქეცია: შეზღუდული რაოდენობის, დაბალი ხარისხის მტკიცებულებების თანახმად, ახალშობილებში ინფექციის რისკი უკიდურესად დაბალია. ინფექციათა უმეტესობის შეძენა პოსტნატალურ პერიოდში ხდება, თუმცა ფიქსირდება ინფექციის თანდაყოლილი შემთხვევებით. ბავშვებისგან განსხვავებით, რომელთაც, როგორც წესი, ასიმპტომური ინფექცია აქვთ, ახალშობილებში შემთხვევათა 2/3 სიმპტომურია და მათ მნიშვნელოვან ნაწილს ესაჭიროება ინტენსიური მკურნალობა. თუმცა, მათი საერთო პროგნოზი შესანიშნავია.[218][219][1026][1036][1037]
ახალშობილთა კლინიკური გამოსავალი: არსებობს შეზღუდული და წინააღმდეგობრივი მტკიცებულება ახალშობილთა მოკლევადიანი ან გრძელვადიანი ავადობის (მაგ., რესპირატორული დაავადება) მომატებული რისკის შესახებ და საჭიროა შემდგომი კვლევების ჩატარება.[1030] არსებობს გარკვეული მტკიცებულება, რომ დედის ინფექციას და პერინატალურ გადაცემას აქვს პოტენციალი გავლენა მოახდინოს ახალშობილის სმენის სისტემაზე, განსაკუთრებით ორსულობის მეორე და მესამე ტრიმესტრში. თუმცა, მონაცემები შეზღუდული და არათანმიმდევრულია და საჭიროა შემდგომი კვლევა.[1038]
სეფსისი (დიაგნოსტიდება სეფსისი-3 კრიტერიუმებით ან ინფექციასთან დაკავშირებული ორგანული უკმარისობის არსებობით, რომელიც საჭიროებს მხარდაჭერას/ჩანაცვლებას) აღწერილია ინტენსიურ განყოფილებაში მყოფი პაციენტების 78%-ში და ჰოსპიტალიზებული პაციენტების 33%-ში.[1039]
გაიდლაინები შოკის მართვისთვის COVID-19-ით კრიტიკულად დაავადებულ პაციენტებში გვირჩევენ კონსერვატიულ გადასხმის სტრატეგიას და ვაზოაქტიურ აგენტს. ნორადრენალინი (ნორეპინეფრინი) არის უპირატესი პირველი რიგის აგენტი მოზრდილებში (ადრენალინი [ეპინეფრინი] ან ნორადრენალინი შეიძლება გამოიყენოთ ბავშვებში). ნორადრენალინს შეგვიძლია დავამატოთ ვაზოპრესინი ან ადრენალინი (ეპინეფრინი) ზრდასრულებში, თუ სამიზნე საშუალო არტერიული წნევა ვერ მიიღწევა მხოლოდ ნორადრენალინის გამოყენებით.[694] დამატებითი ინფორმაციისთვის გაეცანით ადგილობრივ გაიდლაინებს.
დისემინირებული სისხლძარღვშიგა შედედება წარმოადგენს კოაგულაციური უკმარისობის გამოვლინებას და შუალედურ რგოლს მულტიორგანული უკმარისობის ჩამოყალიბებაში. პაციენტებს შესაძლოა ჰქონდეთ სისხლდენის/ჰემორაგიის ან ვენური თრომბოემბოლიის მაღალი რისკი.[1040] დისემინირებული სისხლძარღვშიდა შედედების ჯამური ინციდენტობა შეადგენს 3%-ს და დაკავშირებულია არასასურველ პროგნოზთან. ინციდენტობა უფრო მაღალია დაავადების მძიმე ფორმის და ინტენსიურ განყოფილებაში მოთავსებულ პაციენტებში და ასევე მათში, ვისაც დაუდგა ლეტალური შედეგი, გადარჩენილებთან შედარებით.[1041] COVID-19-თან ასოცირებული კოაგულოპათია, როგორც ჩანს, განსხვავდება დისემინირებული სისხლძარღვშიდა შედედება, თუმცა დისემინირებული სისხლძარღვშიდა შედედება დაფიქსირდა მძიმედ დაავადებულ პაციენტებში. კოაგულაციის ცვლილებები COVID-19 პაციენტებში მსგავსია, მაგრამ არ არის დისემინირებული სისხლძარღვშიდა შედედების იდენტური, და პაციენტების უმრავლესობა არ აკმაყოფილებს დისემინირებული სისხლძარღვშიგა შედედების ჩვეულებრივი ფორმების კრიტერიუმებს.[1042]
კოაგულოპათია ვლინდება მომატებული ფიბრინოგენისა და D-დიმერის, პროთრომბინის დროის, პარციალური თრომბოპლასტინის დროისა და თრომბოციტების რაოდენობის მინიმალური ცვლილებების სახით. ინტერლეიკინ-6-ის მატება კორელირებს ფიბრინოგენის დონის მატებასთან. კოაგულოპათია, როგორც ჩანს, უკავშირდება ავადმყოფობის სიმძიმეს და შედეგობრივ თრომბოანთებას. D-დიმერის დონე ყურადღებით გააკონტროლეთ.[1043]
დაბალმოლეკულური ჰეპარინით ან არაფრაქციული ჰეპარინით ანტიკოაგულაციური თერაპია ასოცირდება უკეთეს პროგნოზთან მძიმე COVID-19-ის მქონე პაციენტებში, რომელთაც აღენიშნებათ სეფსისით ინდუცირებული კოაგულოპათიის ქულა ≥4 ან გამოხატულად მაღალი D-დიმერის დონე.[1044] ჰეპარინით ინდუცირებული თრომბოციტოპენიის მქონე (ან ანამნეზის მქონე) პაციენტებში რეკომენდებულია არგატრობანი ან ბივალირუდინი.[1040]
სისხლდენის შემთხვევაში უნდა იხელმძღვანელოთ დისემინირებულ სისხლძარღვშიგა შედედებასთან ან სეპტიკურ კოაგულოპათიასთან დაკავშირებული სისხლდენის მართვის სტანდარტული გზამკვლევით; თუმცა, სისხლდენა სხვა ასოცირებული ფაქტორების გარეშე იშვიათია.[1043][1045]
სიკვდილის წამყვანი მიზეზი არის სუნთქვის უკმარისობა, რომელიც მწვავე რესპირატორული დისტრესსინდრომითაა განპირობებული.[860] COVID-19-ით გამოწვეული მწვავე რესპირატორული დისტრეს სინდრომის საერთო გაერთიანებული პრევალენტობა გლობალურად იყო 32%.[1046] ბავშვებში შეიძლება სწრაფად განვითარდეს სუნთქვის უკმარისობა.[1047] COVID-19-ის მქონე პაციენტებში შესაძლოა გაზრდილი იყოს ვენტილაციასთან დაკავშირებული პნევმონიის რისკი, დაუინფიცირებელ პაციენტებთან შედარებით. საერთო ჯამში, ხელოვნურ სუნთვასთან დაკავშირებული პნევმონია დაფიქსირდა მექანიკური ვენტილაციის ქვეშ მყოფი პაციენტების 48.2%-ში, ხოლო სიკვდილობა შეადგენდა 51.4%-ს.[1048]
ჰაერის გაჟონვა (პნევმოთორაქსი, პნევმომედიასტიუმი და კანქვეშა ემფიზემა) ასოცირდება უფრო მაღალ სიკვდილობასთან და ხანგრძლივ ყოფნასთან საავადმყოფოში, განსაკუთრებით ხანდაზმულებში. გართულება შეიძლება განვითარდეს დადებითი წნევის ვენტილაციის გარეშეც. ეს ძირითადად გამოწვეულია დაავადების პროგრესირებით, რაც იწვევს ფილტვის პარენქიმის ანთებას და ვენტილაციის სტრესით ალვეოლების დაზიანებას. ინციდენტობა მნიშვნელოვნად განსხვავდება კვლევების მიხედვით და იმატებს დაავადების სიმძიმის მიხედვით. პაციენტების საშუალო ასაკი იყო 58 წელი და 75% იყო მამაკაცი. ჰიპერტენზია იყო ყველაზე გავრცელებული თანმხლები დაავადება, რასაც მოყვებოდა დიაბეტი. იზოლირებული პნევმოთორაქსი იყო ჰაერის გაჟონვის ყველაზე ხშირი ტიპი (48.5%), პაციენტთა 17%-ს განუვითარდა სპონტანური პნევმოთორაქსი. სიკვდილობა იყო 40%. საჭიროა შემდგომი კვლევა.[1049]
მძიმე დაავადების მქონე ზოგიერთ პაციენტს აქვს ციტოკინების გამოთავისუფლების სინდრომის მსგავსი არარეგულირებული ანთებითი პასუხის ლაბორატორიული მაჩვენებლები, რომელიც ხასიათდება პლაზმური გაჟონვით, სისხლძარღვთა გამტარიანობის გაზრდით, დიფუზური სისხლძარღვშიდა შედედებით და იმუნოდეფიციტით. ამ პაციენტებში პროგნოზი არასახარბიელოა. ამ პაციენტებში გამოვლენილია პროანთებითი ციტოკინების, განსაკუთრებით ინტერლეიკინ-6-ის მაღალი დონე შრატში. შეიძლება განვითრებული იყოს მეორადი ჰემოფაგოციტური ლიმფოჰისტიოციტოზის მახასიათებლები. მკურნალობის ვარიანტები მოიცავს ინტერლეიკინ-6 ინჰიბიტორებს (მაგ., ტოცილიზუმაბს), იანუს კინაზას ინჰიბიტორებს (მაგ., ბარიციტინიბი) და ანაკინრას.[1050]
ასევე იხილეთ ბავშვთა ანთებითი მულტისისტემური სინდრომი, ციტოკინის გამოთავისუფლების სინდრომის მსგავსი დაავადება ბავშვებში, ქვემოთ.
ასევე ცნობილია, როგორც პედიატრიული მულტისისტემური ანთებითი სინდრომი, რომელიც ქრონოლოგიურად დაკავშირებულია SARS-CoV-2 ინფექციასთან. არსებობს სახელწოდების სხვადასხვა ვარიაციები. ასევე დაფიქსირდა მულტისისტემური ანთებითი სინდრომი მოზრდილებში (MIS-A), თუმცა უფრო იშვიათად.[1051]
განმარტება: იშვიათი, მაგრამ მძიმე დაგვიანებული გართულება, რომელიც შეიძლება განვითარდეს ბავშვებში და მოზარდებში მწვავე ინფექციის დაწყებიდან დაახლოებით 3-დან 4 კვირამდე (ან უფრო გვიან), სავარაუდოდ პოსტინფექციური ანთებითი პროცესის გამო. სინდრომი ჰგავს, მაგრამ განსხვავდება კავასაკის დაავადებისგან და ასევე იზიარებს საერთო მახასიათებლებს ტოქსიკური შოკის სინდრომთან. სინდრომს დროის კუთხით აქვს მჭიდრო კავშირი SARS-CoV-2-ის ინფექციასთან.[1052] შემთხვევის განსაზღვრება ზოგადად მოიცავს ცხელების არსებობას, მომატებულ ანთებით მარკერებს, მულტიორგანულ დისფუნქციას, SARS-CoV-2-ის მიმართ დადებითი ტესტის ანამნეზს (ან მჭიდრო კონტაქტს დადასტურებულ შემთხვევასთან) და სარწმუნო ალტერნატიული დიაგნოზის არარსებობას. თუმცა, შემთხვევის განსაზღვრებები განსხვავდება.[428][1053] იშვიათად შეიძლება მოხდეს COVID-19 ვაქცინაციის შემდეგ.[1054][1055]
ეპიდემიოლოგია: ბავშვებში მულტისისტემური ანთებითი სინდრომის რისკი დადასტურებული ინფექციიდან 2 თვის ფარგლებში შეადგენდა 0.05%-ს, ერთ-ერთ დანიურ კოჰორტულ კვლევაში.[1056] რისკი შემცირდა პანდემიის მეორე წელს და ასევე შემცირდა SARS-CoV-2 ვარიანტის ევოლუციის პარალელურად.[1057] პედიატრიული მულტისისტემური ანთებითი სინდრომი ფიქსირდებოდა 2023 წელსაც, მაგრამ დაბალი ტემპით პანდემიის ადრეულ პერიოდთან შედარებით.[1058]სისტემურმა მიმოხილვამ აჩვენა, რომ პაციენტების საშუალო ასაკი იყო 7.8 წელი, ხოლო პაციენტების 60% იყო მამრობითი სქესის. სიმსუქნე იყო ხშირი თანმხლები მდგომარეობა, რასაც მოსდევდა რესპირატორული დაავადებები, დღენაკლობა და ასთმა.[1059] მულტისისტემური ანთებითი სინდრომის განვითარების რისკის ფაქტორები მოიცავს მამრობით სქესს, ასაკს 5-დან 11 წლამდე, უცხოეთში დაბადებულ მშობლებს, ასთმას, სიმსუქნეს და სიცოცხლის შემზღუდველ მდგომარეობებს.[1060] უფრო მძიმე შედეგებთან ასოცირებული ფაქტორები: ასაკი> 5 წელი; არა-ესპანური, შავკანიანი ეთნიკური წარმომადგენლობა; დისპნოე ან მუცლის ტკივილის სიმპტომები; მომატებული C რეაქტიული ცილა, ტროპონინი, ფერიტინი, D- დიმერი, თავის ტვინის ნატრიურეტული პეპტიდი ან ინტერლეიკინი -6; და ლიმფოციტების ან თრომბოციტების შემცირებული რაოდენობა.[1061] შემთხვევები იშვიათად დაფიქსირდა ახალშობილებში (დროებით ასოცირებული ანტენატალურ ექსპოზიციასთან) და შეიძლება არსებობეს ახალშობილებში სიკვდილობის უფრო მაღალი რისკი უფროს ბავშვებთან შედარებით.[1062] როგორც ჩანს, სინდრომის რისკი უფრო დაბალია ომიკრონის ვარიანტის ფონზე.[1063]
დიაგნოზი: პაციენტებს ხშირად აღენიშნებათ გამოხატული გულის დისფუნქცია და კუჭ-ნაწლავის სიმპტომები. ყველაზე გავრცელებული გამოვლინებები იყო ცხელება (99%), კუჭ-ნაწლავის სიმპტომები (77%), და დერმატოლოგიური სიმპტომები (63%).[1059] მარცხენა პარკუჭის მნიშვნელოვანი დისფუნქციის საერთო პრევალენტობა იყო 38%, კორონარული ანევრიზმის ან დილატაციის 20%, ხოლო ეკგ დარღვევები/გულის არითმიის პრევალენტობა შეადგენდა 28%-ს.[1064] ახალშობილებს ჩვეულებრივ აღენიშნებათ კარდიორესპირატორული ფუნქციის დარღვევა.[1062] ბავშვების დაახლოებით 20%-ს უვითარდება თირკმლის მწვავე დაზიანება.[1065] გამოყოფილია კლინიკური გამოვლინებების სამი ტიპი: მუდმივი ცხელება და კუჭ-ნაწლავის ტრაქტის სიმპტომები (ყველაზე გავრცელებული ტიპი); შოკი გულის დისფუნქციით; და სიმპტომები, რომლებიც აკმაყოფილებენ (ემთხვევა) კავასაკის დაავადების კრიტერიუმებს.[1066] პედიატრიული მულტისისტემური ანთებითი სინდრომის მქონე პაციენტებს უფრო ხშირად აღენიშნებოდათ რესპირატორული და კუჭ-ნაწლავის სიმპტომები და შოკი კავასაკის დაავადების მქონე პაციენტებთან შედარებით; თუმცა, მათ ჰქონდათ კონიუნქტივიტის უფრო დაბალი სიხშირე.[1067] დაავადება შეიძლება ნაკლებად მძიმე იყოს ომიკრონ ვარიანტით ინფექციის შემდეგ, ალფა და დელტა ვარიანტებთან შედარებით.[1068]
გამოკვლევები: ანთებითი, კოაგულაციის და გულის მარკერები მომატებული იყო პაციენტების უმრავლესობაში.[1059] შრატში ტროპონინის დონის მომატება დაფიქსირდა პაციენტების 33%-ში, ხოლო პრო B ტიპის ნატრიურეზული პეპტიდის (proBNP)/BNP დონის მომატება დაფიქსირდა პაციენტების 44%-ში.[1064]
მართვა: მართვა ძირითადად დამხმარე ხასიათისაა და გულისხმობს მულტიდისციპლინური გუნდის ჩართულობას. პაციენტების დაახლოებით 53% საჭიროებდა ინტენსიურ მკურნალობას.[1059] იმუნომამოდულირებელი თერაპიის ოპტიმალური არჩევანი და კომბინაცია საბოლოოდ არ არის დადგენილი. ჯანმრთელობის მსოფლიო ორგანიზაცია რეკომენდაციას უწევს კორტიკოსტეროიდების გამოყენებას დამხმარე მოვლასთან ერთად (ვიდრე ინტრავენური იმუნოგლობულინი პლუს დამხმარე მოვლა, ან მხოლოდ დამხმარე მოვლა) ჰოსპიტალიზირებულ ბავშვებში 0-დან 18 წლამდე, რომლებიც აკმაყოფილებენ მულტისისტემური ანთებითი სინდრომის შემთხვევის განსაზღვრებას. ის ასევე რეკომენდაციას უწევს კორტიკოსტეროიდების მოხმარებას დამხმარე მოვლასთან ერთად გარდა მათთვის, ვინც აკმაყოფილებს ბავშვთა მულტისისტემური ანთებითი სინდრომის შემთხვევის განსაზღვრებას და კავასაკის დაავადების სადიაგნოსტიკო კრიტერიუმებს.[85] ამერიკის შეერთებულ შტატებში, ამერიკის ინფექციური დაავადებათა საზოგადოება რეკომენდაციას უწევს საწყის თერაპიას ინტრავენური იმუნოგლობულინით და/ან კორტიკოსტეროიდით. ანაკინრა, ტოცილიზუმაბი ან ინფლიქსიმაბი შეიძლება გამოყენებულ იქნას რეფრაქტერულ შემთხვევებში.[465] გაიდლაინები გამოქვეყნებულია რევმატოლოგიის ამერიკული კოლეჯის მიერ.[1069] დამატებითი ინფორმაციისთვის გაეცანით თქვენს ადგილობრივ გაიდლაინებს.
პროგნოზი: პაციენტთა მცირე ჯგუფში 1 წლიანი შემდგომი დაკვირვების თანახმად, უმრავლესობას ჰქონდა კარგი შედეგები, საშუალო და გრძელვადიანი სერიოზული შედეგების გარეშე.[1070] პაციენტებზე ავადმყოფობის შემდგომი 6-თვიანი მეთვალყურეობის შედეგად აღმოჩნდა, რომ გულის, კუჭ-ნაწლავის ტრაქტის, თირკმელების, ჰემატოლოგიური და ოტორინოლარინგოლოგიური კლინიკური შედეგები დიდწილად ალაგებული იყო 6 თვის თავზე. ხშირი აღმოჩნდა კუნთური დაღლილობა და ემოციური სისუსტე.[1071] სიკვდილობის სიხშირე იყო 3.9%.[1059]
მომავალი COVID-19 ვაქცინაცია: შეზღუდულია მონაცემები COVID-19 ვაქცინების უსაფრთხოების შესახებ იმ ადამიანებში, რომლებსაც ჰქონდათ მულტისისტემური ანთებითი სინდრომი ბავშვებში ან მოზრდილებში და რომლებსაც ჯერ არ მიუღიათ ვაქცინა. მულტისისტემური ანთებითი სინდრომის ანამნეზი ბავშვებში ან მულტისისტემური ანთებითი სინდრომის ანამნეზი მოზრდილებში შეიძლება იყოს ვაქცინაციის დროს სიფრთხილის ფაქტორი. დამატებითი ინფორმაციისთვის გაეცანით თქვენს ადგილობრივ გაიდლაინებს.
ასევე ცნობილია, როგორც თრომბოზი თრომბოციტოპენიური სინდრომით (TTS) და ვაქცინით გამოწვეული პროთრომბული იმუნური თრომბოციტოპენია (VIPIT). ამ სინდრომის შესახებ მტკიცებულებები შეზღუდულია. ადენოვირუსის ვექტორის ვაქცინები, სინდრომის გამომწვევი მიზეზი, აღარ არის ხელმისაწვდომი უმეტეს ქვეყნებში.
განმარტება: თრომბოზის პროთრომბოზული დაავადება თანმხლები თრომბოციტოპენიით და ანტიაგრეგანტი ფაქტორი 4 (ანტი-PF4) ანტისხეულების განვითარება, რომელიც მიმდინარეობს ადენოვირუსის ვექტორზე დაფუძნებული COVID-19-ის ვაქცინით იმუნიზაციის შემდეგ. თრომბოზი უჩვეულო ადგილებში (მაგალითად, ცერებრალური ვენური სინუსის თრომბოზი, თრომბოზი, არტერიული თრომბოზი) გვხვდება და შეიძლება იყოს მრავალფოკალური. სინდრომი კლინიკურად წააგავს ჰეპარინით გამოწვეულ თრომბოციტოპენიას. ზუსტი პათოფიზიოლოგია უცნობია, მაგრამ არსებობს რამდენიმე ჰიპოთეზა. შეიძლება იყოს სწრაფად პროგრესირებადი და ფატალური.[1072][1073] შემთხვევები ასევე დაფიქსირდა მესენჯერული რნმ ვაქცინების გამოყენებისას, თუმცა უფრო იშვიათად.[1074][1075][1076]
ეპიდემიოლოგია: დიდი ბრიტანეთის ობსერვაციული მონაცემები მიუთითებს იმაზე, რომ თრომბოზული მოვლენის რისკი ყველაზე მაღალი იყო 40 წელზე ნაკლები ასაკის ადამიანებში, 16.1 და 36.3 მილიონ დოზებზე, ცერებრალური ვენური თრომბოზის ან თრომბოზის სხვა მოვლენის შემთხვევაში (რიგითობა დაცულია), ყველაზე მაღალი რისკით ვაქცინაციიდან 4-13 დღის ფარგლებში.[1077] აშშ-ში, Janssen ვაქცინით ინდუცირებული თრომბოზული თრომბოციტოპენიის ჯამური რისკი შეადგენს 3.83 შემთხვევას ვაქცინის მიმღებ ყოველ მილიონ პირზე, საიდანაც ყველაზე ხშირად აღნიშნული მოვლენები 30-49 წლის ქალებში (8.8 შემთხვევა მილიონ დოზაზე) და 40-49 წლის ქალებში (9.02 შემთხვევა მილიონ დოზაზე) ფიქსირდებოდა, შემთხვევის ლეტალობის მაჩვენებლით 15%.[1078] შემთხვევები დაფიქსირდა ვაქცინაციიდან 48 დღემდე.[1079]
დიაგნოზი: ურჩიეთ ადენოვირუსის ვექტორის ვაქცინით აცრილ პირებს, რომლებსაც აღენიშნებათ რაიმე მძიმე სიმპტომი ვაქცინაციიდან 4 -დან 30 დღემდე, მიმართონ სასწრაფო სამედიცინო დახმარებას.[1080][1081] პაციენტთა დაახლოებით ნახევარს აღენიშნება თავის ტვინის ვენური სინუსის თრომბოზი.[1082] თავის ტკივილი ყველაზე ხშირი წარმდგენი სიმპტომია და შესაძლოა წინ უსწრებდეს ვაქცინით ინდუცირებულ თრომბოზულ თრომბოციტოპენიას რამდენიმე დღით ადრე.[1083][1084] ნიშნები და სიმპტომებია: ახლადგამოვლენილი თავის ტკივილი, რომელიც მძიმდება და არ რეაგირებს ჩვეულებრივ ტკივილგამაყუჩებლებზე; უჩვეულო თავის ტკივილი, რომელსაც თან ახლავს დაბინდული მხედველობა, გულისრევა და ღებინება, მეტყველების გართულება, სისუსტე, ძილიანობა ან გულყრები; ახალი, აუხსნელი ჩალურჯება ან სისხლდენა და სუნთქვის უკმარისობა, ტკივილი გულმკერდის არეში, ფეხის შეშუპება ან პერსისტენტული ტკივილი მუცლის არეში. დასვით შეკითხვა ვაქცინაციის ანამნეზის შესახებ VITT-ზე ეჭვის დროს. მწვავედ შეუძლოდ მყოფი პირები მიმართეთ გადაუდებელი სამედიცინო დახმარების განყოფილებაში დაუყოვნებლივ.[1081] პაციენტებს შეიძლება იშვიათად აღენიშნებოდეთ იშემიური ინსულტი.[1085][1086] შეატყობინეთ ყველა შემთხვევის შესახებ ადგილობრივ ორგანოებს, ვაქცინების გვერდითი მოვლენების შეტყობინების სისტემის საშუალებით.
გამოკვლევები: როგორც წესი, რეკომენდებულია სისხლის საერთო ანალიზი (თრომბოციტებთან ერთად), კოაგულოგრამა (მათ შორის ფიბრინოგენი და D-დიმერი), სისხლის ნაცხი/პერიფერიული სისხლის ნაცხი და თრომბოციტის ფაქტორი 4-ის ფერმენტთან შეკავშირებული იმუნოსორბენტული ანალიზი ნებისმიერ პაციენტში, რომელსაც COVID-19-ის ვაქცინაციის შემდეგ 42 დღის ფარგლებში აღენიშნება მწვავე თრომბოზი ან ახლად გამოვლენილი თრომბოციტოპენია. ტიპური ლაბორატორიული მახასიათებლებია თრომბოციტოპენია, D-დიმერის დონის მატება ვენური თრომბოემბოლიისთვის მოსალოდნელ დონეზე მეტად და დაბალი ან ნორმალური ფიბრინოგენის დონე. ფიქსირდება ასევე ანტისხეუელბი თრომბოციტების ფაქტორი 4-ის მიმართ. იმავე დღეს შეუკვეთეთ რადიოლოგიური კვლევები, ნიშნების და სიმპტომების ლოკაციის მიხედვით თრომბოზის დასადასტურებლად. განმეორებითი რადიოლოგიური კვლევა შეიძლება საჭირო იყოს პაციენტებში, რომელთა სისხლის ანალიზიც მიუთითებს სავარაუდო VITT-ზე, მაგრამ თრომბოზი არ ვლინდება რადიოლოგიურად ან კლინიკურად/ლაბორატორიულად ეჭვია პროგრესირებაზე.[1081][1087][1088][1089][1090]
დიფდიაგნოსტიკა: თრომბოციტოპენიის სხვა შესაძლო მიზეზებია: ონკოლოგიური დაავადება, ანტიფოსფოლიპიდური სინდრომი, ჰეპარინით ინდუცირებული თრომბოციტოპენია, თრომბოზული თრომბოციტოპენიური პურპურა, პაროქსიზმული ღამის ჰემოგლობინურია. გაითვალისწინეთ ალტერნატიული დიაგნოზები იმ შემთხვევებში, როცა სისხლის ანალიზით სავარაუდოა VITT. VITT-ის მქონე პირების მცირე ნაწილს არ აქვს თრომბოციტოპენია თავდაპირველად. შესაბამისად, გაუმეორეთ სისხლის ანალიზი 2-3 დღეში ან სიმპტომების დამძიმებისას თუ კლინიკური ეჭვი რჩება. განიხილეთ შემდგომი კვლევები ჰემატოლოგთან.[1081]
მართვა: საჭიროა სწრაფი მკურნალობა. გაიარეთ კონსულტაცია ჰემატოლოგთან მკურნალობის დაწყების ან დამატების გადაწყვეტამდე. შეზღუდულია ინფორმაცია ამ მდგომარეობის ოპტიმალური მკურნალობის შესახებ; თუმცა, მართვა მსგავსია ჰეპარინით ინდუცირებული თრმობოციტოპენიის მართვისა. პირველი რიგის მკურნალობა არის ინტრავენური იმუნოგლობულინის სასწრაფი გამოყენება. მეორე დოზა შეიძლება განიხილებოდეს თუ 2-3 დღის შემდეგ რეაგირება ადეკვატურია. ზოგიერთი ექსპერტი რეკომენდაციას უწევს კორტიკოსტეროიდების გამოყენებას, განსაკუთრებით თუ არასაკმარისია ინტრავენური იმუნოგლობულინი. ანტიკოაგულაცია უმჯობესია არა-ჰეპარინზე დაფუძნებული თერაპიით, როგორიცაა პირდაპირი პერორალური ანტიკოაგულაცია, ფონდაპარინუქსი, დანაპაროიდი ან არგატრობანი, კლინიკური სურათის მიხედვით. ანტიკოაგულაცია უნდა დაიწყოს დაუყოვნებლივ, როცა სარგებელი აჭარბებს სისხლდენის რისკს. დააკვირდით პასუხს ანტიკოაგულაციაზე თუ პაციენტის კლინიკური მდგომარეობა შეიცვლება და მოარგეთ მკურნალობა საჭიროებისამებრ. თავი აარიდეთ თრომბოციტების გადასხმას (გარდა გადაუდებელი მდგომარეობისა), ჰეპარინს (ჰეპარინის ჩარეცხვის ხსნარის ჩათვლით), დაბალმოლეკულურ ჰეპარინს და K ვიტამინის ანტაგონისტებს (მაგ. ვარფარინი). ჰეპარინი შეიძლება გამოიყენოთ, თუ ჰეპარინზე დაფუძნებული ანტიკოაგულანტები არ არის ხელმისაწვდომი განიხილეთ პლაზმის გადასხმა, ფიბრინოგენის ჩანაცვლება ან რიტუქსიმაბი შერჩეულ პაციენტებში. ზოგიერთ პაციენტს შეიძლება დაჭირდეს ქირურგიული ჩარევა თრომბოზის პრევენციისთვის.[1081][1087][1088][1089][1090][1091]
მონიტორინგი: გაწერის შემდეგ პაციენტი ჰემატოლოგის მეთვალყურეობის ქვეშ უნდა იყოს. შეაფასეთ სიმპტომები და გაზომეთ D-დიმერი, ფიბრინოგენი და თრომბოციტების რაოდენობა ყოველ 2-3 დღეში, პირველი 2 კვირის განმავლობაში. გაიმეორეთ ფერმენტული იმუნოსორბენტული ანალიზი (ELISA) თრომბოციტების ფაქტორ 4-ის ანტისხეულებზე, პირველი 4 კვირის განმავლობაში. გაიმეორეთ ტესტები ყოველთვიურად პირველი 6 თვის განმავლობაში და თუ რეციდივი არ დაფიქსირდა ყოველ 3 თვეში. როცა თრომბოციტების ფაქტორ 4-ის ანტისხეულები აღარ გამოვლინდება, შეაფასეთ რამდენად საჭიროა შემდგომი მკურნალობა და მონიტორინგი.[1081]
პროგნოზი: გართულებების შედეგად სიკვდილობა 39%-ს აღწევს.[1083] სიკვდილობის რისკს მნიშვნელოვნად ზრდის ფიბრინოგენის დონე, ასაკი, თრომბოციტების რაოდენობა და ინტრაცერებრული ჰემორაგია ან ცერებრული ვენური თრომბოზი.[1092] მიმართეთ ადგილობრივ გაიდლაინებს VITT-ის ეპიზოდის შემდეგ ვაქცინაციის შესახებ.
მართვის რეკომენდაციები იცვლება და გაიდლაინებს შორის არსებობს განსხვავებები. მიმართეთ ადგილობრივ და უახლეს გაიდლაინებს ამ მდგომარეობის დიაგნოზისა და მართვის შესახებ დეტალური ინფორმაციისთვის.
Examples of learned societies with treatment recommendations Opens in new window
თრომბოემბოლიური მოვლენები, რომლებიც განსხვავდება ვაქცინით ინდუცირებული იმუნური თრომბოზული თრომბოციტოპენიისგან, შეიძლება განვითარდეს COVID-19-ის ნებისმიერი ვაქცინით ვაქცინაციის შემდეგ, მაგრამ ყველაზე ხშირად ვლინდება ადენოვირუსის ვექტორული ვაქცინებით ვაქცინაციის შემდეგ. ვენური თრომბოზი უფრო ხშირად ფიქსირდებოდა, ვიდრე არტერიული თრომბოზი. ცერებრული ვენების თრომბოზი იყო ყველაზე ხშირი გამოვლინება ვენური თრომბოზით დაავადებულ პაციენტებში, რასაც მოჰყვებოდა ღრმა ვენების თრომბოზი. მიოკარდიუმის ინფარქტი ხშირი იყო არტერიული თრომბოზის მქონე პაციენტებში, რასაც სიხშირით მოჰყვებოდა იშემიური ინსულტი.[1093] ადენოვირუსის ვექტორული ვაქცინები შეიძლება ასოცირებული იყოს ფილტვის ემბოლიის და მიოკარდიუმის ინფარქტის მომატებულ ინციდენტობასთან, აცრიდან მეორე კვირაში.[1094]
COVID-19-თან ასოცირებული ასპერგილოზი (CAPA) შეიძლება განვითარდეს კრიტიკულად დაავადებულ ადამიანებში. ეს არის შესწავლილი მიზეზი იმისა, რომ მკურნალობის მიუხედავად პაციენტის კლინიკური მდგომარეობა არ უმჯობესდება.[397]
ეპიდემიოლოგია: ერთ-ერთი კვლევის თანახმად დაფიქსირდა ინტენსიური თერაპიის განყოფილებაში მოთავსებული პაციენტების 10.2%-ში.[1095] რისკფაქტორები მოიცავს ხანდაზმულ ასაკს, ფილტვების ქრონიკულ დაავადებას (მათ შორის უკვე არსებული ფქოდ), ღვიძლის ქრონიკულ დაავადებას, ჰემატოლოგიურ ავთვისებიან სიმსივნეებს, ცერებროვასკულარულ დაავადებას, თირკმელების ჩანაცვლებით თერაპიას, მექანიკურ ვენტილაციას, იმუნოსუპრესიას, ინტერლეიკინ-6 ინჰიბიტორების მიღებას და მაღალი დოზებით კორტიკოსტეროიდების გამოყენებას.[397][1096][1097][1098]
დიაგნოზი: ასპერგილოზი გაითვალისწინეთ პაციენტებში, რომელთა მდგომარეობაც მძიმდება ოპტიმალური დამხმარე თერაპიის მიუხედავად, ან რადიოლოგიურად/კლინიკურად აღინიშნება საეჭვო ნიშნები.[397][1096] არ არსებობს კონკრეტული ნიშნები ან სიმპტომები. დააფუძნეთ თქვენი გადაწყვეტილებები ინდივიდუალურ რისკფაქტორებს და პაციენტის კლინიკურ მდგომარეობას და ჩართეთ მულტიდისციპლინური გუნდი (ინფექციონისტის ჩათვლით).[397] ხშირად ვლინდება, როგორც COVID-19 პნევმონია, ფილტვის ასპერგილოზის კომპიუტერული ტომოგრაფიის სკანირებით გამოვლენილი ჩვეული ანომალიების გარეშე.[1099] მიმართეთ თქვენს ადგილობრივ პროტოკოლებს COVID-19-თან ასოცირებული ასპერგილოზის დიაგნოზის შესახებ.
გამოკვლევები: გამოიყენეთ მთელი რიგი ტესტები სარწმუნო დიაგნოზის ალბათობის გასაზრდელად; იგულისხმება ბრონქოალვეოლური ლავაჟიც, თუ ეს შესაძლებელია. ტესტი სოკოს საწინააღმდეგო რეზისტენტობაზე, თუ ასპერგილუსის იზოლატი კულტივირებულია. არ დანიშნოთ ტესტები, თუ კლინიკური ეჭვი დაბალია.[397]
მართვა: რეკომენდებულია სოკოს საწინააღმდეგო თერაპია. გამოიყენეთ სოკოს საწინააღმდეგო თერაპია მხოლოდ იმ შემთხვევაში, თუ გამოკვლევები მხარს უჭერს COVID-19-თან ასოცირებული ასპერგილოზის დიაგნოზს, ან გვაქვს მასზე ეჭვი, მაგრამ გამოკვლევების შედეგები ჯერ არ არის ხელმისაწვდომი. არ არის საკმარისი მტკიცებულება კონკრეტული სოკოს საწინააღმდეგო საშუალებების რეკომენდაციისთვის. განიხილეთ მკურნალობის ვარიანტები მულტიდისციპლინურ გუნდთან (მათ შორის ინფექციონისტთან). შეწყვიტეთ მკურნალობა, თუ გამოკვლევის შედეგები არ დაადასტურებს დიაგნოზს.[397] მიმართეთ თქვენს ადგილობრივ პროტოკოლებს COVID-19-თან ასოცირებული ასპერგილოზის მართვის შესახებ.
პროგნოზი: აღწერილია სიკვდილობის მაჩვენებელი 55%.[1095][1097]
მუკორმიკოზი (ასევე ცნობილი, როგორც "შავი სოკო") იშვიათად აღინიშნა, განსაკუთრებით დაბალი და საშუალო შემოსავლის მქონე ქვეყნებში, ძირითადად ინდოეთში.[1100] COVID-19-თან ასოცირებული ფილტვის მუკორმიკოზი დიაგნოზირებულია ვირუსოლოგიურად დადასტურებულ COVID-19-თან ერთად ან 3 თვის განმავლობაში. გამოქვეყნებულია დადასტურებული, სავარაუდო ან შესაძლო ფილტვის დაავადების შემთხვევების განსაზღვრებები. შესაძლებელია ასპერგილოზთან კოინფექცია.[1101]
ეპიდემიოლოგია: შემთხვევების დაახლოებით 88% დაფიქსირდა დაბალი ან საშუალო შემოსავლის ქვეყნებში.[1102] ინდოეთში შემთხვევებმა მნიშვნელოვნად იმატა მისი მეორე ტალღის დროს 2021 წლის დასაწყისში.[1103] შემთხვევები დაფიქსირდა სხვა ქვეყნებში, მათ შორის აშშ-ში.[1104] რისკფაქტორებია მამრობითი სქესი, უკონტროლო დიაბეტი და იმუნოსუპრესია (მაგ. კორტიკოსტეროიდებით თერაპიის გამო).[1105][1106]
დიაგნოზი: დაადგინეთ დაბალი ზღურბლი დიაგნოზზე ეჭვის მისატანად. მნიშვნელოვანია არ გამოგრჩეთ გამაფრთხილებელი ნიშნები და სიმპტომები (მაგ. ცხვირის დახშობა; მოშავო-სისხლიანი გამონადენი ცხვირიდან; სახის ან სინუსების ტკივილი; კბილის ტკივილი ან მორყევა; მხედველობის პრობლემები; ჰემოფთიზი, ნეკროზული ფუფხი კანზე, სასაზე ან ცხვირის ღრუში). ნუ დააყოვნებთ, შესაბამისი კვლევები შეუკვეთეთ.[1107] COVID-19-ის დიაგნოზსა და მუკორმიკოზის მტკიცებულებას შორის საშუალო დრო შეადგენდა 15 დღეს. რინო-ორბიტალური მუკორმიკოზი აღმოჩნდა ყველაზე ხშირი (42%), შემდეგ რინო-ორბიტო-ცერებრული მუკორმიკოზი (24%) და ფილტვის მუკორმიკოზი (10%).[1105] დაფიქსირდა მუკორმიკოზის შემთხვევები ატიპურ ადგილებში, ისევე როგორც შემთხვევები COVID-19 გამოჯანმრთელებულ პაციენტებში.[1108][1109] ნუ შეიკავებთ თავს გამოკვლევების აგრესიული დანიშვნისგან საჭიროებისამებრ, სოკოვანი ეტიოლოგიის გამოსავლენად.[1107] ფილტვის მუკორმიკოზის ადრეული დიაგნოსტიკისთვის რეკომენდებულია დრეკადი ბრონქოსკოპია და გულმკერდის ვიზუალიზაცია.[1101]
მართვა: მართვის სტრატეგიებია: ჰიპერგლიკემიის, დიაბეტის ან დიაბეტური კეტოაციდოზის კონტროლი; კორტიკოსტეროიდის დოზის შემცირება მოხსნის მიზნით; იმუნომამოდულირებელი სამკურნალო საშუალებების შეწყვეტა; ექსტენსიური ქირურგიული წმენდა ნეკროზული მასალების მოსაშორებლად; სოკოს საწინააღმდეგო თერაპია (მაგ. ამფოტერიცინ-B საწყისი თერაპიისთვის, შემდეგ პოზაკონაზოლი ან იზავუკონაზოლი შემანარჩუნებელი ან სათადარიგო თერაპიის სახით) 4-6 კვირის განმავლობაში; და შესაბამისი მხარდამჭერი მოვლა და მონიტორინგი. პაციენტები უნდა იმყოფებოდნენ მულტიდისციპლინური გუნდის მეთვალყურეობის ქვეშ, რომელშიც შედის ინფექციური დაავადების სპეციალისტი; ინტენსივისტი; ნევროლოგი; სტომატოლოგი; ოფთალმოლოგი; ყელ-ყურ-ცხვირის სპეციალისტი; და ქირურგი.[1101][1107]
პრევენცია: პრევენცია მოიცავს ჰიპერგლიკემიის კონტროლს; სისხლში გლუკოზის დონის მონიტორინგს COVID-19-ის მქონე პაციენტებში გაწერის შემდეგ (დიაბეტის სტატუსის განურჩევლად); კორტიკოსტეროიდების, ანტიბიოტიკების და სოკოს საწინააღმდეგო მედიკამენტების ფრთხილ გამოყენებას.[1107]
გართულებები: ფილტვის არტერიის ფსევდოანევრიზმის იშვიათი შემთხვევები დაფიქსირდა COVID-19-თან ასოცირებული ფილტვის მუკორმიკოზის დროს.[1110]
პროგნოზი: საერთო სიკვდილობის მაჩვენებელი იყო 39%.[1102] ჯამური სიკვდილობა ინდოეთში (36.5%) ნაკლები იყო გლობალურად აღწერილ მაჩვენებელზე (61.9%), რაც სავარაუდოდ აიხსნება ინოეთში რინოორბიტალური მუკორმიკოზის გავრცელებით.[1103] მომატებული სიკვდილობის რისკ-ფაქტორები მოიცავს ხანდაზმულ ასაკს, სპეციფიკურ თანმხლებ დაავადებებს, ასპერგილუსის ერთობლივ ინფექციას და ტოცილიზუმაბის გამოყენებას.[1102] გადარჩენილთა მნიშვნელოვან ნაწილს აღენიშნებოდა ძალიან მძიმე ნარჩენი მდგომარეობა (მაგ., მხედველობის დაკარგვა).[1100] ფილტვების და რინო-ორბიტო-ცერებრალური მუკორმიკოზის მქონე პაციენტები და ისინი, ვინც მხოლოდ სამედიცინო მკურნალობას იღებენ, არიან სიკვდილობის მომატებულიი რისკის ქვეშ.[1111]
კანდიდემიის საერთო ინციდენტობა მერყეობს 0.7%-დან 23.5%-მდე და უმეტეს შემთხვევაში ვითარდება ინტენსიური თერაპიის განყოფილებაში მექანიკური ვენტილაციის მქონე პაციენტებში.[1112] დაფიქსირდა კანდიდემიის შემთხვევები Candida auris-ით, რომელიც არის მულტირეზისტენტული პათოგენი.[1113] ამ პოპულაციაში გაზრდილი შემთხვევების მიზეზები ცუდად არის შესწავლილი; თუმცა, პაციენტები ექსპოზირდებიან კანდიდემიის მრავალ რისკფაქტორთან, მათ შორისაა კორტიკოსტეროიდული თერაპია, იმუნოსუპრესიული თერაპია, ანტიბიოტიკები და ინტენსიური თერაპიის განყოფილებაში ხანგრძლივი ყოფნა. დაფიქსირდა სიკვდილობის მაღალი მაჩვენებელი.[1114]
პანკრეასის მსუბუქი დაზიანება (განისაზღვრება, როგორც შრატში ამილაზას ან ლიპაზას მატება) დაფიქსირდა პაციენტების 17%-ში, შემთხვევათა ერთ სერიაში.[1115] უცნობია, ეს არის ვირუსის პირდაპირი ეფექტი თუ დამაზიანებელი იმუნური რეაქციის, რომელიც ზოგიერთ პაციენტში ვითარდება. პაციენტებს გამოუვლინდათ მძიმე პანკრეატიტის და მანეკროზებელო პანკრეატიტის მომატებული რისკი, ასევე გაიზარდა კლინიკაში ყოფნის ხანგრძლივობა.[1116] მწვავე პანკრეატიტის მქონე პაციენტებს ჰქონდათ მაღალი ჯამური სიკვდილობა (18.5%) და მნიშვნელოვნად უარესი კლინიკური შედეგები.[1117] ყველაზე ხშირი პირველი სიმპტომი იყო მუცლის ტკივილი.[1118] ანამნეზში პანკრეატიტის ქონა არ წარმოადგენს პანკრეასის ანთების რისკფაქტორს COVID-19-ის დროს.[1119] მიზეზობრივი კავშირი SARS-CoV-2 ინფექციასა და მწვავე პანკრეატიტს შორის არ არის დადგენილი.[1120]
იმუნური თრომბოციტოპენია იშვიათადაა აღწერილი. შემთხვევების უმეტესობა ფიქსირდება >50 წლის პაციენტებში; ბავშვებში შემთხვევების მხოლოდ 7%-ია აღწერილი. შემთხვევების უმეტესობა გამოვლინდა მძიმე-საშუალო COVID-19-ის მქონე პაციენტებში; თუმცა, შემთხვევების 7% აღწერილია უსიმპტომო პაციენტებში. შემთხვევების 20%-ში იწყება COVID-19-ის სიმპტომების გამოვლენიდან 3 კვირაში, უმეტესად კლინიკური გამოჯანმრთელების შემდეგ. მძიმე, სიცოცხლისთვის საშიში სისხლდენა იშვიათია. მკურნალობა გულისხმობს კორტიკოსტეროიდების გამოყენებას, ინტრავენურ იმუნოგლობულინს, თრომბოპოეტინ-რეცეპტორის აგონისტებს.[1121]
ქვემწვავე თიროიდიტი ფარისებრი ჯირკვლის დაავადებაა, რომელიც ვირუსული ან პოსტვირუსული მიზეზით არის განპირობებული. ახალი მტკიცებულებების თანახმად, SARS-CoV-2-ით ინფექციამ შეიძლება გამოიწვიოს ქვემწვავე თირეოიდიტი, შემთხვევის შეტყობინებებსა და აღწერებზე დაყრდნობით.[1122][1123] 21 შემთხვევის მიმოხილვის თანახმად, ეს უფრო ხშირია ქალებში. COVID-19 ავადობას და ქვემწვავე თიროიდიტის სიმპტომების გამოვლენას შორის საშუალოდ 25 დღე იყო. ინფექცია პაციენტების უმრავლესობაში ლაგდება ქვემწვავე თიროიდიტის სიმპტომების გამოვლენამდე. ცხელება და კისრის ტკივილი ყველაზე ხშირი პირველი ჩივილები იყო. სიმპტომები მკურნალობით ალაგდა ყველა პაციენტში; თუმცა, 5 პაციენტი აღნიშნავდა ჰიპოთიროიდულ დაავადებას შემდგომი მეთვალყურეობის დროს.[1124]
COVID-19-მა შეიძლება ასევე გამოიწვიოს ფარისებრი ჯირკვლის აუტოიმუნური დაავადება ან გააძლიეროს ფარისებრი ჯირკვლის ფონური დაავადება რემისიის დროს. დაფიქსირდა გრეივის დაავადების, ჰაშიმოტოს თირეოიდიტის და პოსტნატალური თირეოიდიტის შემთხვევები.[1125]
კრიტიკულ პაციენტებში შეიძლება განვითარდეს გასტროინტესტინური გართულებები; თუმცა, უცნობია, კრიტიკული ავადმყოფობის გამოხატულებაა ეს თუ COVID-19-ის სპეციფიკური ნიშანია. ერთი კვლევის თანახმად, COVID-19-ის მქონე პაციენტებში უფრო მაღალი იყო გასტროინტესტინური გართულებების გამოვლენის რისკი, ვიდრე არმქონე პაციენტებში; კერძოდ, გვხვდება ტრანსამინიტი, მძიმე ილეუსი და მეზენტერული იშემია.[1126] მწვავე მეზენტერული იშემიის მქონე პაციენტებში, წვრილი ნაწლავის იშემია იყო მუცლის ღრუს კომპიუტერულ ტომოგრაფიაზე ყველაზე გავრცელებული მახასიათებელი, რასაც სიხშირით მოჰყვებოდა იშემიური კოლიტი. არაოკლუზიური მეზენტერული იშემია იყო ნაწლავის დაზიანების ყველაზე გავრცელებული დამახასიათებელი სურათი.[1127]
მაკროვასკულური არტერიული/ვენური თრომბოზი გამოვლენილია ნაწლავის იშემიის მქონე პაციენტების 50%-ში. ჯამური სიკვდილობა გასტროინტესტინური იშემიის მქონე COVID-19 პაციენტებში და რადიოლოგიურად გამოხატული მეზენტერული თრომბოზული ოკლუზიის მქონე პაციენტებში იყო, შესაბამისად, 38.7% და 40%.[1128] ნაწლავების იშემიის მქონე პაციენტებს ხშირად უვლინდებათ მუცლის ტკივილი და ღებინება. მართვა გულისხმობს კუჭის დეკომპრესიას, სითხეების მიწოდებას, ჰემოდინამიკურ მხარდაჭერასა და ქირურგიულ ჩარევას.[1129]
პაციენტებს შესაძლოა ჰქონდეთ კუჭ-ნაწლავის ტრაქტიდან სისხლდენის მომატებული რისკი ზოგად მოსახლეობასთან შედარებით; თუმცა, მტკიცებულებები შეზღუდულია. კუჭ-ნაწლავის ტრაქტიდან სისხლდენის მაჩვენებელი შეადგენდა 2%-ს.[1130] გასტროინტესტინური ჰემორაგიის რისკფაქტორები COVID-19-ის დროს მოიცავს კუჭ-ნაწლავის ტრაქტიდან სისხლდენის და ანტიკოაგულანტების გამოყენების ანამნეზს.[1131]
მწვავე ტელოგენური ცვენა, დიფუზური თმის ცვენის ტიპი, დაფიქსირდა პაციენტებში, რომლებიც გამოჯანმრთელდნენ ინფექციისგან. პაციენტების საშუალო ასაკი იყო 44 წელი და პაციენტების უმეტესობა იყო ქალი. საშუალო ხანგრძლივობა COVID-19-ის სიმპტომების დაწყებიდან ტელოგენური ცვენის გამოჩენამდე იყო 74 დღე. პაციენტების უმეტესობა გამოჯანმრთელდა; თუმცა, პაციენტთა მცირე ნაწილს განუვითარდა თმის მუდმივი ცვენა. სტრესი შეიძლება იყოს ხელშემწყობი ფაქტორი.[1132] ასევე დაფიქსირდა ინფექციის შემდეგ ახალდაწყებული ალოპეციის, ასევე რეციდივების ან გამწვავების შემთხვევები.[1133]
არსებობს ახალი მტკიცებულებები, რომ პაციენტებს იშვიათად აქვთ ქვედა საშარდე გზების და მამაკაცის სასქესო სისტემის ჩართულობის ნიშნები, სიმპტომები და რადიოლოგიური და ლაბორატორიული მახასიათებლები. ეს შეიძლება მოიცავდეს დისკომფორტს, შეშუპებას ან ტკივილს (მწვავე ორქიტი, ეპიდიდიმიტი ან ეპიდიდიმო-ორქიტი); დაბალი დინების პრიაპიზმს; დარღვეულ სპერმატოგენეზს (მათ შორის სპერმის რაოდენობის შემცირება, სპერმის კონცენტრაციის კლება, სპერმის მოძრაობის დარღვევა და ნორმალური სპერმის მორფოლოგია); შარდის ბუშტის სისხლდენას; შარდის მწვავე შეკავებას; და ქვედა საშარდე გზების არსებული სიმპტომების გაუარესებას (პროსტატის კეთილთვისებიანი ჰიპერპლაზიის გამწვავების ჩათვლით). როგორც ჩანს, სპერმის პარამეტრები ნორმას უბრუნდება პაციენტების გამოჯანმრთელებისას. საჭიროა შემდგომი კვლევა.[1134][1135][1136][1137][1138]
პაროსმია (სუნის არასწორი აღქმა) გვიანი სიმპტომია, რომელიც შეიძლება განვითარდეს ინფიცირებიდან დაახლოებით 3 თვის შემდეგ. ეს შეიძლება განვითარდეს ყოველგვარი წინა აშკარა სუნის დაკარგვის გარეშე, ან შეიძლება მოჰყვეს აღდგენის ხანმოკლე პერიოდს საწყისი ანოსმიიდან. არ არსებობს ეფექტური, მტკიცებულებებზე დაფუძნებული მკურნალობა; თუმცა, პაციენტს უნდა მიეცეს სასარგებლო რჩევები გამოჯანმრთელებამდე პაროსმიასთან ერთად ცხოვრების შესახებ.[573]
ამ მასალის გამოყენება ექვემდებარება ჩვენს განცხადებას
