ეტიოლოგია
ვირუსოლოგია
მძიმე მწვავე რესპირატორული სინდრომის კორონავირუსი 2 (SARS-CoV-2) აქამდე უცნობი ბეტაკორონავირუსია, რომელიც 2019 წლის დეკემბერში აღმოაჩინეს უცნობი ეტიოლოგიის პნევმონიის მქონე პაციენტების კლასტერებში (ჩინეთის ჰუბეის პროვინციაში, ქალაქ ვუჰანში), ბრონქოალვეოლურ ლავაჟის ნიმუშებში.[27]
კორონავირუსები გარსიანი რნმ ვირუსების დიდი ოჯახია, რომელთაგან ზოგიერთი იწვევს ავადმყოფობას ადამიანში (მაგ., გაციება, მძიმე მწვავე რესპირატორული სინდრომი [SARS], შუა აღმოსავლეთის რესპირატორული სინდრომი [MERS]), ხოლო სხვები ცირკულირებენ ძუძუმწოვრებსა და ფრინველებში. იშვიათად ცხოველის კორონავირუსი გადადის ადამიანებზე, შემდეგ კი ადამიანებს შორის ვრცელდება. ასე მოხდა მძიმე მწვავე და შუა აღმოსავლეთის რესპირატორული სინდრომების გამომწვევი ვირუსების შემთხვევაშიც.
SARS-CoV-2 მიეკუთვნება Sarbecovirus ქვეგვარს, ოჯახს - Coronaviridae, იგი მეშვიდე კორონავირუსია, რომელიც ადამიანებს აინფიცირებს. ვირუსი წააგავს SARS-ის მსგავს კორონავირუსს, რომელიც ღამურებში გვხვდება, თუმცა განსხვავდება SARS-CoV და MERS-CoV ვირუსებისგან.[28][29]
იხ. კლასიფიკაციის სექცია ქვემოთ, SARS-CoV-2-ის ვარიანტების შესახებ დამატებითი ინფორმაციისთვის.
[Figure caption and citation for the preceding image starts]: ილუსტრაცია, რომელზეც ჩანს მძიმე მწვავე რესპირატორული სინდრომის კორონავირუსი-2-ის (SARS-CoV-2) ულტრასტრუქტურული მორფოლოგია ელექტრონული მიკროსკოპიით.დაავადებათა კონტროლისა და პრევენციის ცენტრები (CDC) [Citation ends].
ვირუსის წარმოშობა
პაციენტების თავდაპირველ უმეტესობას დაუდგინდა კავშირი სამხრეთ ჩინეთის ჰუანანის ზღვის პროდუქტების ბაზართან, რომელიც არის ცოცხალი ან "სველი" ბაზარი, რაც მიუთითებს ვირუსის ზოონოზურ წარმოშობაზე.[30][31][32] პირველ 425 დადასტურებულ შემთხვევაში ვირუსის გავრცელების დინამიკის თავდაპირველი შეფასების თანახმად, 2020 წლის 1 იანვრამდე შემთხვევების 55% დაკავშირებული იყო ჰუანანის სამხრეთ ჩინეთის ზღვის პროდუქტების ბაზართან; ამ თარიღის შემდეგ კი შემთხვევების მხოლოდ 8.6% უკავშირდება ბაზარს. ეს მეტყველებს ახლო კონტაქტისას ადამიანიდან ადამიანზე გადაცემაზე 2019 წლის დეკემბრის მეორე ნახევრიდან.[32] უფრო ახალი კვლევების თანახმად, ვირუსი უფრო ადრე წარმოიშვა, ვიდრე აქამდე ეგონათ სხვა ქვეყნებში.[33][34]
ზოონოზური წარმოშობა ჯერ კიდევ არ არის დადასტურებული. ზოგიერთი კვლევის თანახმად, SARS-CoV-2- შეიძლება იყოს ღამურის კორონავირუსის და უცნობი წარმოშობის კორონავირუსის რეკომბინანტი. პანგოლინები და წაულები ნავარაუდებია, როგორც შუამავალი მასპინძლები. თუმცა, ამჟამად არ არსებობს მტკიცებულება, რომელიც ადასტურებს ღამურიდან ადამიანზე ვირუსის ტრანსმისიას შუამავალი ცხოველის მეშვეობით.[35] SARS-CoV-2-ის წარმოშობის დასადგენად საჭიროა დამატებითი კვლევების წარმოება.
გავრცელების დინამიკა
რესპირატორული გზით გადადება გავრცელების მთავარი გზაა, რისკის მთავარი განმსაზღვრელი ფაქტორებია სიახლოვე და ვენტილაცია.[36] არსებული მტკიცებულებების თანახმად, ადამიანებს შორის გადაცემა ძირითადად ხდება მაშინ, როდესაც ინფიცირებული ადამიანი მჭიდრო კონტაქტშია მეორე ადამიანთან. ვირუსი შეიძლება გავრცელდეს ინფიცირებული ადამიანის პირიდან ან ცხვირიდან მცირე თხევადი ნაწილაკებით (უფრო დიდი წვეთებიდან პატარა აეროზოლებამდე ზომით), როდესაც ადამიანი ახველებს, აცემინებს, მღერის, მძიმედ სუნთქავს ან საუბრობს. ახლო მანძილზე კონტაქტმა შეიძლება გამოიწვიოს ვირუსის ინჰალაცია ან ინოკულაცია პირის ღრუს, ცხვირის ან თვალების მეშვეობით.[37]
აეროზოლური ტრანსმისია შესაძლოა მოხდეს სამედიცინო დაწესებულებაში, აეროზოლის წარმომქნელი პროცედურების შესრულების დროს. არსებობს ეპიდაფეთქების ზოგიერთი ანგარიში, რომლის მიხედვით ინფექციის აეროგენული ტრანსმისია საზოგადოებრივ პრიობებშიც შესაძლებელია (გარკვეულ შემთხვევებში); თუმცა, ამ ანგარიშებში საუბარია შენობის შიგნით არსებულ, ხალმხრავალ სივრცეებზე, რომელსაც ცუდი ვენტილაციური სისტემა აქვს და სადაც ინფიცირებული პაციენტი შესაძლოა მძიმედ სუნთქავდეს (მაგ. რესტორნები, გუნდური სიმღერის პრაქტიკის სივრცეები, ფიტნეს დარბაზები).[37][38] ამასთან, აღნიშნული კლასტერების დეტალური გამოკვლევით ირკვევა, რომ ამ ანგარიშებში აღწერილი ტრანსმისიის ფაქტების რეალური მიზეზი შესაძლოა ვირუსის წვეთებით და ფომიტებით გავრცელება იყოს.[37] მიუხედავად იმისა, რომ პაციენტებთან ახლოს ან მოშორებით ჰაერში ვლინდებოდა SARS-CoV-2 რნმ, ნიმუშების მცირე ნაწილში იყო ცოცხალი ვირუსი.[39] გადაცემის რისკი ბევრად დაბალია გარეთ, ვიდრე შენობებში. შეზღუდული რაოდენობის კვლევების თანახმად, გადაცემის სიხშირე <1%-ზე.[40][41]არადამაჯერებელია მტკიცებულებები იმის თაობაზე, რომ საინჰალაციო მკურნალობები იწვევენ SARS-CoV-2-ის მსგავსი კორონავირუსების ტრანსმისიის რისკის ზრდას და არსებობს მინიმალური პირდაპირი მტკიცებულებები SARS-CoV-2-ის ტრანსმისიის რისკთან დაკავშირებით.[42]
ფომიტური გადაცემა (ფომიტებთან პირდაპირი კონტაქტით) შეიძლება მოხდეს, მაგრამ მტკიცებულება გავრცელების ამ გზასთან დაკავშირებით არ არის ცალსახა. იმ შემთხვევებში, როცა იყო ეჭვი ფომიტებით გადაცემაზე, ვერ გამოირიცხა რესპირატორული გადაცემა.[36] კვლევების უმეტესობა აღწერს ვირუსის არსებობას ზედაპირებზე. თუმცა, მტკიცებულება მწირია ცოცხალი ვირუსის არსებობის შესახებ.[43] რეპლიკაციის უნარის მქონე ვირუსი უფრო სავარაუდოა, რომ გამოვლინდეს, როდესაც პოლიმერაზული ჯაჭვური რეაქციის ციკლის ბარიერი ინფიცირებული პირების კლინიკური ნიმუშებისთვის არის <30 (ანუ მაღალი ვირუსული დატვირთვა).[44]
მიუხედავად იმისა, რომ შესაძლებელია ფეკალურ-ორალური გზით გადაცემა (ან რესპირატორული გადაცემა აეროზოლირებული განავლით), მტკიცებულება ძალიან მწირი და სუსტია.[36]
არ არის აღწერილი გადაცემა სხვა ბიოლოგიური სითხეებით (მაგ. სქესობრივი კავშირი ან სისხლისმიერი).[36] მიუხედავად იმისა, რომ ვირუსი აღმოჩენილია ბიოლოგიურ სითხეებში (მაგ. სპერმა, შარდი, თავზურგტვინის სითხე, თვალის სითხეები), ვირუსის ან ვირუსული კომპონენტების არსებობა არ ნიშნავს ინფექციურობას.[45] შეზღუდულია მონაცემები ორგანოების დონორებისგან ინფექციის გადაცემის რისკის შესახებ. თუმცა, როგორც ჩანს, არსებობს გადაცემის დაბალი რისკი ფილტვგარე (ანუ თირკმელების, ღვიძლის, გულის) ორგანოებიდან SARS-CoV-2-დადებითი დონორებისგან, მიუხედავად იმისა, არის თუ არა დონორი სიმპტომური ორგანოს ამოკვეთის დროს.[46]
იშვიათად ხდება პერინატალური (ვერტიკალური) ტრანსმისია ასევე ფიქსირდება ვირუსის ტრანსპლაცენტური გადაცემაც. ვერტიკალური ტრანსმისიის გავრცელების და გადაცემის დროის შესახებ მტკიცებულებების რაოდენობა შეზღუდულია.[47] საჭიროა მაღალი ხარისხის კვლევები იმის დასადგენად, ხდება თუ არა პერინატალური გადაცემა.[48] ვირუსის ფრაგმენტები გამოვლენილია დედის რძეში; თუმცა, ეს იშვიათია და, არსებობის შემთხვევში, უკავშირდება ჩვილებში მსუბუქი სიმპტომების განვითრებას.[49]
ერთ-ერთი სისტემური მიმოხილვის მიხედვით, ნოზოკომიური ტრანსმისია დაფიქსირდა პაციენტთა 44%-ში; თუმცა, ეს მიმოხილვა შემოიფარგლა შემთხვევათა სერიით, რომელიც ჩატარდა ვუჰანში, ეპიდაფეთქების დასაწყისში, ინფექციის პრევენციისა და კონტროლის ზომების მიღებამდე.[50] საავადმყოფოში შეძენილმა ინფექციებმა შეადგინა დიდ ბრიტანეთში 2020 წლის თებერვლიდან აგვისტომდე დაფიქსირებული ინფექციების დაახლოებით 11.3%. პიკი დაფიქსირდა მაისში, 15.8%. 2020 წლის ოქტომბერში, ზოგიერთ რეგიონში დაფიქსირდა 25%-მდე სიხშირე. სიხშირე შესამჩნევად უფრო მაღალი იყო საზოგადოებრივ საცხოვრებელ საავადმყოფოებში (61.9%) და ფსიქიკური ჯანმრთელობის საავადმყოფოებში (67.5%), ვიდრე მწვავე და ზოგადი პროფილის საავადმყოფოებში (9.7%).[51][52] ინდექს შემთხვევებთან ექსპოზირებული სამედიცინო პერსონალის (არ იგულისხმება აეროზოლის წარმომქმნელი პროცედურები) აღმწერი კვლევების მიხედვით არ ფიქსირდება (ან ფიქსირდება მცირე რაოდენობით) ინფექციის ნოზოკომიური ტრანსმისიის შემთხვევა, როდესაც პერსონალი იყენებს კონტაქტურ და წვეთოვან დაცვის ზომებს.[53] რისკი სამედიცინო პერსონალისთვის, რომლებიც ასრულებენ ტრაქეოსტომიას ან პროცედურაში ასისტენტად იღებენ მონაწილეობას, როგორც ჩანს, დაბალია.[54]
BMJ: visualising SARS-CoV-2 transmission routes and mitigations Opens in new window
ტრანსმისიის დინამიკა სიმპტომებთან მიმართებაში
გადაცემა უფრო სავარაუდოა თუ კონტაქტების ექსპოზიცია მოხდა ინფიცირებული პირის (ინდექს პაციენტი) სიმპტომების დაწყებიდან მალევე.
ახლო კონტაქტებზე გადაცემის რისკი უფრო მაღალი იყო თუ ექსპოზიცია მოხდა პაციენტის სიმპტომების დაწყებიდან 2-3 დღის შემდეგ. ინფიცირებულ კონტაქტებს შორის, უსიმპტომო ინფექცია უფრო ხშირი იყო თუ პირი ექსპოზირებული იყო უსიმპტომო ინდექს პაციენტთან, რაც მიუთითებს, რომ ინდექს პაციენტში მიმდინარე დაავადების სიმძიმე შეიძლება კავშირში იყოს დაავადების კლინიკურ მიმდინარეობასთან შემდგომ პაციენტში.[55]
ინფექციურობის საშუალო ხანგრძლივობა მსუბუქი დაავადების მქონე პაციენტებში რეალურ სამყაროში საზოგადოებრივ პირობებში (ომიკრონამდელი ვარიანტი) იყო დაახლოებით 5 დღე (დიაპაზონი 3-დან 7 დღემდე) ერთ კვლევაში. სიმპტომების დაწყების მედიანა იყო 3 დღე ვირუსული რნმ და ინფექციური დატვირთვის პიკის გამოვლენამდე. შემთხვევების 25%-ზე ნაკლებში ვირუსი გამოიყოფა სიმპტომების დაწყებამდე. შემთხვევების ორი მესამედი კვლავ ინფექციური იყო სიმპტომების დაწყებიდან 5 დღის შემდეგ, ხოლო ერთი მესამედი კვლავ ინფექციური იყო 7 დღის შემდეგ.[56]
შემდგომი გადაცემა იცვლება კონკრეტული მასპინძლისა და კონტაქტის ფაქტორების და ექსპოზიციის ხასიათის მიხედვით. გადაცემის მატებასთან დაკავშირებული ფაქტორები:[57]
გარემო ფაქტორები: შენობის შიგნით ყოფნა, ცუდი ვენტილაცია, ხალხმრავლობა, სიახლოვე, საერთო საგნების გამოყენება, ცივი გარემო ტემპერატურა, დაბალი ტენიანობა
მასპინძლის ფაქტორები: ინფიცირება ბოლო პერიოდში, მაღალი ვირუსული დატვირთვა, მძიმე დაავადება, ასაკი, თანმხლები დაავადებების არსებობა, იმუნოდეფიციტი
ქცევითი ფაქტორები: სიმღერა/ყვირილი, ხველა/ცემინება, ჩახუტება/კოცნა, ნიღბის ეტიკეტი, ხელების ჰიგიენა, კონტაქტის ხანგრძლივობა
ვირუსული ფაქტორები: ცვლილებები ვირუსის გენომში, რომელიც დაკავშირებულია გაზრდილ ტრანსმისიულობასთან.
სიმპტომური გავრცელება
გადაცემა ძირითადად ხდება რესპირაციული წვეთებით ან აეროზოლებით ინფიცირებულ სიმპტომურ შემთხვევასთან ახლო კონტაქტის დროს. გადამდებლობა დამოკიდებულია ადამიანის მიერ გამოყოფილი სიცოცხლისუნარიანი ვირუსის რაოდენობაზე, კონტაქტის ტიპზე, გარემოზე და ინფექციის პრევენციისა და კონტროლის ღონისძიებებზე.[37]
პრესიმპტომური გადაცემა
გადაცემა შეიძლება მოხდეს ინკუბაციურ პერიოდში სიმპტომების დაწყებამდე.
მიუხედავად იმისა, რომ არსებობს პრესიმპტომური ადამიანებისგან ინფექციის მტკიცებულება, არსებობს შეზღუდული მტკიცებულება იმის შესახებ, თუ რამდენად ხშირია ეს მოვლენა და გადაცემის სავარაუდო სიხშირე ძალიან ცვალებადია.[58][59]
ერთ-ერთი სისტემური მიმოხილვის თანახმად, პრესიმპტომურ ინდექს შემთხვევებთან ექსპოზირებული ადამიანების მხოლოდ 7% დაინფიცირდა.[60] SARS-CoV-2 ვირუსით კონტროლირებადი ექსპერიმენტული ინოკულაციის შემდეგ, ჰაერში და გარემოში ვირუსის მხოლოდ 7% იყო გამოვლენილი პირველ სიმპტომამდე, რაც მიუთითებს იმაზე, რომ პრესიმპტომური გადაცემა პასუხისმგებელია ინფექციების მცირე ნაწილზე.[61]
სიმპტომების არმქონე პაციენტები შესაძლოა იყვნენ პრესიმპტომურ ფაზაში ან დარჩნენ მუდმივად ასიმპტომურები.
უსიმპტომო გადაცემა
უსიმპტომო შემთხვევების (ლაბორატორიულად დადასტურებული ინფექცია, არ აქვს სიმპტომები) მიერ ვირუსის გავრცელება აღწერილია; თუმცა, მტკიცებულება მეტწილად ჩინეთის მონაცემებს ეფუძნება და აქვს შეზღუდვები (მაგ. შემთხვევების მცირე რაოდენობა, ზოგიერთი შემთხვევა პრესიმპტომური იყო და არა უსიმპტომო).[62][63][64][65][66][67] არაერთი კვლევის თანახმად ვერ გამოვლინდა SARS-CoV-2-ის უსიმპტომო მტარებლებისგან ინფექციის გავრელების მტკიცებულება, მათ შორის ვუჰანის დაახლოებით 10 მილიონ მოსახლეზე ჩატარებული კვლევის მიხედვით.[68][69][70][71] ერთ-ერთი სისტემური მიმოხილვის თანახმად, უსიმპტომო ინდექს შემთხვევებთან ექსპოზირებული ადამიანების მხოლოდ 1% დაინფიცირდა, რაც მიუთითებს შეზღუდულ ინფექციურობაზე.[60]
ომიკრონის ვარიანტთან დაკავშირებული გადაცემის დინამიკის მტკიცებულებები შერეულია, ზოგიერთი კვლევა ვარაუდობს, რომ სიმპტომური შემთხვევები უფრო მეტად გადასცემდა ინფექციას უსიმპტომო შემთხვევებთან შედარებით, ხოლო სხვა კვლევები არ აჩვენებს განსხვავებას.[72]
მოსახლეობაში უსიმპტომო შემთხვევების პრევალენტობის გამოთვლა რთულია. ერთ-ერთმა მიმდინარე სისტემურმა მიმოხილვამ და მეტა-ანალიზმა აჩვენა, რომ მუდმივად უსიმპტომო შემთხვევების პროპორციის კვარტილთაშორისი დიაპაზონი იყო 14%-დან 50%-მდე სხვადასხვა კვლევაში; თუმცა, ჰეტეროგენულობა მაღალი იყო, ამიტომ კვლევამ არ შეაფასა საერთო უსიმპტომო ინფექციების საშუალო პროპორცია.[73] 130 000-ზე მეტი ადამიანის მეტა-ანალიზმა დაადგინა, რომ 21.7% რჩება უსიმპტომო ინფექციის მთელი პერიოდის განმავლობაში (პრესიმპტომური შემთხვევების გამოკლების შემდეგ). ქვეჯგუფის ანალიზმა აჩვენა, რომ უსიმპტომო ინფექციების საერთო მაჩვენებელი უფრო მაღალი იყო ორსულ ქალებში (48.8%) და ბავშვებში (32.1%). აფრიკულმა კვლევებმა აჩვენა ყველაზე მაღალი უსიმპტომო ინფექციის მაჩვენებელი, ხოლო აზიურმა კვლევებმა კი ყველაზე დაბალი.[74] უსიმპტომო ინფექციების გაერთიანებული პროცენტი შეფასებულია 25.5%-დან 32.4%-მდე ომიკრონის ვარიანტით ინფიცირებულ პაციენტებში.[75]
ასიმპტომური ტრანსმისიის წყარო შესაძლოა იყოს სამედიცინო პერსონალი. ინფიცირებული პაციენტების განყოფილებაში მომუშავე სამედიცინო პერსონალის 7.6% დადებითი იყო SARS-CoV-2-ის ანტისხეუელბზე; თუმცა, მათგან მხოლოდ 58% აღნიშნავდა სიმპტომების არსებობას.[76]
მიუხედავად იმისა, რომ მოზრდილ ბავშვებში უსიმპტომო ინფექციის მაჩვენებლები უფრო მაღალია, ვიდრე <1 წლის ასაკის ჩვილებში, სიმპტომური დაავადების მქონე ბავშვების უმრავლესობა, როგორც ჩანს, არ არის ინფექციის "ჩუმი" გამავრცელებელი.[21]
სუპერ-გავრცელება
მსგავსი მოვლენები დაკავშირებულია ეპიდაფეთქების დასაწყისში ფეთქებად, სწრაფ ზრდასა და შემდგომ ეტაპებზე სტაბილურ გავრცელებასთან. მაგალითები მოიცავს საეკლესიო/რელიგიურ შეკრებებს, ოჯახურ ან სოციალურ შეკრებებს, საგუნდო პრაქტიკას, დახურულ რეკრეაციულ სპორტულ აქტივობებს, ღამის კლუბებს, რესტორნებს, ბიზნეს კონფერენციებს და ქოლ-ცენტრებში მუშაობას. ფართოდ გავრცელებული ტრანსმისია აგრეთვე ფიქსირდება გრძელვადიანი მოვლის დაწესებულებებში, უსახლკაროთა თავშესაფრებში, პენიტენციურ დაწესებულებებში, ხორცისა და ფრინველის გადამამუშავებელ სათავსებში, ასევე საკრუიზო გემებზე.[77]
შეზღუდული გადაცემა დაფიქსირდა ბავშვთა მოვლის, სკოლისა და უნივერსიტეტის პირობებში.[78][79] არსებობს შეზრუდული რაოდენობის, მაღალი ხარისხის მტკიცებულებები სკოლებში გადაცემის მასშტაბის დასადგენად ან საზოგადოებაში ტრანსმისიის მაჩვენებლებთან მის შესადარებლად. თუმცა, მზარდია იმ მტკიცებულებების მოცულობა, რომლის თანახმად., მოსწავლეებთან შედარებით (1.66%), ინფექციის დაზიანებადობის მაჩვენებელი სასკოლო პერსონალში (1.18%) უფრო დაბალია. ახალი მტკიცებულებებით ნაჩვენებია, რომ ინფექციის შეტევის საერთო მაჩვენებელი და SARS-CoV-2 დადებითობის მაჩვენებელი სკოლის პირობებში დაბალია.[80][81] ადგილობრივ მოსახლეობაში ინფიცირების დაბალი ინციდენტობის პერიოდებში სკოლებში, სადაც არაფარმაცევტული ჩარევები განხორციელდა, სკოლის პერსონალისთვის რისკი ზოგადად არ არის უფრო მაღალი ვიდრე ზოგადი პოპულაციის რისკი და არ არის შედარებადი სხვა მაღალი რისკის პროფესიებთან (მაგ., ჯანდაცვის მუშაკები ). კვლევები, რომლებიც ასახავს ინფექციის მაღალი ინციდენტობის პერიოდებს, შეზღუდულია, მაგრამ აჩვენებს უფრო მაღალ რისკს სკოლის პერსონალისთვის ასეთ პირობებში.[82] ერთ-ერთი კვლევის თანახმად, ინგლისში, ინფიცირება შემთხვევების ახლო კონტაქტებში, მეორეულ სკოლებსა და კოლეჯებში, გახლდათ იშვიათი (დაახლოებით 2%).[83]
ამ პირთაგან ზოგიერთი შეიძლება იყოს ვირუსის სუპერ-გამავრცელებელი, მაგრამ ამის მიზეზი ხშირად უფრო კომპლექსურია, ვიდრე ვირუსის ჭარბი გამოყოფა და სავარაუდოდ სხვადასხვა ქცევითი თუ გარემო ფაქტორით აიხსნება.[84]
ვირუსის გავრცელების ფაქტორები
ინკუბაციის პერიოდი
ინკუბაციური პერიოდი გრძელდება 1-დან 14 დღემდე, მედიანა 5-7 დღეა.[85][86][87] თუმცა, ინკუბაციური პერიოდი თანდათან მცირდება ალფა ვარიანტიდან ომიკრონის ვარიანტამდე: თავდაპირველი ვირუსი - 5.2 დღე; ალფა ვარიანტი - 5 დღე; ბეტა ვარიანტი - 4.5 დღე; დელტა ვარიანტი - 4.41 დღე; ომიკრონის ვარიანტი - 3.42 დღე. საერთო საშუალო ინკუბაციური პერიოდი იყო 6.57 დღე (დიაპაზონი 1.8-დან 18.87 დღემდე) და უფრო მაღალი იყო ხანდაზმულებში (7.43 დღე) და ბავშვებში (8.82 დღე).[88]
რეპროდუქციის რიცხვი (R₀)
სისტემური მიმოხილვისა და ანალიზის მიხედვით, რეპროდუქციის ინდექსი არის 2.69 (ეფუძნება 2020 წლის იანვრიდან აგვისტომდე გამოქვეყნებულ ლიტერატურას). თუმცა, R₀ განსხვავდება სხვადასხვა ფაქტორების გათვალისწინებით.[89]
მეორეული დაზიანებადობის მაჩვენებელი
ჯამური მეორეული დაზიანებადობის მაჩვენებელი ინდექს შემთხვევის ახლო კონტაქტებში დაახლოებით 7%-ია. ეს მაჩვენებელი ეყრდნობა პანდემიის ადრეული პერიოდის მონაცემებს.[90] ჯამური მაჩვენებელი მერყეობს კონტაქტის გარემოებებს შორის, სავარაუდო მაჩვენებელია 18.9%-დან 21.1%-მდე საყოფაცხოვრებო გარემოში (2021 წლის 17 ივნისის მონაცემებით), 3.6%-ით სამედიცინო დაწესებულებებში, 1.2%-დან 5.9%-მდე სოციალურ გარემოში და 1.9%-მდე სამუშაო ადგილებზე. სიხშირე უფრო მაღალია სიმპტომური ინდექს შემთხვევების დროს, უსიმპტომო პაციენტებთან შედარებით; და ზრდასრულებში, ბავშვებთან შედარებით.[73][91][92][93]მოცირკულირე SARS-CoV-2 ვარიანტების გამო, მეორადი დაზიანებადობის უფრო მაღალი საერთო მაჩვენებელი - 37.3% დაფიქსირდა შინამეურნეობის გარემოში, შედარებით უფრო ახალი მეტა-ანალიზის მიხედვით.[94] ხანდაზმულთა მოვლის დაწესებულებებში მეორადი დაზიანებადობის საერთო გაერთიანებული მაჩვენებელი გაცილებით მაღალი იყო: 42% მაცხოვრებლებს შორის და 22% პერსონალს შორის.[95] ბავშვებში და ახალგაზრდებში ეს მაჩვენებელი უფრო მაღალი იყო შინამეურნეობაში, ვიდრე სკოლაში.[96] მეორადი დაზიანებადობის მაჩვენებელი საყოფაცხოვრებო გარემოში პედიატრიული საწყისი შემთხვევიდან გადაცემის გამო მერყეობდა 0%-დან 75%-მდე კვლევებში.[97]ომიკრონის ვარიანტის მეორადი დაზიანებადობის მაჩვენებელი უფრო მაღალია SARS-CoV-2-ის სხვა ვარიანტებთან შედარებით.[94][98]
ვირუსული დატვირთვა
ვირუსული დატვირთვა, როგორც ჩანს, ვირუსის გადაცემის წამყვანი მამოძრავებელია; უფრო მაღალი ვირუსული დატვირთვა დაკავშირებულია მეორეული დაზიანებადობის გაზრდილ მაჩვენებელთან და სიმპტომური დაავადების განვითარების უფრო მაღალ რისკთან.[99] ვირუსული დატვირთვა ყველაზე მაღალია ზემო სასუნთქ გზებში (ნაზოფარინქსი და ოროფარინქსი), ინფექციის საწყის ეტაპებზე (პიკს, ძირითადად დაავადების პირველ კვირას აღწევს) და შემდეგ იზრდება ქვედა სასუნთქ გზებშიც (ნახველი). ვირუსული დატვირთვა მცირდება სიმპტომების გამოვლენის შემდეგ. მძიმე დაავადების მქონე პაციენტებს ვირუსული დატვირთვა უფრო მაღალი აქვთ, ვიდრე მსუბუქ შემთხვევებს. ვირუსული დატვირთვის შედარება ზედა სასუნთქ ტრაქტში შესაძლებელია ასიმპტომურ და სიმპტომმურ პაციენტებს შორის; თუმცა, კვლევათა დიდი ნაწილი აჩვენებს, რომ ვირუსის კლირენსი ასიმპტომურ პაციენტებში უფრო მაღალია, სიმპტომურ პაციენტებთან შედარებით.[100]
ვირუსის გამოყოფა
ვირუსის გამოყოფის საშუალო ხანგრძლივობა დამოკიდებულია ნიმუშზე: 17 დღე ზედა სასუნთქ გზებში (მაქსიმუმ 83 დღე); 14.6 დღე ქვედა სასუნთქ გზებში (მაქსიმუმ 59 დღე); და 17.2 დღე განავალში (მაქსიმუმ 126 დღე). ვირუსის გამოყოფის ხანგრძლივობა უფრო მეტი იყო სიმპტომურ პაციენტებში, ვიდრე უსიმპტომოებში, ბავშვებში, შედარებით ზრდასრულებთან და ასევე მძიმე მდგომარეობაში მყოფ პაციენტებში, მსუბუქ პაციენტებთან შედარებით.[100][101] იმუნოკომპრომისული პაციენტები ვირუსს შეიძლება გამოყოფდნენ 2 თვის განმავლობაში.[102] არის ანგარიშები სუპერ გამომყოფების შესახებ, რომლებიც გამოყოფენ ვირუსს დიდი ხნის განმავლობაში (ყველაზე ხანგრძლივი შემთხვევა დაფიქსირდა, როდესაც პაციენტი ტესტზე დადებითი იყო 505 დღის განმავლობაში).[103] არ არსებობს ზუსტი მტკიცებულება ვირუსის გამოყოფის ხანგრძლივობისა და ინფექციურობის ხანგრძლივობის შესახებ.[104] დაავადების მსუბუქი და საშუალო სიმძიმის შემთხვევაში, სიმპტომების გამოვლენიდან 10 დღის შემდეგ, ხოლო მძიმე და კრიტიკული დაავადების შემთხვევაში 20 დღის შემდეგ არ ფიქსირდება სიცოცხლისუნარიანი ვირუსის იზოლირების ფაქტი, მიუხედავად ვირუსის განგრძობადი გამოყოფისა.[36] სრულად ვაქცინირებულ ადამიანებს შეიძლება ჰქონდეთ სიცოცხლისუნარიანი გამოყოფის მოკლე ხანგრძლივობა, ნაწილობრივ ვაქცინირებულ ან არავაქცინირებულ ადამიანებთან შედარებით.[105]
სიცოცხლისუნარიანი ვირუსის გამოდევნის საშუალო ხანგრძლივობა იყო 5.2 დღე ომიკრონის ვარიანტისთვის, ხოლო ხანგრძლივობა ოდნავ უფრო მაღალი იყო სიმპტომურ პაციენტებში უსიმპტომო პაციენტებთან შედარებით (თუმცა განსხვავება არ იყო სტატისტიკურად მნიშვნელოვანი).[106]
პათოფიზიოლოგია
ზუსტი პათოფიზიოლოგია უცნობია, ნაწილობრივ სიკვდილის შემდგომი კვლევების სიმცირის გამო.[107] პათოფიზიოლოგია წააგავს სხვა კორონავირუსულ ინფექციებს. თუმცა, ახალი მტკიცებულების თანახმად, COVID-19-ს აქვს გამორჩეული პათოფიზიოლოგიური ნიშნები, რაც გამოყოფს მას სხვა გენეზის რესპირატორული უკმარისობებისგან.[108]
SARS-CoV-2 ებმის ანგიოტენზინ-გარდამქმნელი ფერმენტის-2 (ACE2) რეცეპტორს მასპინძლის უჯრედებზე, განიცდის ინტერნალიზაციას და გადის რეპლიკაციას. ACE2 რეცეპტორები უხვად გვხვდება ზედა და ქვედა სასუნთქ გზებში და ასევე მიოკარდიუმის უჯრედებში, თირკმლის ეპითელიუმში, ენტეროციტებში, რამდენიმე ორგანოს ენდოთელიუმში, რაც ახსნის ფილტვგარე გამოვლინებებს, რომლებიც დაავადებას ახასიათებს.[109] სიკვდილის შემდგომ კვლევებში ვირუსული რნმ იდენტიფიცირებულია მრავალ ორგანოში.[107]
[Figure caption and citation for the preceding image starts]: COVID-19-ის და ხანგრძლივი COVID-ის მულტიორგანული გართულებები. SARS-CoV-2 ვირუსი ორგანოების უჯრედებში შედის ACE2 რეცეპტორის გამოყენებითBMJ. 2021;374:n1648 [Citation ends].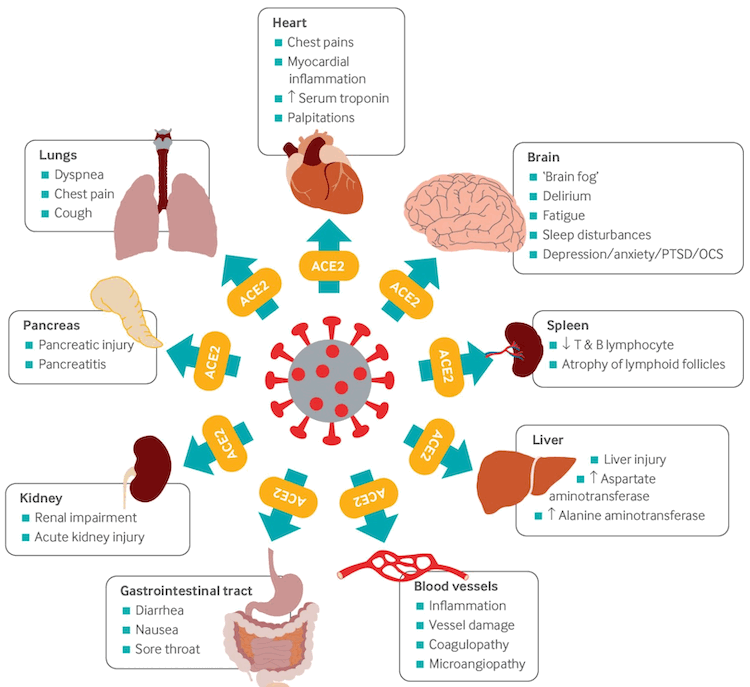
ვირუსი იყენებს მასპინძლის ტრანსმემბრანულ პროტეაზა სერინ 2-ს (TMPRSS2) ვირუსის წვეროს ცილის პრაიმინგის, ასევე ვირუსისა და მასპინძელი უჯრედის მემბრანების შეერთების მიზნით.[110] SARS-CoV-2-ის წვეროს ცილა ძირითად როლს ასრულებს ანგოტენზინგარდამქმნელი ფერმენტი 2-ის რეცეპტორის ამოცნობის და მემბრანის შერწყმის პროცესში. უნიკალური სტრუქტურული მახასიათებელი, SARS-CoV-1-თან შედარებით, ამ ვირუსს ანიჭებს მასპინძლის უჯრედზე ACE2-ის რეცეპტორთან შეკავშირების უფრო მაღალი აფინურობას.[111] ფურინის მსგავსი გაჭრის ადგილი, როგორც ჩანს, არ გვხვდება სხვა კორონავირუსებში.[112] SARS-CoV-2-ის წვერის ცილასა და ანგიოტენზინგარდამქმნელი ფერმენტი-2-ს (ACE2) შორის შეკავშირების ენერგია ყველაზე მაღალი აღმოჩნდა ადამიანებში ყველა სახეობიდან, რაც მიანიშნებს, რომ წვეროს ცილა უნიკალურად განვითარებულია ისე, რომ უკავშიორდება და აინფიცირებს ACE2-ის გამომხატველ უჯრედებს ადამიანში.[113] მზარდია იმ მტკიცებულებების რაოდენობა, რომელთა მიხედვით მხოლოდ წვეროს ცილასაც შეუძლია ენდოთელიური უჯრედების დაზიანება ანგიოტერნზინგარდამქმნელი ფერმენტი 2-ის დერეგულაციით და, საბოლოო ჯამში, მიტოქონდრიის ფუნქციის ინჰიბირების გზით. საჭიროა დამატებითი კვლევები, რათა გაირკვეს, შეუძლია თუ არა მხოლოდ წვეროს ცილას უჯრედის სასიგნალო ჯაჭვის გამოწვევა, რაც, თავის მხრივ, არაერთი ბიოლოგიურ პროცესს განაპირობებს.[114][115] SARS-CoV-2-ის სხვადასხვა ვარიანტი შესაძლოა მეტად გადმდები იყოს, სულ მცირე ნაწილობრივ, ანგიოტენზინგარდამქმნელი ფერმენტი 2-ის რეცეპტორის მიმართ წვეროს ცილის შეკავშირების გაძლიერებული აფინურობის მიზეზით.[116]
[Figure caption and citation for the preceding image starts]: ვირუსის რეპლიკაციის ციკლიBMJ. 2020;371:m3862 [Citation ends].
უჯრედების პირდაპირი დაზიანების გარდა, მძიმე დაავადება ხშირად რთულდება ინფექციური მიკროანგიოპათიით ან ჰიპერკოაგულაციური მდგომარეობით, რომელიც იწვევს კაპილარულ, ვენურ და/ან არტერიულ თრომბოზს, რამაც შეიძლება გამოიწვიოს სამიზნე ორგანოების დაზიანება დისტალური თრომბული ან ემბოლიური დაავადების გამო. ფართოდ გავრცელებული მიკროთრომბები გამოვლენილია თითქმის ყველა ორგანოში აუტოფსიურ კვლევებში. ფატალურ შემთხვევებში წამყვანი პათოლოგიური ნიშნებია: ალვეოლების დიფუზური დაზიანება, კოაგულოპათია და ჰემოდინამიკური უკმარისობა. ფილტვგარე ორგანოების ჩართულობა გულისხმობს მსუბუქ პარენქიმულ ანთებას (მაგ. მიოკარდიტი, ჰეპატიტი, ენცეფალიტი). პირდაპირი ვირუსული ციტოპათიური დაზიანება ფილტვგარე ორგანოებში არ ფიქსირდებოდა ორგანული უკმარისობის მიზეზად.[107][109][117] ფილტვგარე ორგანოებში გამოვლენილი ნიშნების უმეტესობა დაკავშირებული იყო ქრონიკულ დაავადებებთან.[118] SARS-CoV-2-ით გამოწვეულმა ენდოთელიტმა შეიძლება ითამაშოს როლი როგორც რესპირატორულ, ისე არა რესპირატორულ გამოვლინებებში.[119]
სამი ძირითადი ქსოვილის ფენოტიპი გაჩნდა სიკვდილის შემდგომი ფილტვის ქსოვილში: კლასიკური ფენოტიპი, რომელიც ხასიათდება პროგრესირებადი დიფუზური ალვეოლარული დაზიანებით; ბრონქოპნევმონია მეორადი ინფექციისგან; და ქსოვილის თრომბოზი. ეს ფენოტიპები არ არის ურთიერთგამომრიცხავი და შეიძლება იყოს ურთიერთერთგადამფარავი.[120] ფილტვის მძიმე დაავადება არის ფიბროზული რემოდელირების და მეორადი ლობულური მიკროიშემიის შედეგი, რაც იწვევს ფიბროზული ინტერსტიციული ფილტვის დაავადების გამორჩეულ ფორმას.[121]
SARS-CoV-2 პლაცენტიტი არის განსხვავებული პათოლოგიური ერთეული, რომელიც დაფიქსირდა ორსულ ქალებში და ახასიათებს მასიური პერივილოზური ფიბრინის დეპონირება და ქრონიკული ჰისტიოციტური ინტერვილოზიტი. ეს დაკავშირებულია სპონტანური აბორტის გაზრდილ რისკთან.[122]
გენეტიკურ ფაქტორებს შეიძლება ჰქონდეს როლი ინფექციისადმი მიდრეკილებასა და დაავადების სიმძიმეზე; თუმცა საჭიროა შემდგომი კვლევები.[123][124]
კლასიფიკაცია
მძიმე მწვავე რესპირატორული სინდრომის კორონავირუსი 2-ის (SARS-CoV-2) ვარიანტების კლასიფიკაცია
ყველა ვირუსი, მათ შორის SARS-CoV-2, იცვლება დროთა განმავლობაში. ცვლილებათა უმრავლესობას აქვს მცირე ან არ აქვს გავლენა ვირუსის თვისებებზე; თუმცა, ზოგიერთი ცვლილება შესაძლოა ზემოქმედებდეს ვირუსის გადაცემის უნარზე, დაავადების სიმძიმეზე, დიაგნოსტიკური ტესტების სიზუსტეზე, თერაპიულ საშუალებებსა და ვაქცინებზე.
SARS-CoV-2 ვარიანტები ჩნდება და ცირკულირებს მსოფლიოს მასშტაბით პანდემიის დაწყების დღიდან. მათი მონიტორინგი რუტინულად მიმდინარეობს და ისინი კლასიფიცირდებიან, როგორც მონიტორინგის ქვეშ მყოფი ვარიანტები, ინტერესის ვარიანტები ან შემაშფოთებელი ვარიანტები ჯანმრთელობის მსოფლიო ორგანიზაციის მიერ.[2] კლასიფიკაციის სისტემები ქვეყნების მიხედვით შეიძლება განსხვავდებოდეს.
დიდ ბრიტანეთში, დიდი ბრიტანეთის ჯანმრთელობის უსაფრთხოების სააგენტოს (UKHSA) მიერ ვარიანტები კლასიფიცირდება როგორც შემაშფოთებელი, განსაზღვრული ან სიგნალი.[3]
აშშ-ის დაავადებათა კონტროლისა და პრევენციის ცენტრების მიერ ვარიანტები კლასიფიცირებულია, როგორც მონიტორინგის ქვეშ მყოფი ვარიანტები, ინტერესის ვარიანტები, საგულისხმო ვარიანტები ან მნიშვნელოვანი შედეგების ვარიანტები.[4]
ჯანმრთლობის მსოფლიო ორგანიზაციამ შექმნა მარტივი ეტიკეტები შემაშფოთებელი ვარიანტებისთვის ბერძნული ანბანის ასოების გამოყენებით. ადრე ინტერესის ვარიანტებიც ბერძნული ანბანის მიხედვით სახელდებოდა, მაგრამ ახლა ასე აღარ არის. ეს არ ცვლის არსებულ სამეცნიერო სახელებს (მაგ. Pango, Nextstrain, GISAID), რომლებიც კვლავ გამოიყენება კვლევებში.[2]
ვარიანტი მონიტორინგის ქვეშ
ჯანმრთელობის მსოფლიო ორგანიზაცია განსაზღვრავს მონიტორინგის ქვეშ მყოფ ვარიანტს, როგორც ვარიანტს გენეტიკური ცვლილებებით, რომლებიც, სავარაუდოდ, გავლენას ახდენს ვირუსის მახასიათებლებზე და ზრდის ვირუსის გამრავლების რისკს სხვა მოცირკულირე ვარიანტებზე მეტად (შედარებითი ზრდის უპირატესობა გლობალურად ან ჯანმრთელობის მსოფლიო ორგანიზაციის მხოლოდ ერთ რეგიონში), მაგრამ ფენოტიპური ან ეპიდემიოლოგიური ზემოქმედების მტკიცებულებები გაურკვეველია, რაც საჭიროებს გაძლიერებულ მონიტორინგს და ხელახლა შეფასებას ახალი მტკიცებულებების მოლოდინში. თუ ვარიანტს აქვს უჩვეულოდ დიდი რაოდენობით მუტაციები ცნობილ ანტიგენურ უბნებში, მაგრამ მცირე რაოდენობით სიკვენსები, და შეუძლებელია მისი შედარებითი ზრდის უპირატესობის შეფასება, ასეთი ვარიანტი ასევე შეიძლება განისაზღვროს მონიტორინგის ქვეშ მყოფ ვარიანტად, თუ არსებობს მტკიცებულება საზოგადოებრივ პირობებში გავრცელებაზე ორ ან მეტ ქვეყანაში, 2-4 კვირის პერიოდის განმავლობაში.[5]
ინტერესის ვარიანტი
ჯანმრთელობის მსოფლიო ორგანიზაცია ინტერესის ვარიანტს განსაზღვრავს, როგორც გენეტიკური ცვლილებების მქონე ვარიანტს, რომელზეც მოსალოდნელია ან ცნობილია, რომ შეცვლილი აქვს მახასიათებლები, მაგ. ტრანსმისიულობა, ვირულენტობა, ანტისხეულებისგან თავის დაძვრენა, სამკურნალო საშუალებების მიმართ მოწყვლადობა და დიაგნოსტიკის სირთულე; და ფიქსირდება შედარებითი ზრდის უპირატესობა სხვა მოცირკულირე ვარიანტებთან შედარებით ჯანმოს ორ ან მეტ რეგიონში, მზარდი პრევალენტობით და შემთხვევათა რაოდენობის ზრდით, ან რაიმე სხვა ეპიდემიოლოგიური შედეგებით, რაც მიანიშნებს საზოგადოებრივი ჯანმრთელობის გლობალურ საფრთხეზე.[5]
საგულისხმო ვარიანტი
ჯანმრთელობის მსოფლიო ორგანიზაცია განსაზღვრავს საგულისხმო/შემაშფოთებელ ვარიანტს, როგორც ვარიანტს, რომელიც აკმაყოფილებს ინტერესის ვარიანტის განმარტებას (იხ. ზემოთ) და ასოცირდება ზომიერი ან მაღალი დონის მტკიცებულებებთან (ჯანმო-ს მიერ შესრულებული რისკის შეფასების გზით), ჩამოთვლილთაგან ერთი კრიტერიუმისთვის მაინც:[5]
კლინიკური დაავადების სიმძიმის საზიანო ცვლილება, ან
ეპიდემიოლოგიური სურათის ცვლილება, რომელიც ახდენს არსებით გავლენას ჯანდაცვის სისტემების უნარზე, უზრუნველყონ ზრუნვა პაციენტებზე COVID-19 ან სხვა დაავადებებით და, შესაბამისად, საჭიროებს ზოგად საზოგადოებრივი ჯანმრთელობის ჩარევებს, ან
არსებული ვაქცინების ეფექტურობის მნიშვნელოვანი დაქვეითება მძიმე დაავადებისგან თავის დასაცავად.
ადრინდელი შემაშფოთებელი ვარიანტები
SARS-CoV-2 ვარიანტების უმეტესობა ახლა გამქრალია, ამჟმინდელი მოცირკულირე შემაშფოთებელი ვარიანტია ომიკრონ ვარიანტი და მისი ქვევარიანტები (იხ ქვემოთ). ვარიანტები თანმიმდევრულად ცვლიდნენ ერთმანეთს პანდემიის დაწყებიდან, ყველაზე წარმატებული ვარიანტები იყო ალფა (B.1.1.7), დელტა (B.1.617.2), და ომიკრონი (B.1.1.529). ალფა და დელტა გაჩნდა 2020 წლის ბოლოს, ხოლო ომიკრონი გამოჩნდა 2021 წლის ბოლოს.
ალფა ვარიანტი იყო უფრო ადვილად გავრცელებადი, ვიდრე თავდაპირველი ვირუსი და ასოცირდებოდა ჰოსპიტალიზაციისა და ინტენსიური თერაპიის განყოფილებაში მოთავსების მომატებულ რისკთან (რაც მიუთითებს უფრო მძიმე დაავადებაზე), მაგრამ არა სიკვდილობის მატებასთან, თავდაპირველ ვირუსთან შედარებით, თუმცა მონაცემები ურთიერთსაწინააღმდეგოა. ვარიანტი არ იყო დაკავშირებული სიმპტომების ცვლილებებთან ან მათ ხანგრძლივობასთან.[6][7][8][9]
დელტას ვარიანტი უფრო გადამდები იყო ვიდრე თავდაპირველი ვირუსი და ალფა ვარიანტი და ასოცირებული იყო ჰოსპიტალიზაციის მომატებულ რისკთან (უფრო მძიმე დაავადება) შედარებით ალფა და ბეტა ვარიანტებთან, რომლებიც იმავე დროს ცირკულირებდნენ. თუმცა, მონაცემები ზუსტი არ ყოფილა. ლეტალობის მაჩვენებელი ნაკლები იყო ალფა ვარიანტთან შედარებით.[3][10]
ომიკრონის ვარიანტი ვარიანტი
ამჟამად ცირკულირებენ ომიკრონის ვარიანტები. ომიკრონის ვარიანტი მოიცავს მშობლის შტოს B.1.1.529 და მის შთამომავლებს (ქვევარიანტები) BA.1, BA.2, BA.3, BA.4 და BA.5, ისევე როგორც მათ სხვადასხვა ქვეხაზებს.
ჯანმრთელობის მსოფლიო ორგანიზაცია ომიკრონის ქვეხაზების კლასიფიკაციას ცალკეულად ახდენს, შემდეგ კატეგორიებად: ვარიანტები მონიტორინგის ქვეშ, ინტერესის ვარიანტები და შემაშფოთებელი ვარიანტები. ადრე, ომიკრონის ყველა ქვეხაზი კლასიფიცირებული იყო, როგორც შემაშფოთებელი ვარიანტები. ეს კლასიფიკაცია არ იყო საკმარისად დეტალური, რათა შეგვედარებინა ახალი შთამომავალი ხაზები (შეცვლილი ფენოტიპებით) ომიკრონის მშობელ ხაზებთან BA.1, BA.2, BA.3, BA4 და BA.5.[11]
ომიკრონი არის მეტად განსხვავებული ვარიანტი მუტაციების მაღალი რაოდენობით. არ არსებობს გადაცემის გზა, რომელიც აკავშირებს Omicron-ს მის წინამორბედებთან (ალფა, დელტა) და შეფასებულია, რომ მისი უახლოესი დადგენილი გენეტიკური წინაპარის არსებობა, სავარაუდოდ, 2020 წლის შუა პერიოდის შემდეგ თარიღდება.[12] შემთხვევები პირველად სამხრეთ აფრიკაში 2021 წლის ნოემბერში დაფიქსირდა. ომიკრონს აქვს მნიშვნელოვანი ზრდის უპირატესობა დელტასთან შედარებით და სწრაფად ჩაანაცვლა დელტა გლობალურად. ომიკრონის ვარიანტი გახდა დომინანტური ვარიანტი ბევრ ქვეყანაში და შეადგენდა საჯაროდ ხელმისაწვდომი სეკვენსების 98%-ზე მეტს 2022 წლის თებერვლიდან.[11]
მონაცემები მიუთითებს ომიკრონის ვარიანტის შემცირებული სიმძიმისა და სიკვდილობის მტკიცებულებაზე დელტა ვარიანტთან შედარებით, ასაკის, სქესის, ეთნიკური წარმომავლობის, გადატანილი ინფექციის, ვაქცინაციის სტატუსის, თანმხლები დაავადებების და რეგიონის და საჯარო/კერძო სექტორის ეფექტების კორექტირების შემდეგ.[13][14] სიკვდილობის უმეტესობა დაფიქსირდა ≥65 წელზე უფროსი ასაკის ზრდასრულებში და ≥3 თანმხლები სამედიცინო მდგომარეობის მქონე პაციენტებში.[15] ცხოველთა კვლევებიდან და ადამიანის ქვედა და ზედა სასუნთქი გზების ex vivo კულტურებიდან მიღებული მტკიცებულებები მიუთითებს იმაზე, რომ ომიკრონი არ აინფიცირებს უჯრედებს ფილტვებში ღრმად ისე ადვილად, როგორც ზედა სასუნთქი გზების უჯრედებს.[16][17] გავრცელება, დაავადების სიმძიმე/ჰოსპიტალიზაციის მაჩვენებელი და ვაქცინის ეფექტურობა შეიძლება განსხვავდებოდეს ომიკრონის სპეციფიკური ქვეხაზიდან გამომდინარე.
პანდემიის დროს გამოვლინდა SARS-CoV-2-ის რამდენიმე რეკომბინანტული ვარიანტი და მათი უმრავლესობა ვირუსს არანაირ უპირატესობას არ ანიჭებს.
ამჟამად მიმოქცევაში არსებული ვარიანტები
ამჟამად არ ცირკულირებს არცერთი შემაშფოთებელი ვარიანტი. დამატებითი ინფორმაციის მისაღებად გაეცანით ადგილობრივი საზოგადოებრივი ჯანდაცვის ორგანოების მითითებებს. ხელმისაწვდომია ჩამოთვლილი რესურსები:
ამ მასალის გამოყენება ექვემდებარება ჩვენს განცხადებას
