COPD-ის მკურნალობის მთავარ მიზანს წარმოადგენს, სიმპტომების პრევენცია და კონტროლი, სიმძიმისა და გამწვავებების რიცხვის შემცირება, რესპირატორული შესაძლებლობების და დატვირთვის მიმართ ტოლერანტობის ზრდა და სიკვდილობის შემცირება.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
სისტემური მიმოხილვით FEV1-ის დაკლების სიჩქარე ზომიერად მცირდება პაციენტებთან, რომლებსაც ფარმაკოლოგიური თერაპია უტარდებათ.[78]Celli BR, Anderson JA, Cowans NJ, et al. Pharmacotherapy and lung function decline in patients with chronic obstructive pulmonary disease. A systematic review. Am J Respir Crit Care Med. 2021 Mar 15;203(6):689-98.
https://www.atsjournals.org/doi/10.1164/rccm.202005-1854OC
http://www.ncbi.nlm.nih.gov/pubmed/32966751?tool=bestpractice.com
[79]Yang IA, Ferry OR, Clarke MS, et al. Inhaled corticosteroids versus placebo for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2023 Mar 27;(3):CD002991.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD002991.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/36971693?tool=bestpractice.com
საჭიროა შემდგომი კვლევა იმის გასარკვევად, თუ რომელი პაციენტები იღებენ ყველაზე მეტ სარგებელს.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
არსებობს თერაპიის ეტაპობრივი მიდგომა და მკურნალობა უნდა იყოს ინდივიდუალური ჯანმრთელობის ზოგადი მდგომარეობის და თანმხლები დაავადებების გათვალისწინებით. თუ COPD-ით დაავადებულ პაციენტს აქვს თანმხლები ასთმა, ის უპირველეს ყოვლისა უნდა იმართებოდეს ასთმის გაიდლაინების მიხედვით.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
იხ ასთმა მოზრდილებში. ალფა-1 ანტიტრიფსინის დეფიციტის მართვის შესახებ დეტალებისთვის იხ ალფა-1 ანტიტრიფსინის დეფიციტი.
თერაპიული მიდგომა მოიცავს რისკ-ფაქტორების შემცირებას, დაავადების შესაბამის შეფასებას, პაციენტის განათლებას, სტაბილური COPD-ის ფარმაკოლოგიურ და არაფარმაკოლოგიურ მართვას და მისი გამწვავებების მკურნალობას.
ჯანმრთელობის მსოფლიო ორგანიზაცია რეკომენდაციას უწევს ფქოდ-ის სტაბილური ფორმის სამართავ ჩამოთვლილ მინიმალურ ჩარევებს პირველადი ჯანდაცვის პირობებში.
WHO: package of essential noncommunicable (PEN) disease interventions for primary health care
Opens in new window
დაავადების მიმდინარეობის შეფასება და მონიტორინგი
COPD -ის მიმდინარე მონიტორინგი და შეფასება მკურნალობის მიზნის მიღწევას უზრუნველყოფს. ცხოვრების ხარისხი და პაციენტების კეთილდღეობის განცდა უმჯობესდება და ჰოსპიტალიზაცია მნიშვნელოვნად მცირდება, როდესაც გამოყენებულია დაავადების თვით- ან პროფესიული მონიტორინგი.[80]Lemmens KM, Nieboer AP, Huijsman R. A systematic review of integrated use of disease-management interventions in asthma and COPD. Respir Med. 2009 May;103(5):670-91.
http://www.ncbi.nlm.nih.gov/pubmed/19155168?tool=bestpractice.com
სამედიცინო ისტორიის ასეთი შეფასება უნდა მოიცავდეს:
რისკ-ფაქტორების ექსპოზირებას და პრევენციულ ზომებს:
თამბაქოს მოწევა
შენობის შიგნით და გარეთ ჰაერის დაბინძურება
პროფესიული ექსპოზიცია(კვამლი,მტვერი და სხვ.)
გრიპის და პნევმოკოკის ვაქცინაცია
ავადმყოფობის მიმდინარეობა და გართულებების გამოვლინება:
ფიზიკური დატვირთვის მიმართ ტოლერანტობის შემცირება
სიმპტომების მატება
ძილის ხარისხის გაუარესება
სამსახურის ან სხვა აქტივობებეის გაცდენა
მედიკამენტური ან სხვა სახის მკურნალობა:
ინჰალატორის გამოყენების სიხშირე
ყველა ახალი მედიკამენტი
სამედიცინო რეჟიმის დაცვის ხარისხი
ინჰალატორის სწორედ გამოყენების უნარი
გვერდითი მოვლენები
გამწვავებების ანამნეზი
სასწრაფო დახმარების ან გადაუდებელი თერაპიის განყოფილებებში ვიზიტების რაოდენობა
პერორული კორტიკოსტეროიდების ახლო წარსულში გამოყენების მწვავე საჭიროება
გამწვავების სიხშირე, სიმძიმე და სავარაუდო მიზეზები უნდა შეფასდეს
თანმხლები დაავადებები:
ასევე, ფილტვის ფუნქციური ტესტები უნდა ჩატარდეს შედარებით ადრე ან ხშირად იმ შემთხვევაში, თუ სიმპტომები მნიშვნელოვნად მატულობს.
Cochrane-ის ერთმა მიმოხილვამ დაადგინა, რომ დაავადების ინტეგრირებული მენეჯმენტი (IDM), რომლის დროსაც ჯანდაცვის რამდენიმე პროვაიდერი (ფიზიოთერაპევტი, პულმონოლოგი, მედდა და ა.შ.) ერთდეოულად მუშაობს პაციენტთან, სავარაუდოდ აუმჯობესებს დაავადებისთვის სპეციფიური სიცოცხლის ხარისხს, პაციენტის ფიზიკურ შესაძლებლობებს, ჰოსპიტალიზაციის საჭიროებას და ჰოსპიტალში დაყოვნებას.[81]Poot CC, Meijer E, Kruis AL, et al. Integrated disease management interventions for patients with chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2021 Sep 8;(9):CD009437.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD009437.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/34495549?tool=bestpractice.com
[  ]
What are the effects of integrated disease management (IDM) interventions for people with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.3877/fullShow me the answer[Evidence A]76ea49b7-0eff-463d-90da-4755f900cedfccaAრა შედეგები მოაქვს დაავადების ინტეგრირებული მართვის (IDM) ინტერვენციებს ფილტვების ქრონიკული ობსტრუქციული დაავადების (COPD) მქონე ადამიანებისთვის?
]
What are the effects of integrated disease management (IDM) interventions for people with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.3877/fullShow me the answer[Evidence A]76ea49b7-0eff-463d-90da-4755f900cedfccaAრა შედეგები მოაქვს დაავადების ინტეგრირებული მართვის (IDM) ინტერვენციებს ფილტვების ქრონიკული ობსტრუქციული დაავადების (COPD) მქონე ადამიანებისთვის?
ქრონიკული მართვა: საფეხურეობრივი მკურნალობა GOLD -ის კლასიფიკაციის მიხედვით
ფქოდ-ის გლობალური ინიციატივის გაიდლაინების თანახმად რეკომენდებულია, რომ პაციენტის საწყისი მკურნალობა დიაგნოზის დროს დადგინდეს პაციენტის ფქოდ-ის გლობალური ინიციატივის ჯგუფის მიხედვით:[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
ყველა პაციენტს სიმპტომების დაუყოვნებლივი შემსუბუქებისთვის უნდა დაენიშნოს ხანოკლე მოქმედების ბრონქოდილატატორი ხანმოკლე მოქმედების ბრონქოდილატორებზე ორგანიზმის არასათანადო დამყოლობა შეიძლება იყოს გამწვავების გამოვლინება.
A ჯგუფის პაციენტებისთვის (რამდენიმე სიმპტომი [ბრიტანეთის სამედიცინო კვლევის საბჭოს მოდიფიცირებული სკალით {mMRC} 0-1 ან COPD შეფასების ტესტით {CAT} <10] და გამწვავების დაბალი რისკი [0-1 გამწვავება წელიწადში, არ საჭიროებს ჰოსპიტალიზაციას]), ხანმოკლე ან ხანგრძლივი მოქმედების ბრონქოდილატატორი რეკომენდებულია როგორც პირველი რიგის მკურნალობა. ხანგრძლივი მოქმედების ბეტა-2 აგონისტები (LABAs) და ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტების (LAMAs) დანიშვნა უპირატესია ხანმოკლე მოქმედების ბრონქოდილატატორებთან შედარებით, გარდა იმ პაციენტებისა, რომლებსაც ძალიან იშვიათი ქოშინი აქვთ.
B ჯგუფის პაციენტებისთვის (მეტი სიმპტომები [mMRC ≥2 ან CAT ≥10] და გამწვავების დაბალი რისკი [0-1 გამწვავება წელიწადში, არ საჭიროებს ჰოსპიტალიზაციას]), LABA/LAMA კომბინირებული მკურნალობა უნდა დაინიშნოს პირველ რიგში, თუ არ არის გვერდითი მოვლენების ან ხელმისაწვდომობის პრობლემები. წინააღმდეგ შემთხვევაში, შეიძლება დაინიშნოს მონოთერაპია LAMA ან LABA. არ არსებობს მტკიცებულება იმის თაობაზე, რომ რეკომენდაცია უპირატესად ერთი კლასის ხანგრძლივი მოქმედების ბრონქოდილატატორით მონოთერაპიას გაეწიოს, მსხვა ბრონქოდილატატორით მონოთერაპიასთან შედარებით. ბრონქოდილატატორის შერჩევა დამოკიდებული უნდა იყოს იმაზე თუ როგორია პაციენტის აღქმა სიმპტომების შემსუბუქებასთან დაკავშირებით. B ჯგუფში მყოფ პაციენტებს შეიძლება ჰქონდეთ თანმხლები დაავადებები, რომლებიც დამატებით სიმპტომებს იწვევენ და პროგნოზზე გავლენას ახდენენ, ამიტომ ნებისმიერი პოტენციური თანმხლები დაავადება უნდა იქნას გათვალისწინებული და გამოკვლეული.
E ჯგუფის პაციენტებისთვის (გამწვავების მაღალი რისკი [≥2 გამწვავება წელიწადში, ან ≥1, რომელიც საჭიროებს ჰოსპიტალიზაციას] და სიმპტომების გამოვლენის ნებისმიერი დონე), LABA/LAMA კომბინირებული მკურნალობა პირველი რიგის მკურნალობაა გვერდითი მოვლენების ან ხელმისაწვდომობის პრობლემების არარსებობის შემთხვევაში. საინჰალაციო კორტიკოსტეროიდი (ICS) LABA/LAMA კომბინაციაზე შეიძლება დაემატოს, თუ პაციენტის სისხლში ეოზინოფილების რაოდენობა ≥300 უჯრედი/მიკროლიტრია (სამმაგი თერაპია). ICS-ის გამოყენება მარტო LABA-სთან ერთად არ არის რეკომენდებული.
[Figure caption and citation for the preceding image starts]: COPD-ის საწყისი ფარმაკოლოგიური მართვაფილტვების ქრონიკული ობსტრუქციული დაავადების გლობალური ინიციატივა (GOLD). ფილტვების ქრონიკული ობსტრუქციული დაავადების დიაგნოსტიკის, მართვისა და პრევენციის გლობალური სტრატეგია (2023 წლის ანგარიში); რგამოყენებულია ნებართვით [Citation ends].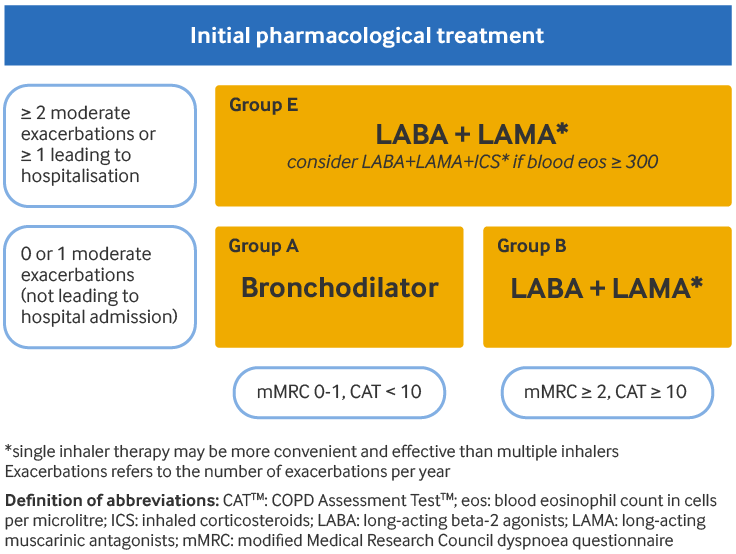
შემდგომი მკურნალობა განისაზღვრება პაციენტის ქოშინის/ფიზიკური დატვირთვის შეზღუდვის ხარისხის და გამწვავებების სიხშირის განხილვის შემდეგ და არ არის დამოუკიდებელი დიაგნოსტიკისას განსაზღვრულ პაციენტის GOLD-ის ჯგუფზე. GOLD-ი გირჩევთ მკურნალობის სხვადასხვა გზას, რაც დამოკიდებულია იმაზე, რომელია მკურნალობის ძირითადი მიზანი: ქოშინის/ფიზიკური დატვირთვის შეზღუდვის სიმპტომების მოხსნა, თუ გამწვავების შემცირება. თუ მკურნალობა საჭიროა ორივე მიზნით, კლინიცისტები უნდა მიჰყვნენ გამწვავების სამკურნალო მიდგომას.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
ნებისმიერი სახით მკურნალობის კორექტირებამდე პაციენტებთან განხილული უნდა იყოს სიმპტომები და გამწვავების რისკი და ასევე უნდა შეფასდეს ინჰალატორის გამოყენების ტექნიკა და მკურნალობისადმი დამყოლობა. უნდა შეფასდეს არაფარმაკოლოგიური მკურნალობის როლიც. თუ პაციენტის პასუხი საწყის მკურნალობაზე შესაბამისია, მაშინ საწყისი მკურნალობა შეიძლება შენარჩუნდეს. ფარმაკოლოგიური მკურნალობის კორექტირება შეიძლება მიოცავდეს თერაპიის ესკალაციას ან დეესკალაციას, ასევე ინჰალატორის გამოცვლას ან იმავე ჯგუფის მედიკამენტის სხვა წარმომადგენლის დანიშვნას. თუ მკურნალობა შეიცვალა, მაშინ კლინიცისტებმა უნდა განიხილონ პაციენტის კლინიკური პასუხი და ნებისმიერი პოტენციური გვერდითი მოვლენა.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
რეკომენდებული ესკალაციური თერაპია პერსისტენტული დისპნოეს/ფიზიკური დატვირთვის შეზღუდვის დროს, თავდაპირველი თერაპიის შემდეგ, ასეთია:[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
პაციენტებმა, რომლებიც იღებენ ხანგრძლივი მოქმედების ბრონქოდილატატორის მონოთერაპიას, უნდა დაიწყონ მეორე ხანგრძლივი მოქმედების ბრონქოდილატატორი. თუ სიმპტომები არ გაუმჯობესდება, ინჰალატორის მოწყობილობის ან მედიკამენტის შეცვლა შეიძლება იქნას განხილული.
გამოსაკვლევი და სამკურნალოა სხვა მიზეზებით გამოწვეული დისპნოე. ასევე უნდა შეფასდეს ინჰალატორის გამოყენების ტექნიკა, ვინაიდან არასწორად გამოყენების შემთხვევაში მკურნალობა წარუმატებელი იქნება.
რეკომენდებული ესკალაციური თერაპია პერსისტენტული გამწვავებების დროს, თავდაპირველი თერაპიის შემდეგ, ასეთია:[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
პაციენტებმა, რომლებსაც ხანგრძლივი მოქმედების ბრონქოდილატატორით მონოთერაპია უტარდებათ, უნდა გააფართოვონ თერაპია LABA/LAMA-მდე. სისხლში ეოზინოფილების რაოდენობის მიხედვით შეიძლება პროგნოზირება, რომელ პაციენტს ექნება პასუხი კორტიკოსტეროიდებით მკურნალობაზე.[70]Bafadhel M, Peterson S, De Blas MA, et al. Predictors of exacerbation risk and response to budesonide in patients with chronic obstructive pulmonary disease: a post-hoc analysis of three randomised trials. Lancet Respir Med. 2018 Feb;6(2):117-26.
http://www.ncbi.nlm.nih.gov/pubmed/29331313?tool=bestpractice.com
[71]Harries TH, Rowland V, Corrigan CJ, et al. Blood eosinophil count, a marker of inhaled corticosteroid effectiveness in preventing COPD exacerbations in post-hoc RCT and observational studies: systematic review and meta-analysis. Respir Res. 2020 Jan 3;21(1):3.
https://respiratory-research.biomedcentral.com/articles/10.1186/s12931-019-1268-7
http://www.ncbi.nlm.nih.gov/pubmed/31900184?tool=bestpractice.com
[72]Oshagbemi OA, Odiba JO, Daniel A, et al. Absolute blood eosinophil counts to guide inhaled corticosteroids therapy among patients with COPD: systematic review and meta-analysis. Curr Drug Targets. 2019;20(16):1670-9.
http://www.ncbi.nlm.nih.gov/pubmed/31393244?tool=bestpractice.com
LABA/LAMA/ICS-ით სამმაგ თერაპიაზე გადასვლა შეიძლება განხილულ იყოს პაციენტებთან, რომლებიც იტარებენ ხანგრძლივი მოქმედების ბრონქოდილატატორით მონოთერაპიას, თუ მათთან პერიფერიული ეოზინოფილების რაოდენობა არის ≥300 უჯრედი/მიკროლიტრი. ნაკლებად სავარაუდოა, რომ ICS სასარგებლო იყოს პაციენტებთან, რომელთა სისხლში ეოზინოფილების რაოდენობა არის <100 უჯრედი/მიკროლიტრი.
თუ პაციენტი იღებს ხანგრძლივი მოქმედების ბეტა-2 აგონისტის/მუსკარინული ანტაგონისტის კომბინაციას და ეოზინოფილები არის ≥100 უჯრედი/მიკროლიტრზე, საჭიროა ესკალაცია სამმაგ თერაპიაზე- ხანგრძლივი მოქმედების ბეტა-2 აგონისტის/მუსკარინული ანტაგონისტი/საინჰალაციო კორტიკოსტეროიდი. მრავალი კვლევის მიხედვით, რეკომენდებულია სამმაგი თერაპია ხანგრძლივი მოქმედების ბეტა-2 აგონისტი/ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტი/ინჰალაციური კორტიკოსტეროიდებით, რადგან აღნიშნული უპირატესია ერთმაგ ან ორმაგ თერაპიასთან შედარებით ხანგრძლივი მოქმედების ბეტა-2 აგონისტი/ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტის ან ხანგრძლივი მოქმედების ბეტა-2 აგონისტი/ინჰალაციური კორტიკოსტეროიდების კომბინაციებში, საშუალო-მძიმე ფქოდ-ის გამწვავებების და ჰოსპიტალიზაციის სიხშირის შემცირების თვალსაზრისით.[74]Cazzola M, Rogliani P, Calzetta L, et al. Triple therapy versus single and dual long-acting bronchodilator therapy in COPD: a systematic review and meta-analysis. Eur Respir J. 2018 Dec 13;52(6):1801586.
https://erj.ersjournals.com/content/52/6/1801586
http://www.ncbi.nlm.nih.gov/pubmed/30309975?tool=bestpractice.com
[82]Singh D, Papi A, Corradi M, et al. Single inhaler triple therapy versus inhaled corticosteroid plus long-acting beta2-agonist therapy for chronic obstructive pulmonary disease (TRILOGY): a double-blind, parallel group, randomised controlled trial. Lancet. 2016 Sep 3;388(10048):963-73.
http://www.ncbi.nlm.nih.gov/pubmed/27598678?tool=bestpractice.com
[83]Vestbo J, Papi A, Corradi M, et al. Single inhaler extrafine triple therapy versus long-acting muscarinic antagonist therapy for chronic obstructive pulmonary disease (TRINITY): a double-blind, parallel group, randomised controlled trial. Lancet. 2017 May 13;389(10082):1919-29.
http://www.ncbi.nlm.nih.gov/pubmed/28385353?tool=bestpractice.com
[84]Papi A, Vestbo J, Fabbri L, et al. Extrafine inhaled triple therapy versus dual bronchodilator therapy in chronic obstructive pulmonary disease (TRIBUTE): a double-blind, parallel group, randomised controlled trial. Lancet. 2018 Mar 17;391(10125):1076-84.
http://www.ncbi.nlm.nih.gov/pubmed/29429593?tool=bestpractice.com
[85]Lipson DA, Barnacle H, Birk R, et al. FULFIL Trial: once-daily triple therapy for patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2017 Aug 15;196(4):438-46.
https://www.atsjournals.org/doi/full/10.1164/rccm.201703-0449OC
http://www.ncbi.nlm.nih.gov/pubmed/28375647?tool=bestpractice.com
[86]Lipson DA, Barnhart F, Brealey N, et al. Once-daily single-inhaler triple versus dual therapy in patients with COPD. N Engl J Med. 2018 May 3;378(18):1671-80.
https://www.nejm.org/doi/10.1056/NEJMoa1713901
http://www.ncbi.nlm.nih.gov/pubmed/29668352?tool=bestpractice.com
[87]Rojas-Reyes MX, García Morales OM, Dennis RJ, et al. Combination inhaled steroid and long-acting beta₂-agonist in addition to tiotropium versus tiotropium or combination alone for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2016 Jun 6;(6):CD008532.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD008532.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/27271056?tool=bestpractice.com
[88]Lai CC, Chen CH, Lin CYH, et al. The effects of single inhaler triple therapy vs single inhaler dual therapy or separate triple therapy for the management of chronic obstructive pulmonary disease: a systematic review and meta-analysis of randomized controlled trials. Int J Chron Obstruct Pulmon Dis. 2019 Jul 11;14:1539-48. [Erratum in: Int J Chron Obstruct Pulmon Dis. 2020 Jan 21;15:155-6.]
https://www.dovepress.com/the-effects-of-single-inhaler-triple-therapy-vs-single-inhaler-dual-th-peer-reviewed-fulltext-article-COPD
http://www.ncbi.nlm.nih.gov/pubmed/31371939?tool=bestpractice.com
[89]Rabe KF, Martinez FJ, Ferguson GT, et al. Triple inhaled therapy at two glucocorticoid doses in moderate-to-very-severe COPD. N Engl J Med. 2020 Jul 2;383(1):35-48.
http://www.ncbi.nlm.nih.gov/pubmed/32579807?tool=bestpractice.com
ამერიკის თორაკალური საზოგადოების გაიდლაინები რეკომენდაციას უწევენ სამმაგი თერაპიის გამოყენებას პაციენტებთან, რომლებსაც ჰქონდათ ერთი ან მეტი გამწვავება, რომელიც საჭიროებდა ორალურ კორტიკოსტეროიდებს, ანტიბიოტიკებს ან ჰოსპიტალიზაციას გასულ წელს და რომლებსაც აღენიშნებათ ქოშინის სიმპტომები ან ფიზიკური ტოლერანტობის დაქვეითება, მიუხედავად LABA/LAMA ორმაგი თერაპიისა.[90]Nici L, Mammen MJ, Charbek E, et al. Pharmacologic management of chronic obstructive pulmonary disease. An official American Thoracic Society clinical practice guideline. Am J Respir Crit Care Med. 2020 May 1;201(9):e56-69.
https://www.atsjournals.org/doi/10.1164/rccm.202003-0625ST
http://www.ncbi.nlm.nih.gov/pubmed/32283960?tool=bestpractice.com
დიდი ბრიტანეთის გაიდლაინების მიხედვით, სამმაგი თერაპია რეკომენდებულია, თუ მიუხედავად ორმაგი თერაპიისა (კომბინაციური რეჟიმი ხანგრძლივი მოქმედების ბეტა-2 აგონისტებით და მუსკარინული ანტაგონისტებით) აღინიშნება გამწვავება ჰოსპიტალიზაციის საჭიროებით, ან ორი საშუალო სიმძიმის გამწვავება წლის განმავლობაში.[2]National Institute for Health and Care Excellence. Chronic obstructive pulmonary disease in over 16s: diagnosis and management. Jul 2019 [internet publication].
https://www.nice.org.uk/guidance/ng115
თუ პაციენტს უტარდება ორმაგი თერაპია (კომბინაციური რეჟიმი გახანგრძლივებული მოქმედების ბეტა-2 აგონისტებით და მუსკარინული ანტაგონისტებით) და სისხლში ეოზინოფილები <100 უჯრედი/მიკროლიტრზე, საჭიროა როფლუმილასტის ან აზითრომიცინის დამატება.
LABA/ICS არ არის რეკომენდებული GOLD-ის მიერ. თუმცა, თუ COPD-ის მქონე პაციენტს, რომელსაც ასთმის ნიშნები არ აქვს, მიღებული აქვს ეს მკურნალობა და კარგად კონტროლირებადია, მათთან შეიძლება გაგრძელდეს LABA/ICS. თუ პაციენტს აქვს შემდგომი გამწვავებები, ისინი უნდა გადავიდნენ სამმაგ თერაპიაზე LAMA-ს დამატებით. თუ მათ აქვთ საგულისხმო სიმპტომები, პაციენტები შეიძლება გადავიდნენ LABA/LAMA-ზე.
თუ პაციენტს დანიშნული აქვს LABA/LAMA/ICS რეჟიმს შეიძლება დაემატოს როფლუმილასტი ან აზიტრომიცინი. როფლუმილასტი შეიძლება დაინიშნოს პაციენტებთან ფორსირებული ამოსუნთქვის მოცულობით 1 წამში (FEV1) < სავარაუდოს 50%-ით და ქრონიკული ბრონქიტით, განსაკუთრებით იმ შემთხვევაში, თუ მათ ჰქონდათ მინიმუმ ერთი ჰოსპიტალიზაცია გამწვავების გამო ბოლო ერთი წლის განმავლობაში. აზიტრომიცინის დანიშვნისას გასათვალისწინებელია ანტიბიოტიკების მიმართ რეზისტენტობის განვითარების რისკი. საინჰალაციო კორტიკოსტეროიდი შეიძლება შეწყდეს თუ უეფექტოა ან გვერდით მოვლენებს იწვევს. თუ სისხლში ეოზინოფილების რაოდენობა ≥300 უჯრედი/მიკროლიტრზეა, საინჰალაციო კორტიკოსტეროიდის მოხსნის შემდეგ გამწვავების რისკი ყველაზე მაღალია.[75]Chapman KR, Hurst JR, Frent SM, et al. Long-term triple therapy de-escalation to indacaterol/glycopyrronium in patients with chronic obstructive pulmonary disease (SUNSET): a randomized, double-blind, triple-dummy clinical trial. Am J Respir Crit Care Med. 2018 Aug 1;198(3):329-39.
https://www.atsjournals.org/doi/10.1164/rccm.201803-0405OC
http://www.ncbi.nlm.nih.gov/pubmed/29779416?tool=bestpractice.com
ყველ პაციენტს უნდა ჩაუტარდეს სწავლება , ვაქცინაცია და გაეწიოს ყველა სახის დახმარება მოწევის შესაწყვეტად.
[Figure caption and citation for the preceding image starts]: ესკალაციის თერაპია COPD-ის მქონე პაციენტებისთვის. აბრევიატურების განმარტება: ICS: საინჰალაციო კორტიკოსტეროიდები; LABA: ხანგრძლივი მოქმედების ბეტა-2 აგონისტები; LAMA: ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტებიფილტვების ქრონიკული ობსტრუქციული დაავადების გლობალური ინიციატივა (GOLD). ფილტვების ქრონიკული ობსტრუქციული დაავადების დიაგნოსტიკის, მართვისა და პრევენციის გლობალური სტრატეგია (2023 წლის ანგარიში); რგამოყენებულია ნებართვით [Citation ends].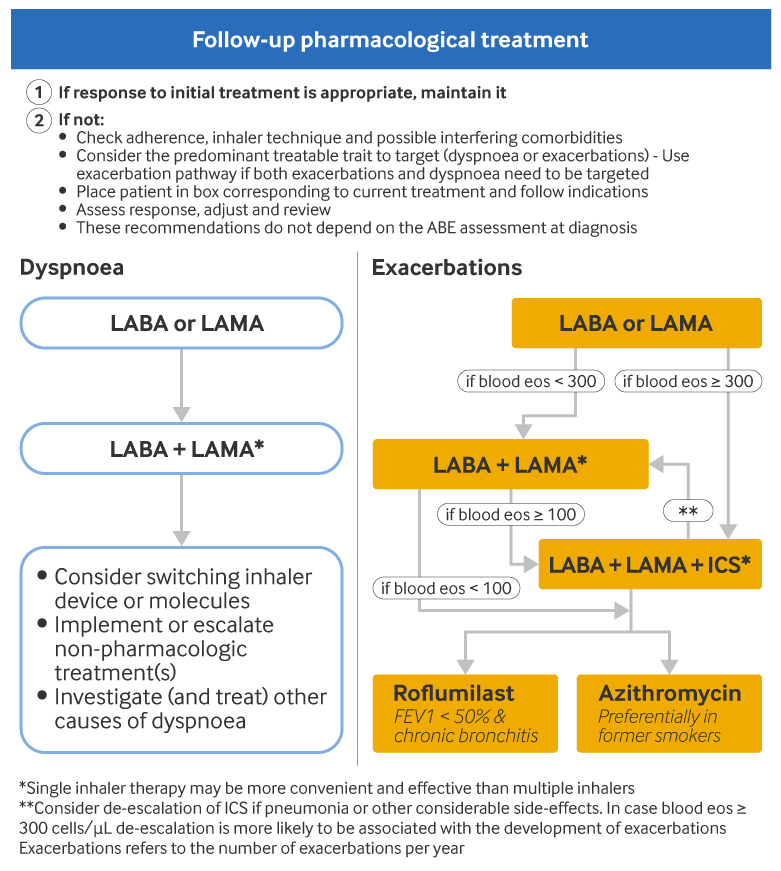
ბრონქოდილატორები
ბეტა აგონისტები ფართოდ გამოიყენება ფქოდ-ის მკურნალობაში. მედიკამენტების ეს კლასი ზრდის უჯრედშიდა cAMP-ის დონეს, რაც იწვევს სასუნთქი გზების გლუვი კუნთების მოდუნებას და რეზისტენტობის შემცირებას. მუსკარინული ანტაგონისტი (ანტიქოლინერგული აგენტი) მოქმედებს გლუვ სასუნთქ კუნთებზე, როგორც ბრონქოდილატატორი, ქოლინერგული რეცეპტორების დაბლოკვით. ეს იწვევს კუნთების მოდუნებასა და ჰაერის ნაკადის დინების შეზღუდვის მოხსნას. ამგვარად, ბეტა აგონისტები და ანტიქოლინერგული საშუალებები მოქმედებენ, როგორც ბრონქოდილატატორები სხვადასხვა მექნიზმით. ხელმისაწვდომია როგორც ხანმოკლე მოქმედების, ასევე ხანგრძლივი მოქმედების პრეპარატები.
ხანმოკლე მოქმედების ბეტა აგონისტები (მაგ. სალბუტამოლი) და ხანმოკლე მოქმედების მუსკარინული ანტაგონისტები (მაგ. იპრატროპიუმი) აუმჯობესებს ფილტვის ფუნქციას, სუნთქვას და სიცოცხლის ხარისხს. იპრატროპიუმს შეიძლება ჰქონდეს მცირე უპირატესობა ხანმოკლე მოქმედების ბეტა-2 აგონისტებთან შედარებით, სიცოცხლის ხარისხის გაუმჯობესების კუთხით.[91]Appleton S, Jones T, Poole P, et al. Ipratropium bromide versus short acting beta-2 agonists for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2006 Apr 19;(2):CD001387.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001387.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/16625543?tool=bestpractice.com
ეს აგენტები შეიძლება გამოიყენოთ "სამაშველო" თერაპიად, როდესაც პაციენტი იმყოფება ხანგრძლივი მოქმედების ბრონქოდილატატორულ თერაპიაზე; ასევე შეიძლება გამოიყენოთ როგორც პირველადი მკურნალობა, GOLD ჯგუფის A პაციენტებში, თუ პაციენტებს მხოლოდ ზოგჯერ აქვთ ხოლმე დისპნოე.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
[92]Chen AM, Bollmeier SG, Finnegan PM, et al. Long-acting bronchodilator therapy for the treatment of chronic obstructive pulmonary disease. Ann Pharmacother. 2008 Dec;42(12):1832-42.
http://www.ncbi.nlm.nih.gov/pubmed/18957624?tool=bestpractice.com
თუმცა, ხანმოკლე მოქმედების ბრონქოდილატატორების რეგულარული გამოყენება ზოგადად არ არის რეკომენდებული.
თიოტროპიუმი (ხანგრძივი მოქმედების მუსკარინული ანტაგონისტი, LAMA) ამცირებს გამწვავების რისკს პლაცებოსთან ან სხვა შემანარჩუნებელ მკურნალობებთან შედარებით.[93]Halpin DM, Vogelmeier C, Pieper MP, et al. Effect of tiotropium on COPD exacerbations: a systematic review. Respir Med. 2016 May;114:1-8.
https://www.resmedjournal.com/article/S0954-6111(16)30030-0/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/27109805?tool=bestpractice.com
[  ]
How does tiotropium compare with ipratropium bromide for people with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.2154/fullShow me the answer უახლეს LAMA-ებს, როგორიცაა აკლიდინიუმი, გლიკოპირონიუმი და უმეკლიდინიუმი, აქვთ სულ მცირე თიოტროპიუმთან შედარებითი ეფექტურობა, FEV1-ის საწყისი მაჩვენებლის ცვლილების, გარდამავალი ქოშინის ინდექსის ქულის, სენტ-ჯორჯის რესპირატორული კითხვარის ქულის და მედიკამენტების გამოყენების კუთხით.[94]Ismaila AS, Huisman EL, Punekar YS, et al. Comparative efficacy of long-acting muscarinic antagonist monotherapies in COPD: a systematic review and network meta-analysis. Int J Chron Obstruct Pulmon Dis. 2015 Nov 16;10(1):2495-517.
https://www.dovepress.com/comparative-efficacy-of-long-acting-muscarinic-antagonist-monotherapie-peer-reviewed-fulltext-article-COPD
http://www.ncbi.nlm.nih.gov/pubmed/26604738?tool=bestpractice.com
რევეფენაცინი არის ნებულიზირებული ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტი, რომელიც დამტკიცებულია საშუალო-მძიმე ფქოდ-ის შემანარჩუნებელ თერაპიად. ზოგიერთი კვლევის მიხედვით, არსებობს მოსაზრება, რომ ხანმოკლე და ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტების ფონზე გულსისხლძარღვთა გართულებებთან დაკავშირებული სიკვდილობა გაზრდილია.[95]Hilleman DE, Malesker MA, Morrow LE, et al. A systematic review of the cardiovascular risk of inhaled anticholinergics in patients with COPD. Int J Chron Obstruct Pulmon Dis. 2009 Jun 29;4:253-63.
https://www.dovepress.com/getfile.php?fileID=5012
http://www.ncbi.nlm.nih.gov/pubmed/19657399?tool=bestpractice.com
[96]Wang MT, Liou JT, Lin CW, et al. Association of cardiovascular risk with inhaled long-acting bronchodilators in patients with chronic obstructive pulmonary disease: a nested case-control study. JAMA Intern Med. 2018 Feb 1;178(2):229-38.
https://jamanetwork.com/journals/jamainternalmedicine/fullarticle/2666790
http://www.ncbi.nlm.nih.gov/pubmed/29297057?tool=bestpractice.com
ერთმა კვლევამ დაასკვნა, რომ აკლიდინიუმი ძირითად გულ-სისხლძარღვთა გვერდით მოვლენების მზარდ გამოვლენასთან არ ასოცირდება, პლაცებოსთან შედარებით.[97]Wise RA, Chapman KR, Scirica BM, et al. Effect of aclidinium bromide on major cardiovascular events and exacerbations in high-risk patients with chronic obstructive pulmonary disease: the ASCENT-COPD randomized clinical trial. JAMA. 2019 May 7;321(17):1693-701.
https://jamanetwork.com/journals/jama/fullarticle/2732574
http://www.ncbi.nlm.nih.gov/pubmed/31063575?tool=bestpractice.com
პოპულაციური-კოჰორტული კვლევის თანახმად, ფქოდ-ის მქონე ხანდაზმულ მამაკაცებში ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტების დაწყების შემთხვევაში იმატებს საშარდე ტრაქტის ინფექციების რისკი.[98]Gershon AS, Newman AM, Fischer HD, et al. Inhaled long-acting anticholinergics and urinary tract infection in individuals with COPD. COPD. 2017 Feb;14(1):105-12.
http://www.ncbi.nlm.nih.gov/pubmed/27732117?tool=bestpractice.com
]
How does tiotropium compare with ipratropium bromide for people with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.2154/fullShow me the answer უახლეს LAMA-ებს, როგორიცაა აკლიდინიუმი, გლიკოპირონიუმი და უმეკლიდინიუმი, აქვთ სულ მცირე თიოტროპიუმთან შედარებითი ეფექტურობა, FEV1-ის საწყისი მაჩვენებლის ცვლილების, გარდამავალი ქოშინის ინდექსის ქულის, სენტ-ჯორჯის რესპირატორული კითხვარის ქულის და მედიკამენტების გამოყენების კუთხით.[94]Ismaila AS, Huisman EL, Punekar YS, et al. Comparative efficacy of long-acting muscarinic antagonist monotherapies in COPD: a systematic review and network meta-analysis. Int J Chron Obstruct Pulmon Dis. 2015 Nov 16;10(1):2495-517.
https://www.dovepress.com/comparative-efficacy-of-long-acting-muscarinic-antagonist-monotherapie-peer-reviewed-fulltext-article-COPD
http://www.ncbi.nlm.nih.gov/pubmed/26604738?tool=bestpractice.com
რევეფენაცინი არის ნებულიზირებული ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტი, რომელიც დამტკიცებულია საშუალო-მძიმე ფქოდ-ის შემანარჩუნებელ თერაპიად. ზოგიერთი კვლევის მიხედვით, არსებობს მოსაზრება, რომ ხანმოკლე და ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტების ფონზე გულსისხლძარღვთა გართულებებთან დაკავშირებული სიკვდილობა გაზრდილია.[95]Hilleman DE, Malesker MA, Morrow LE, et al. A systematic review of the cardiovascular risk of inhaled anticholinergics in patients with COPD. Int J Chron Obstruct Pulmon Dis. 2009 Jun 29;4:253-63.
https://www.dovepress.com/getfile.php?fileID=5012
http://www.ncbi.nlm.nih.gov/pubmed/19657399?tool=bestpractice.com
[96]Wang MT, Liou JT, Lin CW, et al. Association of cardiovascular risk with inhaled long-acting bronchodilators in patients with chronic obstructive pulmonary disease: a nested case-control study. JAMA Intern Med. 2018 Feb 1;178(2):229-38.
https://jamanetwork.com/journals/jamainternalmedicine/fullarticle/2666790
http://www.ncbi.nlm.nih.gov/pubmed/29297057?tool=bestpractice.com
ერთმა კვლევამ დაასკვნა, რომ აკლიდინიუმი ძირითად გულ-სისხლძარღვთა გვერდით მოვლენების მზარდ გამოვლენასთან არ ასოცირდება, პლაცებოსთან შედარებით.[97]Wise RA, Chapman KR, Scirica BM, et al. Effect of aclidinium bromide on major cardiovascular events and exacerbations in high-risk patients with chronic obstructive pulmonary disease: the ASCENT-COPD randomized clinical trial. JAMA. 2019 May 7;321(17):1693-701.
https://jamanetwork.com/journals/jama/fullarticle/2732574
http://www.ncbi.nlm.nih.gov/pubmed/31063575?tool=bestpractice.com
პოპულაციური-კოჰორტული კვლევის თანახმად, ფქოდ-ის მქონე ხანდაზმულ მამაკაცებში ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტების დაწყების შემთხვევაში იმატებს საშარდე ტრაქტის ინფექციების რისკი.[98]Gershon AS, Newman AM, Fischer HD, et al. Inhaled long-acting anticholinergics and urinary tract infection in individuals with COPD. COPD. 2017 Feb;14(1):105-12.
http://www.ncbi.nlm.nih.gov/pubmed/27732117?tool=bestpractice.com
ხანგრძლივი მოქმედების ბეტა-2 აგონისტები და ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტები მნიშვნელოვნად აუმჯობესებს ფილტვის ფუნქციას, დისპნოეს და ჯანმრთელობის სტატუსს, ამცირებს გამწვავებების სიხშირეს.
[  ]
How does umeclidinium bromide compare with placebo for people with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1829/fullShow me the answer[Evidence A]81c5e462-8f36-4687-93b0-cd4b9989ab2accaAროგორ შედარდა უმეკლიდინიუმი პლაცებოს ფილტვების ქრონიკული ობსტრუქციული დაავადების (COPD) მქონე ადამიანებთან? სტაბილური COPD-ის შემთხვევაში, თუ მონოთერაპიის შესახებ გადაწყვეტილების მიღებაა საჭირო, უპირატესობა LAMA-ს უნდა მიენიჭოს LABA აგენტებთან შედარებით.[99]Rabe KF, Timmer W, Sagkriotis A, et al. Comparison of a combination of tiotropium plus formoterol to salmeterol plus fluticasone in moderate COPD. Chest. 2008 Aug;134(2):255-62.
http://www.ncbi.nlm.nih.gov/pubmed/18403672?tool=bestpractice.com
ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტები უფრო მეტად ამსუბუქებს გამწვავებებს საშუალო-მძიმე ფქოდ-ის დროს, ვიდრე ხანგრძლივი მოქმედების ბეტა-2 აგონისტები.[100]Vogelmeier C, Hederer B, Glaab T, et al; POET-COPD Investigators. Tiotropium versus salmeterol for the prevention of exacerbations of COPD. N Engl J Med. 2011 Mar 24;364(12):1093-103.
https://www.nejm.org/doi/full/10.1056/NEJMoa1008378
http://www.ncbi.nlm.nih.gov/pubmed/21428765?tool=bestpractice.com
[101]Decramer ML, Chapman KR, Dahl R, et al; INVIGORATE investigators. Once-daily indacaterol versus tiotropium for patients with severe chronic obstructive pulmonary disease (INVIGORATE): a randomised, blinded, parallel-group study. Lancet Respir Med. 2013 Sep;1(7):524-33.
http://www.ncbi.nlm.nih.gov/pubmed/24461613?tool=bestpractice.com
LAMA-ს გრძელვადიანი უსაფრთხოება გამოვლინდა UPLIFT კვლევაში.[102]Celli B, Decramer M, Kesten S, et al. UPLIFT Study Investigators. Mortality in the 4-year trial of tiotropium (UPLIFT) in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2009 Nov 15;180(10):948-55.
https://www.atsjournals.org/doi/full/10.1164/rccm.200906-0876OC
http://www.ncbi.nlm.nih.gov/pubmed/19729663?tool=bestpractice.com
]
How does umeclidinium bromide compare with placebo for people with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1829/fullShow me the answer[Evidence A]81c5e462-8f36-4687-93b0-cd4b9989ab2accaAროგორ შედარდა უმეკლიდინიუმი პლაცებოს ფილტვების ქრონიკული ობსტრუქციული დაავადების (COPD) მქონე ადამიანებთან? სტაბილური COPD-ის შემთხვევაში, თუ მონოთერაპიის შესახებ გადაწყვეტილების მიღებაა საჭირო, უპირატესობა LAMA-ს უნდა მიენიჭოს LABA აგენტებთან შედარებით.[99]Rabe KF, Timmer W, Sagkriotis A, et al. Comparison of a combination of tiotropium plus formoterol to salmeterol plus fluticasone in moderate COPD. Chest. 2008 Aug;134(2):255-62.
http://www.ncbi.nlm.nih.gov/pubmed/18403672?tool=bestpractice.com
ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტები უფრო მეტად ამსუბუქებს გამწვავებებს საშუალო-მძიმე ფქოდ-ის დროს, ვიდრე ხანგრძლივი მოქმედების ბეტა-2 აგონისტები.[100]Vogelmeier C, Hederer B, Glaab T, et al; POET-COPD Investigators. Tiotropium versus salmeterol for the prevention of exacerbations of COPD. N Engl J Med. 2011 Mar 24;364(12):1093-103.
https://www.nejm.org/doi/full/10.1056/NEJMoa1008378
http://www.ncbi.nlm.nih.gov/pubmed/21428765?tool=bestpractice.com
[101]Decramer ML, Chapman KR, Dahl R, et al; INVIGORATE investigators. Once-daily indacaterol versus tiotropium for patients with severe chronic obstructive pulmonary disease (INVIGORATE): a randomised, blinded, parallel-group study. Lancet Respir Med. 2013 Sep;1(7):524-33.
http://www.ncbi.nlm.nih.gov/pubmed/24461613?tool=bestpractice.com
LAMA-ს გრძელვადიანი უსაფრთხოება გამოვლინდა UPLIFT კვლევაში.[102]Celli B, Decramer M, Kesten S, et al. UPLIFT Study Investigators. Mortality in the 4-year trial of tiotropium (UPLIFT) in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2009 Nov 15;180(10):948-55.
https://www.atsjournals.org/doi/full/10.1164/rccm.200906-0876OC
http://www.ncbi.nlm.nih.gov/pubmed/19729663?tool=bestpractice.com
ხანგრძლივი მოქმედების ბეტა-2 აგონისტების და მუსკარინული ანტაგონისტების კომბინაციამ შეიძლება უკეთესი თერაპიული ეფექტი მოგვცეს, ცალკეული კლასისთვის დამახასიათებელი გვერდითი მოვლენების მატების გარეშე.[99]Rabe KF, Timmer W, Sagkriotis A, et al. Comparison of a combination of tiotropium plus formoterol to salmeterol plus fluticasone in moderate COPD. Chest. 2008 Aug;134(2):255-62.
http://www.ncbi.nlm.nih.gov/pubmed/18403672?tool=bestpractice.com
[103]Tashkin DP, Littner M, Andrews CP, et al. Concomitant treatment with nebulized formoterol and tiotropium in subjects with COPD: a placebo-controlled trial. Respir Med. 2008 Apr;102(4):479-87.
http://www.ncbi.nlm.nih.gov/pubmed/18258423?tool=bestpractice.com
[104]Tashkin DP, Pearle J, Iezzoni D, et al. Formoterol and tiotropium compared with tiotropium alone for treatment of COPD. COPD. 2009 Feb;6(1):17-25.
http://www.ncbi.nlm.nih.gov/pubmed/19229704?tool=bestpractice.com
[105]Vogelmeier C, Kardos P, Harari S, et al. Formoterol mono- and combination therapy with tiotropium in patients with COPD: a 6-month study. Respir Med. 2008 Nov;102(11):1511-20.
http://www.ncbi.nlm.nih.gov/pubmed/18804362?tool=bestpractice.com
[106]Maltais F, Bjermer L, Kerwin EM, et al. Efficacy of umeclidinium/vilanterol versus umeclidinium and salmeterol monotherapies in symptomatic patients with COPD not receiving inhaled corticosteroids: the EMAX randomised trial. Respir Res. 2019 Oct 30;20(1):238.
https://respiratory-research.biomedcentral.com/articles/10.1186/s12931-019-1193-9
http://www.ncbi.nlm.nih.gov/pubmed/31666084?tool=bestpractice.com
უმეკლიდინიუმი/ვილანტეროლი, გლიკოპირონიუმი/ფორმოტეროლი, ტიოტროპიუმი/ოლოდატეროლი და აკლიდინიუმი/ფორმოტეროლი დამტკიცებულია COPD-ის სამკურნალოდ. სისტემურმა მიმოხილვებით და მეტა-ანალიზით გამოვლინდა, რომ LABA/LAMA-ით კომბინირებული თერაპია:
ამცირებს გამწვავების სიხშირეს მონოთერაპიასთან შედარებით
ასოცირდება კლინიკურად ფილტვის ფუნქციის და ჯანმრთელობასთან დაკავშირებული ცხოვრების ხარისხის მნიშვნელოვან გაუმჯობესებასთან მსუბუქი/ზომიერი COPD-ის მქონე პაციენტებთან პლაცებოსთან შედარებით[107]Maqsood U, Ho TN, Palmer K, et al. Once daily long-acting beta2-agonists and long-acting muscarinic antagonists in a combined inhaler versus placebo for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2019 Mar 6;(3):CD012930.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD012930.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/30839102?tool=bestpractice.com
[  ]
How does a combined inhaler with once‐daily long‐acting beta2‐agonist (LABA) plus a long‐acting muscarinic antagonist (LAMA) compare with placebo for adults with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2551/fullShow me the answer
]
How does a combined inhaler with once‐daily long‐acting beta2‐agonist (LABA) plus a long‐acting muscarinic antagonist (LAMA) compare with placebo for adults with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2551/fullShow me the answer
ზრდის FEV1-ს და მცირედით ამცირებს პნევმონიის რისკს სტაბილური ფქოდის მქონე პაციენტებთან, მაგრამ ზრდის ყველა მიზეზით სიკვდილის შანსებს 1%-დან 1.4%-მდე.[108]Fukuda N, Horita N, Kaneko A, et al. Long-acting muscarinic antagonist (LAMA) plus long-acting beta-agonist (LABA) versus LABA plus inhaled corticosteroid (ICS) for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2023 Jun 5;6(6):CD012066.
https://www.doi.org/10.1002/14651858.CD012066.pub3
http://www.ncbi.nlm.nih.gov/pubmed/37276335?tool=bestpractice.com
[  ]
How does long‐acting muscarinic antagonist (LAMA) plus long‐acting beta‐agonist (LABA) compare with LABA plus inhaled corticosteroid (ICS) for people with stable chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4356/fullShow me the answer
]
How does long‐acting muscarinic antagonist (LAMA) plus long‐acting beta‐agonist (LABA) compare with LABA plus inhaled corticosteroid (ICS) for people with stable chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4356/fullShow me the answer
უმეკლიდინიუმი/ვილანტეროლი აქვეითებს გამწვავებების რისკს ფქოდ-ის მსუბუქი/საშუალო ფორმების დროს.[107]Maqsood U, Ho TN, Palmer K, et al. Once daily long-acting beta2-agonists and long-acting muscarinic antagonists in a combined inhaler versus placebo for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2019 Mar 6;(3):CD012930.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD012930.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/30839102?tool=bestpractice.com
[  ]
How does a combined inhaler with once‐daily long‐acting beta2‐agonist (LABA) plus a long‐acting muscarinic antagonist (LAMA) compare with placebo for adults with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2551/fullShow me the answer ერთმა სისტემატურმა მიმოხილვამ და ქსელის მეტა-ანალიზმა აჩვენა, რომ ყველა LABA/LAMA ფიქსირებული დოზის კომბინაციას მსგავსი ეფექტურობა და უსაფრთხოება ჰქონდა.[109]Schlueter M, Gonzalez-Rojas N, Baldwin M, et al. Comparative efficacy of fixed-dose combinations of long-acting muscarinic antagonists and long-acting beta2-agonists: a systematic review and network meta-analysis. Ther Adv Respir Dis. 2016 Apr;10(2):89-104.
https://journals.sagepub.com/doi/10.1177/1753465815624612
http://www.ncbi.nlm.nih.gov/pubmed/26746383?tool=bestpractice.com
]
How does a combined inhaler with once‐daily long‐acting beta2‐agonist (LABA) plus a long‐acting muscarinic antagonist (LAMA) compare with placebo for adults with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2551/fullShow me the answer ერთმა სისტემატურმა მიმოხილვამ და ქსელის მეტა-ანალიზმა აჩვენა, რომ ყველა LABA/LAMA ფიქსირებული დოზის კომბინაციას მსგავსი ეფექტურობა და უსაფრთხოება ჰქონდა.[109]Schlueter M, Gonzalez-Rojas N, Baldwin M, et al. Comparative efficacy of fixed-dose combinations of long-acting muscarinic antagonists and long-acting beta2-agonists: a systematic review and network meta-analysis. Ther Adv Respir Dis. 2016 Apr;10(2):89-104.
https://journals.sagepub.com/doi/10.1177/1753465815624612
http://www.ncbi.nlm.nih.gov/pubmed/26746383?tool=bestpractice.com
როგორც ზემოთ აღინიშნა, GOLD საწყისი მედიკამენტის შერჩევის რეკომენდაციას პაციენტის რისკის ჯგუფის (A, B, ან E) მიხედვით იძლევა.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
ფქოდის დროს, როდესაც პაციენტს აღენიშნება დისპნოე ან ფიზიკური დატვირთვის აუტანლობა, ამერიკის თორაკალური საზოგადოების გაიდლაინები რეკომენდაციას უწევს ხანგრძლივი მოქმედების ბეტა-2 აგონისტი/ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტებით ორმაგ თერაპიას და უპირატესობას ანიჭებს მას მონოთერაპიასთან შედარებით.[90]Nici L, Mammen MJ, Charbek E, et al. Pharmacologic management of chronic obstructive pulmonary disease. An official American Thoracic Society clinical practice guideline. Am J Respir Crit Care Med. 2020 May 1;201(9):e56-69.
https://www.atsjournals.org/doi/10.1164/rccm.202003-0625ST
http://www.ncbi.nlm.nih.gov/pubmed/32283960?tool=bestpractice.com
დიდი ბრიტანეთის გაიდლაინებში რეკომენდებულია ხანგრძლივი მოქმედების ბეტა-2 აგონისტი/ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტით ან ხანგრძლივი მოქმედების ბეტა-2 აგონისტი/ინჰალაციური კორტიკოსოსტეროიდების ორმაგი თერაპია, თუ პაციენტს აღენიშნება გამწვავება, არაფარმაკოლოგიური მკურნალობის მიუხედავად და ასევე, რეკომენდებულია ხანმოკლე მოქმედების ბრონქოდილატატორის გამოყენება საჭიროებისამებრ. დიდი ბრიტანეთის გაიდლაინების მიხედვით, მკურნალობის საწყისი რეჟიმის არჩევანი დამოკიდებულია იმაზე, აქვს თუ არა პაციენტს ბრონქული ასთმის მახასიათებლები ან კორტიკოსტეროიდებზე რეაგირების ნიშნები.[2]National Institute for Health and Care Excellence. Chronic obstructive pulmonary disease in over 16s: diagnosis and management. Jul 2019 [internet publication].
https://www.nice.org.uk/guidance/ng115
საინჰალაციო კორტიკოსტეროიდები (ICS)
ჩვენების შემთხვევაში ფქოდის მქონე პაციენტთან, ICS ყოველთვის ხანგრძლივი მოქმედების ბრონქოდილატატორთან კომბინაციაში უნდა დაინიშნოს. ითვლება, რომ ICS ეფექტურია მათი ანთების საწინააღმდეგო ეფექტის გამო. ICS-ის გრძელვადიანი გამოყენება ამცირებს სათადარიგო თერაპიის გამოყენების აუცილებლობას და ამცირებს გამწვავებებს, ასევე შეიძლება შეამციროს სიკვდილიანობა.[110]Spencer S, Calverley PM, Burge PS, et al. Impact of preventing exacerbations on deterioration of health status in COPD. Eur Respir J. 2004 May;23(5):698-702.
https://erj.ersjournals.com/content/23/5/698
http://www.ncbi.nlm.nih.gov/pubmed/15176682?tool=bestpractice.com
[111]Sin DD, Wu L, Anderson JA, et al. Inhaled corticosteroids and mortality in chronic obstructive pulmonary disease. Thorax. 2005 Dec;60(12):992-7.
http://www.ncbi.nlm.nih.gov/pubmed/16227327?tool=bestpractice.com
[112]Lee HW, Park J, Jo J, et al. Comparisons of exacerbations and mortality among regular inhaled therapies for patients with stable chronic obstructive pulmonary disease: systematic review and Bayesian network meta-analysis. PLoS Med. 2019 Nov;16(11):e1002958.
https://journals.plos.org/plosmedicine/article?id=10.1371/journal.pmed.1002958
http://www.ncbi.nlm.nih.gov/pubmed/31730642?tool=bestpractice.com
საინჰალაციო კორტიკოსტეროიდების შემცველი სამკურნალორ რეჟიმები უფრო ეფექტურია გამწვავებების მაღალი რისკის მქონე პაციენტებში (უკანასკნელ წელიწადში ორი ან მეტი გამწვავება და/ან გამწვავების მიზეზით ჰოსპიტალიზაციის ერთი შემთხვევა).[84]Papi A, Vestbo J, Fabbri L, et al. Extrafine inhaled triple therapy versus dual bronchodilator therapy in chronic obstructive pulmonary disease (TRIBUTE): a double-blind, parallel group, randomised controlled trial. Lancet. 2018 Mar 17;391(10125):1076-84.
http://www.ncbi.nlm.nih.gov/pubmed/29429593?tool=bestpractice.com
[86]Lipson DA, Barnhart F, Brealey N, et al. Once-daily single-inhaler triple versus dual therapy in patients with COPD. N Engl J Med. 2018 May 3;378(18):1671-80.
https://www.nejm.org/doi/10.1056/NEJMoa1713901
http://www.ncbi.nlm.nih.gov/pubmed/29668352?tool=bestpractice.com
[113]Wedzicha JA, Banerji D, Chapman KR, et al; FLAME Investigators. Indacaterol-glycopyrronium versus salmeterol-fluticasone for COPD. N Engl J Med. 2016 Jun 9;374(23):2222-34.
https://www.nejm.org/doi/10.1056/NEJMoa1516385
http://www.ncbi.nlm.nih.gov/pubmed/27181606?tool=bestpractice.com
სისხლში ეოზინოფილების რაოდენობით წინასწარ შეიძლება განისაზღვროს ICS-ის დამატების ეფექტურობა რეგულარულ ხანგრძლივი მოქმედების ბრონქოდილატატორულ მკურნალობაზე გამწვავებების თავიდან ასაცილებლად.[71]Harries TH, Rowland V, Corrigan CJ, et al. Blood eosinophil count, a marker of inhaled corticosteroid effectiveness in preventing COPD exacerbations in post-hoc RCT and observational studies: systematic review and meta-analysis. Respir Res. 2020 Jan 3;21(1):3.
https://respiratory-research.biomedcentral.com/articles/10.1186/s12931-019-1268-7
http://www.ncbi.nlm.nih.gov/pubmed/31900184?tool=bestpractice.com
[72]Oshagbemi OA, Odiba JO, Daniel A, et al. Absolute blood eosinophil counts to guide inhaled corticosteroids therapy among patients with COPD: systematic review and meta-analysis. Curr Drug Targets. 2019;20(16):1670-9.
http://www.ncbi.nlm.nih.gov/pubmed/31393244?tool=bestpractice.com
[73]Pascoe S, Barnes N, Brusselle G, et al. Blood eosinophils and treatment response with triple and dual combination therapy in chronic obstructive pulmonary disease: analysis of the IMPACT trial. Lancet Respir Med. 2019 Sep;7(9):745-56.
http://www.ncbi.nlm.nih.gov/pubmed/31281061?tool=bestpractice.com
მცირეა ან საერთოდ არ არის ეფექტი როცა სისხლში ეოზინოფილების რაოდენობა 100 უჯრედი/მიკროლიტრია, მაშინ როცა მაქსიმალური ეფექტი აღინიშნება სისხლში ეოზინოფილების რაოდენობაზე ≥300 უჯრედი/მიკროლიტრზე.[70]Bafadhel M, Peterson S, De Blas MA, et al. Predictors of exacerbation risk and response to budesonide in patients with chronic obstructive pulmonary disease: a post-hoc analysis of three randomised trials. Lancet Respir Med. 2018 Feb;6(2):117-26.
http://www.ncbi.nlm.nih.gov/pubmed/29331313?tool=bestpractice.com
[74]Cazzola M, Rogliani P, Calzetta L, et al. Triple therapy versus single and dual long-acting bronchodilator therapy in COPD: a systematic review and meta-analysis. Eur Respir J. 2018 Dec 13;52(6):1801586.
https://erj.ersjournals.com/content/52/6/1801586
http://www.ncbi.nlm.nih.gov/pubmed/30309975?tool=bestpractice.com
ეს სავარაუდო ზღვრული მაჩვენებლებია, რომლებიც შეიძლება დაეხმარონ კლინიცისტებს წინასწარ განსაზღვრონ ICS მკურნალობის სარგებლის ალბათობა.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
ეოზინოფილების ნებისმიერი რაოდენობის შემთხვევაში, ყოფილი მწეველები მეტად რეაგირებენ კორტიკოსტეროიდებზე, ვიდრე აქტიური მწეველები.[73]Pascoe S, Barnes N, Brusselle G, et al. Blood eosinophils and treatment response with triple and dual combination therapy in chronic obstructive pulmonary disease: analysis of the IMPACT trial. Lancet Respir Med. 2019 Sep;7(9):745-56.
http://www.ncbi.nlm.nih.gov/pubmed/31281061?tool=bestpractice.com
ფქოდ-ის დროს, როგორც აქტიური, ასევე ყოფილი მწეველებისთვის შეიძლება აღმოჩნდეს სასარგებლო ინჰალაციური კორტიკოსტეროიდები ფილტვის ფუნქციის გაუმჯობესებისა და გამწვავებების სიხშირის შემცირების თვალსაზრისით, თუმცა ნაკლებეფექტურია აქტიური მწეველებისთვის ყოფილ მწეველებთან შედარებით.[86]Lipson DA, Barnhart F, Brealey N, et al. Once-daily single-inhaler triple versus dual therapy in patients with COPD. N Engl J Med. 2018 May 3;378(18):1671-80.
https://www.nejm.org/doi/10.1056/NEJMoa1713901
http://www.ncbi.nlm.nih.gov/pubmed/29668352?tool=bestpractice.com
[114]Sonnex K, Alleemudder H, Knaggs R. Impact of smoking status on the efficacy of inhaled corticosteroids in chronic obstructive pulmonary disease: a systematic review. BMJ Open. 2020 Apr 15;10(4):e037509.
https://bmjopen.bmj.com/content/10/4/e037509
http://www.ncbi.nlm.nih.gov/pubmed/32300001?tool=bestpractice.com
ICS-ის მოკლევადიანი გამოყენება (≤1 წელი) შეიძლება დაკავშირებული იყოს FEV1-ის უფრო დიდ გაუმჯობესებასთან, ვიდრე გრძელვადიანი გამოყენება, თუმცა საჭიროა შემდგომი კვლევები ფილტვების ფუნქციაზე მკურნალობის ეფექტის უკეთ გასაგებად.[115]Whittaker HR, Jarvis D, Sheikh MR, et al. Inhaled corticosteroids and FEV1 decline in chronic obstructive pulmonary disease: a systematic review. Respir Res. 2019 Dec 4;20(1):277.
https://respiratory-research.biomedcentral.com/articles/10.1186/s12931-019-1249-x
http://www.ncbi.nlm.nih.gov/pubmed/31801539?tool=bestpractice.com
რამდენიმე კვლევა მიანიშნებს პნევმონიის გაზრდილ რისკზე COPD-ის მქონე პაციენტებში, რომლებიც იღებენ ICS.[79]Yang IA, Ferry OR, Clarke MS, et al. Inhaled corticosteroids versus placebo for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2023 Mar 27;(3):CD002991.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD002991.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/36971693?tool=bestpractice.com
[  ]
What are the benefits and harms of inhaled corticosteroids (ICS) in people with stable chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4293/fullShow me the answer ეს რისკი უფრო მაღალია ფლუტიკაზონისთვის ბუდესონიდთან შედარებით.[116]Suissa S, Patenaude V, Lapi F, et al. Inhaled corticosteroids in COPD and the risk of serious pneumonia. Thorax. 2013 Nov;68(11):1029-36.
https://thorax.bmj.com/content/68/11/1029.long
http://www.ncbi.nlm.nih.gov/pubmed/24130228?tool=bestpractice.com
[117]Lodise TP, Li J, Gandhi HN, et al. Intraclass difference in pneumonia risk with fluticasone and budesonide in COPD: a systematic review of evidence from direct-comparison studies. Int J Chron Obstruct Pulmon Dis. 2020 Nov 11;15:2889-900.
https://www.dovepress.com/intraclass-difference-in-pneumonia-risk-with-fluticasone-and-budesonid-peer-reviewed-fulltext-article-COPD
http://www.ncbi.nlm.nih.gov/pubmed/33204085?tool=bestpractice.com
[118]Yang M, Du Y, Chen H, et al. Inhaled corticosteroids and risk of pneumonia in patients with chronic obstructive pulmonary disease: a meta-analysis of randomized controlled trials. Int Immunopharmacol. 2019 Dec;77:105950.
http://www.ncbi.nlm.nih.gov/pubmed/31629940?tool=bestpractice.com
დანიელ პაციენტთა დიდ ჯგუფში ჩატარებულმა კვლევამ აჩვენა, რომ Pseudomonas aeruginosa-ს, ჰოსპიტალური პნევმონიის ხშირი გამომწვევის, შეძენის რისკი დამოკიდებულია დოზაზე, და ყველაზე მაღალი რისკი ICS-ის მაღალ დოზასთან ასოცირდება. კვლევამ ასევე აჩვენა, რომ P aeruginosa-ს მქონე პაციენტებს უფრო დაბალი BMI და FEV1 აქვთ ვიდრე P aeruginosa-ს არმქონე პაციენტებს.[119]Eklöf J, Ingebrigtsen TS, Sørensen R, et al. Use of inhaled corticosteroids and risk of acquiring Pseudomonas aeruginosa in patients with chronic obstructive pulmonary disease. Thorax. 2022 Jun;77(6):573-80.
https://thorax.bmj.com/content/77/6/573
http://www.ncbi.nlm.nih.gov/pubmed/34446524?tool=bestpractice.com
ერთმა სისტემურმა მიმოხილვამ და მეტა-ანალიზმა აჩვენა, რომ, მიუხედავად ICS-ისთან ასოცირებული პნევმონიის დაუკორექტირებელი რისკის მნიშვნელოვანი ზრდისა, პნევმონიით სიკვდილიანობა და საერთო სიკვდილიანობა არ გაიზარდა რანდომიზებულ კონტროლირებად კვლევებში და შემცირდა ობსერვაციულ კვლევებში.[120]Festic E, Bansal V, Gupta E, et al. Association of inhaled corticosteroids with incident pneumonia and mortality in COPD patients; systematic review and meta-analysis. COPD. 2016 Jun;13(3):312-26.
https://www.tandfonline.com/doi/full/10.3109/15412555.2015.1081162
http://www.ncbi.nlm.nih.gov/pubmed/26645797?tool=bestpractice.com
ამგვარად, საჭიროა მკურნალობის დანიშვნის დროს ინდივიდუალური მიდგომა, რომლის მიხედვითაც შეფასდება პნევმონიის რისკს მკურნალობის სარგებლთან, გამწვავებების შემცირებასთან, შედარებით.[79]Yang IA, Ferry OR, Clarke MS, et al. Inhaled corticosteroids versus placebo for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2023 Mar 27;(3):CD002991.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD002991.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/36971693?tool=bestpractice.com
[121]Welte T. Inhaled corticosteroids in COPD and the risk of pneumonia. Lancet. 2009 Aug 29;374(9691):668-70.
http://www.ncbi.nlm.nih.gov/pubmed/19716946?tool=bestpractice.com
[122]Kew KM, Seniukovich A. Inhaled steroids and risk of pneumonia for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2014 Mar 10;(3):CD010115.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD010115.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/24615270?tool=bestpractice.com
ასევე შემაშფოთებელია ტუბერკულოზისა და გრიპის განვითარების გაზრდილი რისკი COPD-ით დაავადებულ მოზრდილ პაციენტებთან, რომლებიც ICS თერაპიაზე იმყოფებიან, თუმცა ერთმა მეტა-ანალიზმა აჩვენა, რომ ყველა შეფასებული ტუბერკულოზის შემთხვევის 1%-ზე ნაკლები უკავშირდებოდა ICS-ის ექსპოზიციას.[123]Dong YH, Chang CH, Lin Wu FL, et al. Use of inhaled corticosteroids in patients with COPD and the risk of TB and influenza: a systematic review and meta-analysis of randomized controlled trials. Chest. 2014 Jun;145(6):1286-97.
http://www.ncbi.nlm.nih.gov/pubmed/24504044?tool=bestpractice.com
[124]Castellana G, Castellana M, Castellana C, et al. Inhaled corticosteroids and risk of tuberculosis in patients with obstructive lung diseases: a systematic review and meta-analysis of non-randomized studies. Int J Chron Obstruct Pulmon Dis. 2019 Sep 26;14:2219-27.
https://www.dovepress.com/inhaled-corticosteroids-and-risk-of-tuberculosis-in-patients-with-obst-peer-reviewed-fulltext-article-COPD
http://www.ncbi.nlm.nih.gov/pubmed/31576118?tool=bestpractice.com
ICS-მ ასევე შეიძლება გამოიწვიოს ოროფარინგიალური კანდიდოზი და დისფონია.[79]Yang IA, Ferry OR, Clarke MS, et al. Inhaled corticosteroids versus placebo for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2023 Mar 27;(3):CD002991.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD002991.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/36971693?tool=bestpractice.com
[
]
What are the benefits and harms of inhaled corticosteroids (ICS) in people with stable chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4293/fullShow me the answer ეს რისკი უფრო მაღალია ფლუტიკაზონისთვის ბუდესონიდთან შედარებით.[116]Suissa S, Patenaude V, Lapi F, et al. Inhaled corticosteroids in COPD and the risk of serious pneumonia. Thorax. 2013 Nov;68(11):1029-36.
https://thorax.bmj.com/content/68/11/1029.long
http://www.ncbi.nlm.nih.gov/pubmed/24130228?tool=bestpractice.com
[117]Lodise TP, Li J, Gandhi HN, et al. Intraclass difference in pneumonia risk with fluticasone and budesonide in COPD: a systematic review of evidence from direct-comparison studies. Int J Chron Obstruct Pulmon Dis. 2020 Nov 11;15:2889-900.
https://www.dovepress.com/intraclass-difference-in-pneumonia-risk-with-fluticasone-and-budesonid-peer-reviewed-fulltext-article-COPD
http://www.ncbi.nlm.nih.gov/pubmed/33204085?tool=bestpractice.com
[118]Yang M, Du Y, Chen H, et al. Inhaled corticosteroids and risk of pneumonia in patients with chronic obstructive pulmonary disease: a meta-analysis of randomized controlled trials. Int Immunopharmacol. 2019 Dec;77:105950.
http://www.ncbi.nlm.nih.gov/pubmed/31629940?tool=bestpractice.com
დანიელ პაციენტთა დიდ ჯგუფში ჩატარებულმა კვლევამ აჩვენა, რომ Pseudomonas aeruginosa-ს, ჰოსპიტალური პნევმონიის ხშირი გამომწვევის, შეძენის რისკი დამოკიდებულია დოზაზე, და ყველაზე მაღალი რისკი ICS-ის მაღალ დოზასთან ასოცირდება. კვლევამ ასევე აჩვენა, რომ P aeruginosa-ს მქონე პაციენტებს უფრო დაბალი BMI და FEV1 აქვთ ვიდრე P aeruginosa-ს არმქონე პაციენტებს.[119]Eklöf J, Ingebrigtsen TS, Sørensen R, et al. Use of inhaled corticosteroids and risk of acquiring Pseudomonas aeruginosa in patients with chronic obstructive pulmonary disease. Thorax. 2022 Jun;77(6):573-80.
https://thorax.bmj.com/content/77/6/573
http://www.ncbi.nlm.nih.gov/pubmed/34446524?tool=bestpractice.com
ერთმა სისტემურმა მიმოხილვამ და მეტა-ანალიზმა აჩვენა, რომ, მიუხედავად ICS-ისთან ასოცირებული პნევმონიის დაუკორექტირებელი რისკის მნიშვნელოვანი ზრდისა, პნევმონიით სიკვდილიანობა და საერთო სიკვდილიანობა არ გაიზარდა რანდომიზებულ კონტროლირებად კვლევებში და შემცირდა ობსერვაციულ კვლევებში.[120]Festic E, Bansal V, Gupta E, et al. Association of inhaled corticosteroids with incident pneumonia and mortality in COPD patients; systematic review and meta-analysis. COPD. 2016 Jun;13(3):312-26.
https://www.tandfonline.com/doi/full/10.3109/15412555.2015.1081162
http://www.ncbi.nlm.nih.gov/pubmed/26645797?tool=bestpractice.com
ამგვარად, საჭიროა მკურნალობის დანიშვნის დროს ინდივიდუალური მიდგომა, რომლის მიხედვითაც შეფასდება პნევმონიის რისკს მკურნალობის სარგებლთან, გამწვავებების შემცირებასთან, შედარებით.[79]Yang IA, Ferry OR, Clarke MS, et al. Inhaled corticosteroids versus placebo for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2023 Mar 27;(3):CD002991.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD002991.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/36971693?tool=bestpractice.com
[121]Welte T. Inhaled corticosteroids in COPD and the risk of pneumonia. Lancet. 2009 Aug 29;374(9691):668-70.
http://www.ncbi.nlm.nih.gov/pubmed/19716946?tool=bestpractice.com
[122]Kew KM, Seniukovich A. Inhaled steroids and risk of pneumonia for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2014 Mar 10;(3):CD010115.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD010115.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/24615270?tool=bestpractice.com
ასევე შემაშფოთებელია ტუბერკულოზისა და გრიპის განვითარების გაზრდილი რისკი COPD-ით დაავადებულ მოზრდილ პაციენტებთან, რომლებიც ICS თერაპიაზე იმყოფებიან, თუმცა ერთმა მეტა-ანალიზმა აჩვენა, რომ ყველა შეფასებული ტუბერკულოზის შემთხვევის 1%-ზე ნაკლები უკავშირდებოდა ICS-ის ექსპოზიციას.[123]Dong YH, Chang CH, Lin Wu FL, et al. Use of inhaled corticosteroids in patients with COPD and the risk of TB and influenza: a systematic review and meta-analysis of randomized controlled trials. Chest. 2014 Jun;145(6):1286-97.
http://www.ncbi.nlm.nih.gov/pubmed/24504044?tool=bestpractice.com
[124]Castellana G, Castellana M, Castellana C, et al. Inhaled corticosteroids and risk of tuberculosis in patients with obstructive lung diseases: a systematic review and meta-analysis of non-randomized studies. Int J Chron Obstruct Pulmon Dis. 2019 Sep 26;14:2219-27.
https://www.dovepress.com/inhaled-corticosteroids-and-risk-of-tuberculosis-in-patients-with-obst-peer-reviewed-fulltext-article-COPD
http://www.ncbi.nlm.nih.gov/pubmed/31576118?tool=bestpractice.com
ICS-მ ასევე შეიძლება გამოიწვიოს ოროფარინგიალური კანდიდოზი და დისფონია.[79]Yang IA, Ferry OR, Clarke MS, et al. Inhaled corticosteroids versus placebo for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2023 Mar 27;(3):CD002991.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD002991.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/36971693?tool=bestpractice.com
[  ]
What are the benefits and harms of inhaled corticosteroids (ICS) in people with stable chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4293/fullShow me the answer
]
What are the benefits and harms of inhaled corticosteroids (ICS) in people with stable chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4293/fullShow me the answer
მიუხედავად იმისა, რომ იყო შეტყობინებები ICS-ის გამოყენებით ფილტვის კიბოს რისკის როგორც გაზრდის, ისე შემცირების შესახებ, თუმცა როგორც ჩანს, არსებული მონაცემები არ ადასტურებს არცერთ დასკვნას; საჭიროა შემდგომი კვლევები.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
საინჰალაციო კორტიკოსტეროიდების დანიშვნის წინ, ექიმმა უნდა აწონ-დაწონოს პრეპარატის რისკები და სარგებელი პაციენტთან ერთად.[2]National Institute for Health and Care Excellence. Chronic obstructive pulmonary disease in over 16s: diagnosis and management. Jul 2019 [internet publication].
https://www.nice.org.uk/guidance/ng115
ფქოდ-ის გამწვავებების გამო ჰოსპიტალიზაციის ანამნეზი, ორი ან მეტი საშუალო სიმძიმის გამწვავება წელიწადში რეგულარული, ხანგრძლივი მოქმედების ბრონქოდილატატორების მიღების მიუხედავად, სისხლში ეოზინოფილები ≥300 უჯრედი/მიკროლიტრზე, და/ან გადატანილი ან თანმხლები ასთმა მიუთითებს საინჰალაციო კორტიკოსტეროიდის დაწყების საჭიროებაზე.[125]Agusti A, Fabbri LM, Singh D, et al. Inhaled corticosteroids in COPD: friend or foe? Eur Respir J. 2018 Dec 13;52(6):1801219.
https://erj.ersjournals.com/content/52/6/1801219
http://www.ncbi.nlm.nih.gov/pubmed/30190269?tool=bestpractice.com
საინჰალაციო კორტიკოსტეროიდების საწინააღმდეგო ფაქტორებია: პნევმონიის განმეორებითი ეპიზოდები, სისხლში ეოზინოფილების რაოდენობა <100 უჯრედი/მიკროლიტრი და/ან მიკობაქტერიული ინფქეციის ანამნეზი.[125]Agusti A, Fabbri LM, Singh D, et al. Inhaled corticosteroids in COPD: friend or foe? Eur Respir J. 2018 Dec 13;52(6):1801219.
https://erj.ersjournals.com/content/52/6/1801219
http://www.ncbi.nlm.nih.gov/pubmed/30190269?tool=bestpractice.com
ინჰალაციური კორტიკოსტეროიდების გამოყენება გასათვალისწინებელია ფქოდ-ის მქონე პაციენებში, რომელთაც წელიწადში აღენიშნებათ სულ მცირე ერთი საშუალო სიმძიმის გამწვავება, მიუხედავად იმისა, იღებენ თუ არა ისინი ხანგრძლივი მოქმედების ბრონქოდილატატორებს და/ან არის თუ არა პერიფერიული ეოზინოფილების რაოდენობა 100-300 უჯრედი/მიკროლიტრის ფარგლებში.[125]Agusti A, Fabbri LM, Singh D, et al. Inhaled corticosteroids in COPD: friend or foe? Eur Respir J. 2018 Dec 13;52(6):1801219.
https://erj.ersjournals.com/content/52/6/1801219
http://www.ncbi.nlm.nih.gov/pubmed/30190269?tool=bestpractice.com
ევროპის რესპირატორულმა საზოგადოებამ გამოაქვეყნა გაიდლაინი COPD-ის დროს საინჰალაციო კორტიკოსტეროიდების მოხსნის შესახებ.[126]Chalmers JD, Laska IF, Franssen FME, et al. Withdrawal of inhaled corticosteroids in COPD: a European Respiratory Society guideline. Eur Respir J. 2020 Jun 4;55(6):2000351.
https://erj.ersjournals.com/content/55/6/2000351
http://www.ncbi.nlm.nih.gov/pubmed/32366483?tool=bestpractice.com
ფქოდ-ით დაავადებულ პაციენტებში პერორული კორტიკოსტეროიდების ხანგრძლივი გამოყენება რეკომენდებული არ არის.[90]Nici L, Mammen MJ, Charbek E, et al. Pharmacologic management of chronic obstructive pulmonary disease. An official American Thoracic Society clinical practice guideline. Am J Respir Crit Care Med. 2020 May 1;201(9):e56-69.
https://www.atsjournals.org/doi/10.1164/rccm.202003-0625ST
http://www.ncbi.nlm.nih.gov/pubmed/32283960?tool=bestpractice.com
დაავადების მძიმე ფორმის დროს პაციენტთა ნაწილს არ შეუძლია მკურნალობის სრულად შეწყვეტა, გამწვავების დროს პერორული კორტიკოსტეროიდების მიღების შემდეგ. ასეთ შემთხვევაში საჭიროა დოზის რაც შეიძლება დაბალი დონის შენარჩუნება და ოსტეოპოროზის პროფილაქტიკაზე ფიქრი.[2]National Institute for Health and Care Excellence. Chronic obstructive pulmonary disease in over 16s: diagnosis and management. Jul 2019 [internet publication].
https://www.nice.org.uk/guidance/ng115
ბრონქოდილატატორების და კორტიკოსტეროიდების კომბინაცია
ხანგრძლივი მოქმედების ბრონქოდილატატორისა და ICS-ის კომბინირებული პრეპარატი შეიძლება გამოყენებულ იქნას იმ პაციენტებისთვის, რომლებსაც ესაჭიროებათ ორივე ეს პრეპარატი.
[  ]
What are the effects of long‐acting inhaled therapies for adults with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2364/fullShow me the answer ასეთი მიდგომა ზოგჯერ მოსახერხებელია და გვეხმარება ზოგიერთი პაციენტის დაყოლიებაში. ამ კლასში პრეპარატების არჩევა ხელმისაწვდომობას და ინდივიდუალურ დამყოლობას ეფუძნება.[127]Tricco AC, Strifler L, Veroniki AA, et al. Comparative safety and effectiveness of long-acting inhaled agents for treating chronic obstructive pulmonary disease: a systematic review and network meta-analysis. BMJ Open. 2015 Oct 26;5(10):e009183. [Erratum in: BMJ Open. 2019 May 1;9(4):e009183corr1.]
https://bmjopen.bmj.com/content/5/10/e009183.long
http://www.ncbi.nlm.nih.gov/pubmed/26503392?tool=bestpractice.com
კომბინაცია შეიძლება სხვადახვა ინჰალატორით ან ერთი კობინირებუი ინჰალატორით.
]
What are the effects of long‐acting inhaled therapies for adults with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2364/fullShow me the answer ასეთი მიდგომა ზოგჯერ მოსახერხებელია და გვეხმარება ზოგიერთი პაციენტის დაყოლიებაში. ამ კლასში პრეპარატების არჩევა ხელმისაწვდომობას და ინდივიდუალურ დამყოლობას ეფუძნება.[127]Tricco AC, Strifler L, Veroniki AA, et al. Comparative safety and effectiveness of long-acting inhaled agents for treating chronic obstructive pulmonary disease: a systematic review and network meta-analysis. BMJ Open. 2015 Oct 26;5(10):e009183. [Erratum in: BMJ Open. 2019 May 1;9(4):e009183corr1.]
https://bmjopen.bmj.com/content/5/10/e009183.long
http://www.ncbi.nlm.nih.gov/pubmed/26503392?tool=bestpractice.com
კომბინაცია შეიძლება სხვადახვა ინჰალატორით ან ერთი კობინირებუი ინჰალატორით.
მრავალი კვლევის მიხედვით, რეკომენდებულია სამმაგი თერაპია ხანგრძლივი მოქმედების ბეტა-2 აგონისტი/ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტი/ინჰალაციური კორტიკოსტეროიდებით, რადგან აღნიშნული უპირატესია ერთმაგ ან ორმაგ თერაპიასთან შედარებით ხანგრძლივი მოქმედების ბეტა-2 აგონისტი/ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტის ან ხანგრძლივი მოქმედების ბეტა-2 აგონისტი/ინჰალაციური კორტიკოსტეროიდების კომბინაციებში, საშუალო-მძიმე ფქოდ-ის გამწვავებების და ჰოსპიტალიზაციის სიხშირის შემცირების თვალსაზრისით.[74]Cazzola M, Rogliani P, Calzetta L, et al. Triple therapy versus single and dual long-acting bronchodilator therapy in COPD: a systematic review and meta-analysis. Eur Respir J. 2018 Dec 13;52(6):1801586.
https://erj.ersjournals.com/content/52/6/1801586
http://www.ncbi.nlm.nih.gov/pubmed/30309975?tool=bestpractice.com
[82]Singh D, Papi A, Corradi M, et al. Single inhaler triple therapy versus inhaled corticosteroid plus long-acting beta2-agonist therapy for chronic obstructive pulmonary disease (TRILOGY): a double-blind, parallel group, randomised controlled trial. Lancet. 2016 Sep 3;388(10048):963-73.
http://www.ncbi.nlm.nih.gov/pubmed/27598678?tool=bestpractice.com
[83]Vestbo J, Papi A, Corradi M, et al. Single inhaler extrafine triple therapy versus long-acting muscarinic antagonist therapy for chronic obstructive pulmonary disease (TRINITY): a double-blind, parallel group, randomised controlled trial. Lancet. 2017 May 13;389(10082):1919-29.
http://www.ncbi.nlm.nih.gov/pubmed/28385353?tool=bestpractice.com
[84]Papi A, Vestbo J, Fabbri L, et al. Extrafine inhaled triple therapy versus dual bronchodilator therapy in chronic obstructive pulmonary disease (TRIBUTE): a double-blind, parallel group, randomised controlled trial. Lancet. 2018 Mar 17;391(10125):1076-84.
http://www.ncbi.nlm.nih.gov/pubmed/29429593?tool=bestpractice.com
[85]Lipson DA, Barnacle H, Birk R, et al. FULFIL Trial: once-daily triple therapy for patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2017 Aug 15;196(4):438-46.
https://www.atsjournals.org/doi/full/10.1164/rccm.201703-0449OC
http://www.ncbi.nlm.nih.gov/pubmed/28375647?tool=bestpractice.com
[86]Lipson DA, Barnhart F, Brealey N, et al. Once-daily single-inhaler triple versus dual therapy in patients with COPD. N Engl J Med. 2018 May 3;378(18):1671-80.
https://www.nejm.org/doi/10.1056/NEJMoa1713901
http://www.ncbi.nlm.nih.gov/pubmed/29668352?tool=bestpractice.com
[87]Rojas-Reyes MX, García Morales OM, Dennis RJ, et al. Combination inhaled steroid and long-acting beta₂-agonist in addition to tiotropium versus tiotropium or combination alone for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2016 Jun 6;(6):CD008532.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD008532.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/27271056?tool=bestpractice.com
[88]Lai CC, Chen CH, Lin CYH, et al. The effects of single inhaler triple therapy vs single inhaler dual therapy or separate triple therapy for the management of chronic obstructive pulmonary disease: a systematic review and meta-analysis of randomized controlled trials. Int J Chron Obstruct Pulmon Dis. 2019 Jul 11;14:1539-48. [Erratum in: Int J Chron Obstruct Pulmon Dis. 2020 Jan 21;15:155-6.]
https://www.dovepress.com/the-effects-of-single-inhaler-triple-therapy-vs-single-inhaler-dual-th-peer-reviewed-fulltext-article-COPD
http://www.ncbi.nlm.nih.gov/pubmed/31371939?tool=bestpractice.com
[89]Rabe KF, Martinez FJ, Ferguson GT, et al. Triple inhaled therapy at two glucocorticoid doses in moderate-to-very-severe COPD. N Engl J Med. 2020 Jul 2;383(1):35-48.
http://www.ncbi.nlm.nih.gov/pubmed/32579807?tool=bestpractice.com
ICS-ის გამოყენება ასევე ანელებს გამწვავების შემდეგ ფილტვის ფუნქციის დაქვეითების ტემპს პაციენტებთან, რომლებსაც აქვთ მსუბუქი და საშუალო სიმძიმის COPD და მომატებული ეოზინოფილები სისხლში.[128]Kerkhof M, Voorham J, Dorinsky P, et al. Association between COPD exacerbations and lung function decline during maintenance therapy. Thorax. 2020 Sep;75(9):744-53.
https://thorax.bmj.com/content/75/9/744
http://www.ncbi.nlm.nih.gov/pubmed/32532852?tool=bestpractice.com
ერთმა რანდომიზებულმა კონტროლირებადმა კვლევამ აჩვენა ყველა მიზეზით სიკვდილიანობის შემცირება პაციენტებთან FEV1 <50%-ით და ბოლო წელს სულ მცირე ერთი გამწვავებით, რომლებიც იღებდნენ ფლუტიკაზონის ფუროატს/უმეკლიდინიუმს/ვილანტეროლს, იმ პაციენტებთან შედარებით, რომლებიც იღებენ უმეკლიდინიუმს/ვილანტეროლს. პაციენტებს მსუბუქი COPD-ით და ბოლო წელს მინიმუმ ორი ზომიერი ან ერთი მძიმე გამწვავებით ასევე აღენიშნებობათ ყველა მიზეზით სიკვდილიანობის კლება ფლუტიკაზონის ფუროატის/უმეკლიდინიუმის/ვილანტეროლის მიღებისას, უმეკლიდინიუმ/ვილანტეროლთან შედარებით.[129]Lipson DA, Crim C, Criner GJ, et al. Reduction in all-cause mortality with fluticasone furoate/umeclidinium/vilanterol in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2020 Jun 15;201(12):1508-16.
https://www.atsjournals.org/doi/10.1164/rccm.201911-2207OC
http://www.ncbi.nlm.nih.gov/pubmed/32162970?tool=bestpractice.com
ერთ-ერთ სხვა რანდომიზებულ კვლვევაშიც, სამმაგი თერაპიის მიმღებ ჯგუფში (ბუდესონიდი/გლიკოპირონიუმი/ფორმოტეროლი), დაფიქსირდა მსგავსი შედეგები სიკვდილობის თვალსაზრისით, თუმცა იყენებდნენ საინჰალაციო კორტიკოსტეროიდის უფრო მაღალ დოზას.[89]Rabe KF, Martinez FJ, Ferguson GT, et al. Triple inhaled therapy at two glucocorticoid doses in moderate-to-very-severe COPD. N Engl J Med. 2020 Jul 2;383(1):35-48.
http://www.ncbi.nlm.nih.gov/pubmed/32579807?tool=bestpractice.com
[130]Martinez FJ, Rabe KF, Ferguson GT, et al. Reduced all-cause mortality in the ETHOS trial of budesonide/glycopyrrolate/formoterol for chronic obstructive pulmonary disease. A randomized, double-blind, multicenter, parallel-group study. Am J Respir Crit Care Med. 2021 Mar 1;203(5):553-64.
https://www.atsjournals.org/doi/10.1164/rccm.202006-2618OC
http://www.ncbi.nlm.nih.gov/pubmed/33252985?tool=bestpractice.com
იმავე კვლევამ აჩვენა, რომ სამმაგი თერაპიის დროს ბუდესონიდის დოზის გაზრდა არ ამცირებს გამწვავებების სიხშირეს, სტანდარტულ სამმაგ თერაპიასთან შედარებით.[89]Rabe KF, Martinez FJ, Ferguson GT, et al. Triple inhaled therapy at two glucocorticoid doses in moderate-to-very-severe COPD. N Engl J Med. 2020 Jul 2;383(1):35-48.
http://www.ncbi.nlm.nih.gov/pubmed/32579807?tool=bestpractice.com
ორივე კვლევის ფარგლებში, სიკვდილობის კუთხით არ აღმოჩნდა განსხვავება ხანგრძლივი მოქმედების ბეტა-2 აგონისტი/საინჰალაციო კორტიკოსტეროიდებით ორმაგ თერაპიასთნ შედარებით.[89]Rabe KF, Martinez FJ, Ferguson GT, et al. Triple inhaled therapy at two glucocorticoid doses in moderate-to-very-severe COPD. N Engl J Med. 2020 Jul 2;383(1):35-48.
http://www.ncbi.nlm.nih.gov/pubmed/32579807?tool=bestpractice.com
[129]Lipson DA, Crim C, Criner GJ, et al. Reduction in all-cause mortality with fluticasone furoate/umeclidinium/vilanterol in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2020 Jun 15;201(12):1508-16.
https://www.atsjournals.org/doi/10.1164/rccm.201911-2207OC
http://www.ncbi.nlm.nih.gov/pubmed/32162970?tool=bestpractice.com
[130]Martinez FJ, Rabe KF, Ferguson GT, et al. Reduced all-cause mortality in the ETHOS trial of budesonide/glycopyrrolate/formoterol for chronic obstructive pulmonary disease. A randomized, double-blind, multicenter, parallel-group study. Am J Respir Crit Care Med. 2021 Mar 1;203(5):553-64.
https://www.atsjournals.org/doi/10.1164/rccm.202006-2618OC
http://www.ncbi.nlm.nih.gov/pubmed/33252985?tool=bestpractice.com
სამმაგ თერაპიაზე ჩატარებულმა სამი კვლევის ანალიზმა COPD-ის, ჰაერის ნაკადის მძიმე შეზღუდვის და ანამნეზში გამწვავებების მქონე პაციენტებთან სამმაგი თერაპიის პირობებში აჩვენა სიკვდილიანობის უმნიშვნელო შემცირების ტენდენცია, ICS-ის გარეშე მკურნალობასთან შედარებით.[131]Vestbo J, Fabbri L, Papi A, et al. Inhaled corticosteroid containing combinations and mortality in COPD. Eur Respir J. 2018 Dec 13;52(6):1801230.
https://erj.ersjournals.com/content/52/6/1801230
http://www.ncbi.nlm.nih.gov/pubmed/30209195?tool=bestpractice.com
ეს შედეგები აძლიერებს 200-ზე მეტი კვლევის მეტაანალიზის შედეგებს: სამმაგი თერაპია უზრუნველყოფდა სიკვდილიანობის მნიშვნელოვან შემცირებას ორმაგი თერაპიის წინააღმდეგ, თუმცა ასოცირებული იყო პნევმონიის უფრო დიდ რისკთან. ფილტვების ფუნქციის ან ჯანმრთელობასთან დაკავშირებული ცხოვრების ხარისხის თვალსაზრისით სამკურნალო რეჟიმების მიხედვით განსხვავება არ დაფიქსირებულა.[132]Axson EL, Lewis A, Potts J, et al. Inhaled therapies for chronic obstructive pulmonary disease: a systematic review and meta-analysis. BMJ Open. 2020 Sep 29;10(9):e036455.
https://bmjopen.bmj.com/content/10/9/e036455
http://www.ncbi.nlm.nih.gov/pubmed/32994234?tool=bestpractice.com
სამმაგი თერაპიის დანიშვნამდე კლინიცისტებმა უნდა შეაფასონ შეიძლება თუ არა სხვა ფიზიკურმა ან მენტალურმა მდგომარეობამ გამოიწვიოს პაციენტის სიმპტომები. დიდი ბრიტანეთის გაიდლაინებით, სამმაგ მკურნალობაზე მყოფი პაციენტების ყოველდღიურ სიმპტომებზე შეფასებაა რეკომენდებული მკურნალობის 3 თვის თავზე. მკურნალობა უნდა შეიცვალოს LABA/LAMA-ით, თუ პაციენტის სიმპტომები არ გაუმჯობესდა.[2]National Institute for Health and Care Excellence. Chronic obstructive pulmonary disease in over 16s: diagnosis and management. Jul 2019 [internet publication].
https://www.nice.org.uk/guidance/ng115
თუ უკანასკნელი წლის განმავლობაში პაციენტს არ ჰქონია გამწვავებები, შესაძლებელია საინჰალაციო კორტიკოსტეროიდების შეჩერება.[90]Nici L, Mammen MJ, Charbek E, et al. Pharmacologic management of chronic obstructive pulmonary disease. An official American Thoracic Society clinical practice guideline. Am J Respir Crit Care Med. 2020 May 1;201(9):e56-69.
https://www.atsjournals.org/doi/10.1164/rccm.202003-0625ST
http://www.ncbi.nlm.nih.gov/pubmed/32283960?tool=bestpractice.com
რეალური მონაცემების ერთმა სისტემურმა მიმოხილვამ მცირე მტკიცებულებიდან მტკიცებულებების არარსებობა აჩვენა მკურნალობის გაუარესებული გამოსავლის თვალსაზრისით შემთხვევებში, სადაც ICS მოხსნილი იყო და გაგრძელებული იყო ზომიერიდან მძიმე ფორმის COPD-ის მქონე პაციენტების შესაბამისი ფარმაკოლოგიური მართვა.[133]Rogliani P, Ritondo BL, Gabriele M, et al. Optimizing de-escalation of inhaled corticosteroids in COPD: a systematic review of real-world findings. Expert Rev Clin Pharmacol. 2020 Sep;13(9):977-90.
https://www.tandfonline.com/doi/full/10.1080/17512433.2020.1817739
http://www.ncbi.nlm.nih.gov/pubmed/32885691?tool=bestpractice.com
ფოსფოდიესთერაზა-4-ის ინჰიბიტორი
როფლუმილასტი არის ორალური ფოსფოდიესტერაზა-4-ის ინჰიბიტორი, რომელიც აფერხებს cAMP-ის დაშლას. ის შეიძლება დაინიშნოს პაციენტებთან, ვისთანაც FEV1 < სავარაუდოს 50%, არის ქრონიკული ბრონქიტი, იღებენ LABA/LAMA/ICS-ს, განსაკუთრებით იმ შემთხვევაში, თუ მათ ჰქონდათ მინიმუმ ერთი ჰოსპიტალიზაცია გამწვავების გამო ბოლო ერთი წლის განმავლობაში.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
როფლუმილასტის გამოყენება აუმჯობესებს ფილტვის ფუნქციასა და დიდი ალბათობით ამცირებს გამწვავებების რიცხვს. თუმცა, მცირედ ეფექტი აქვს სიცოცხლის ხარისხსა და სიმპტომებზე.[134]Janjua S, Fortescue R, Poole P. Phosphodiesterase-4 inhibitors for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2020 May 1;(5):CD002309.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD002309.pub6/full
http://www.ncbi.nlm.nih.gov/pubmed/32356609?tool=bestpractice.com
[  ]
How do phosphodiesterase‐4 inhibitors compare with placebo for people with chronic obstructive pulmonary disease?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.3151/fullShow me the answer
]
How do phosphodiesterase‐4 inhibitors compare with placebo for people with chronic obstructive pulmonary disease?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.3151/fullShow me the answer
ანტიბიოტიკები
გამწვავების რისკის შესამცირებლად შეიძლება გავითვალისწინოთ პროფილაქტიკური ანტიბიოტიკები, მაგ. მაკროლიდები, განსაკუთრებით ხშირი გამწვავებების დროს, რომლებიც რეზისტენტულია სტანდარტული თერაპიის მიმართ.[135]Simoens S, Laekeman G, Decramer M. Preventing COPD exacerbations with macrolides: a review and budget impact analysis. Respir Med. 2013 May;107(5):637-48.
http://www.ncbi.nlm.nih.gov/pubmed/23352223?tool=bestpractice.com
[136]Lee JS, Park DA, Hong Y, et al. Systematic review and meta-analysis of prophylactic antibiotics in COPD and/or chronic bronchitis. Int J Tuberc Lung Dis. 2013 Feb;17(2):153-62.
http://www.ncbi.nlm.nih.gov/pubmed/23317949?tool=bestpractice.com
[137]Uzun S, Djamin RS, Kluytmans JA, et al. Azithromycin maintenance treatment in patients with frequent exacerbations of chronic obstructive pulmonary disease (COLUMBUS): a randomised, double-blind, placebo-controlled trial. Lancet Respir Med. 2014 May;2(5):361-8.
http://www.ncbi.nlm.nih.gov/pubmed/24746000?tool=bestpractice.com
[138]Janjua S, Mathioudakis AG, Fortescue R, et al. Prophylactic antibiotics for adults with chronic obstructive pulmonary disease: a network meta-analysis. Cochrane Database Syst Rev. 2021 Jan 15;(1):CD013198.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD013198.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/33448349?tool=bestpractice.com
Cochrane-ის ერთმა მიმოხილვამ გამწვავებების და სერიოზული გვერდითი მოვლენების შემცირების და ცხოვრების ხარისხის გაუმჯობესების თვალსაზრისით მაკროლიდები დაასახელა პირველ ადგილზე, ფთორქინოლონების და ტეტრაციკლინების წინ.[138]Janjua S, Mathioudakis AG, Fortescue R, et al. Prophylactic antibiotics for adults with chronic obstructive pulmonary disease: a network meta-analysis. Cochrane Database Syst Rev. 2021 Jan 15;(1):CD013198.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD013198.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/33448349?tool=bestpractice.com
ფქოდ-ის მქონე პაციენტებში პროფილაქტიკური მაკროლიდური ანტიბიოტიკები ამცირებs გამწვავებების სიხშირეს, თუმცა აზითრომიცინის ხანგრძლივი გამოყენება იწვევს სმენის მძიმე დაქვეითებას, რაც, ხშირად შექცევად ხასიათისაა.[139]Herath SC, Normansell R, Maisey S, et al. Prophylactic antibiotic therapy for chronic obstructive pulmonary disease (COPD). Cochrane Database Syst Rev. 2018 Oct 30;(10):CD009764.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD009764.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/30376188?tool=bestpractice.com
[  ]
What are the effects of prophylactic antibiotics for people with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2431/fullShow me the answer არ არსებობს მტკიცებულებები აზითრომიცინით მკურნალობის ეფექტიანობის შესახებ 1 წელზე ხანგრძლივად.
]
What are the effects of prophylactic antibiotics for people with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2431/fullShow me the answer არ არსებობს მტკიცებულებები აზითრომიცინით მკურნალობის ეფექტიანობის შესახებ 1 წელზე ხანგრძლივად.
მიიჩნევა, რომ აზითრომიცინი ყველაზე მეტად ეფექტურია გამწვავების პრევენციის თვალსაზრისით და ხასიათდება მეტი ეფექტურობით ხანდაზმულ პაციენტებში, ფქოდ-ის გლობალური ინიციატივის კლასიფიკაციით მსუბუქი სტადიების დროს. აქტიურ მწეველებში მკურნალობის სარგებლის მტკიცებულებები მცირეა.[140]Han MK, Tayob N, Murray S, et al. Predictors of chronic obstructive pulmonary disease exacerbation reduction in response to daily azithromycin therapy. Am J Respir Crit Care Med. 2014 Jun 15;189(12):1503-8.
https://www.atsjournals.org/doi/full/10.1164/rccm.201402-0207OC#.V9weczUpW9Y
http://www.ncbi.nlm.nih.gov/pubmed/24779680?tool=bestpractice.com
აზითრომიცინი ზრდის მაკროლიდის მიმართ რეზისტენტული მიკროორგანიზმების კოლონიზაციის რისკს და არ უნდა დაინიშნოს პაციენტებში, რომელთაც აღენიშნებათ სმენის დაქვეითბა, ტაქიკარდია მოსვენებულ მდგომარეობაში ან QTc ინტერვალის პროლონგირების მკაფიო რისკი.[141]Albert RK, Connett J, Bailey WC, et al; COPD Clinical Research Network. Azithromycin for prevention of exacerbations of COPD. N Engl J Med. 2011 Aug 25;365(8):689-98.
https://www.nejm.org/doi/full/10.1056/NEJMoa1104623
http://www.ncbi.nlm.nih.gov/pubmed/21864166?tool=bestpractice.com
პირველ რიგში, განიხილება აზითრომიცინის დანიშვნა (და არა მხოლოდ), ყოფილ მწეველებში, რომელთაც შესაბამისი მკურნალობის მიუხედავად აქვთ მუდმივი გამწვავებები.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
დიდი ბრიტანეთის გაიდლაინების რეკომენდაციით, პროფილაქტიკური აზითრომიცინი უნდა განვიხილოთ პაციენტებში, რომელთაც ყოველწლიურად აღნიშნებათ კორტიკოსტეროიდული თერაპიის ჩვენებით მიმდინარე სამზე მეტი გამწვავება ან სულ მცირე 1 გამწვავება, რომელსაც დასჭირდა ჰოსპიტალიზაცია.[142]Smith D, Du Rand I, Addy CL, et al. British Thoracic Society guideline for the use of long-term macrolides in adults with respiratory disease. Thorax. 2020 May;75(5):370-404.
https://thorax.bmj.com/content/75/5/370
http://www.ncbi.nlm.nih.gov/pubmed/32303621?tool=bestpractice.com
პროფილაქტიკური ანტიბიოტიკების დაწყებამდე უნდა ჩატარდეს საბაზისო ეკგ და ღვიძლის ფუნქციური ტესტები, ნახველის ნიმუშის კულტურალური კვლევა და მგრძნობელობის ტესტირება (ტუბერკულოზის ტესტირების ჩათვლით), ნახველის კლირენსის ტექნიკის ოპტიმიზაცია უნდა მოხდეს და ბრონქოექტაზია CT სკანირებით უნდა გამოირიცხოს.[2]National Institute for Health and Care Excellence. Chronic obstructive pulmonary disease in over 16s: diagnosis and management. Jul 2019 [internet publication].
https://www.nice.org.uk/guidance/ng115
[142]Smith D, Du Rand I, Addy CL, et al. British Thoracic Society guideline for the use of long-term macrolides in adults with respiratory disease. Thorax. 2020 May;75(5):370-404.
https://thorax.bmj.com/content/75/5/370
http://www.ncbi.nlm.nih.gov/pubmed/32303621?tool=bestpractice.com
ეკგ და ღვიძლის ტესტები უნდა ჩატარდეს მკურნალობიდან 1 თვის შემდეგ. ფთორქინოლონების, ტეტრაციკლინების და მაკროლიდების შედარებამ, რომლებიც COPD-ით დაავადებულ პირებთან 12-13 კვირის განმავლობაში იყო დანიშნული, ეფექტურობის და უსაფრთხოების თვალსაზრისით ანტიბიოტიკების ჯგუფებს შორის განსხვავება არ გამოავლინა, თუმცა ამასთანავე ჩართული კვლევების რაოდენობა და კვლევების ხანგრძლივობა მცირე იყო; ამ მიმართულებით შემდგომი კვლევაა საჭირო.[143]Threapleton CJ, Janjua S, Fortescue R, et al. Head-to-head oral prophylactic antibiotic therapy for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2019 May 24;(5):CD013024.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD013024.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/31125127?tool=bestpractice.com
პროფილაქტიკური ანტიბიოტიკოთერაპია უნდა გადაიხედოს მე-6 და მე-12 თვეებზე, რათა განისაზღვროს სარგებელი გამწვავებების სიხშირის კუთხით.[142]Smith D, Du Rand I, Addy CL, et al. British Thoracic Society guideline for the use of long-term macrolides in adults with respiratory disease. Thorax. 2020 May;75(5):370-404.
https://thorax.bmj.com/content/75/5/370
http://www.ncbi.nlm.nih.gov/pubmed/32303621?tool=bestpractice.com
თუ ანტიბიოტიკოთერაპია არაეფექტურია, უნდა შეწყდეს.
მეთილქსანტინები
თეოფილინი (მეთილქსანტინური აგენტი) არის ბრონქოდილატატორი, რომელიც ზრდის ციკლურ ადენოზინ მონოფოსფატს, რაც თავის მხრივ იწვევს სასუნთქი გლუვი კუნთების მოდუნებას. ის ფართოდ არ გამოიყენება, რადგან ახასიათებს ლიმიტირებული თერაპიული ეფექტი, მაღალი რისკი და ხშირად სხვა პრეპარატებთან ურთიერთქმედება. ფქოდ-ის საშუალო და მძიმე ხარისხის დროს, თეოფილინის ეფექტები ფილტვის ფუნქციაზე მინიმალურია.[144]Ram FSF, Jones P, Jardim J, et al. Oral theophylline for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2002;(4):CD003902.
http://www.ncbi.nlm.nih.gov/pubmed/12519617?tool=bestpractice.com
დიდმა რანდომიზებულმა კონტროლირებადმა კვლევამ ცალკე ან პრედნიზოლონთან ერთად დანიშნული პერორალური თეოფილინის ეფექტი მძიმე COPD-ის გამწვავებაზე არ აჩვენა.[145]Jenkins CR, Wen FQ, Martin A, et al; TASCS study investigators. The effect of low-dose corticosteroids and theophylline on the risk of acute exacerbations of COPD: the TASCS randomised controlled trial. Eur Respir J. 2021 Jun 10;57(6):2003338.
https://erj.ersjournals.com/content/57/6/2003338
http://www.ncbi.nlm.nih.gov/pubmed/33334939?tool=bestpractice.com
სპეციალისტმა თეოფილინი შეიძლება დანიშნოს მაშინ, როდესაც პაციენტთან საინჰალაციო თერაპიის ყველა ვარიანტი გამოყენებულია. თეოფილინი არ არის რეკომენდებული, მანამ სანამ გრძელვადიანი ბრონქოდილატატორები არ არის ხელმისაწვდომი ან მათი შეძენა შეუძლებელია.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
პაციენტების განათლება და დამოუკიდებელი მართვა
ყველა პაციენტს უნა ჩაუტარდეს სწავლება დაავადების მიმდინარეობის, გამწვავების და დეკომპენსაციის სიმპტომების შესახებ. მათი მოლოდინი დაავადების მიმდინარეობის, მკურნალობის და პროგნოზის შესახებ რეალისტური უნდა იყოს. მნიშვნელოვანია გვახსოვდეს, რომ არ არსებობს მედიკამენტი, რომელსაც შეუძლია შეცვალოს ფილტვის ფუნქციური რეგრესი ხანგრძლივ პერსპექტივაში და რომ ფარმაკოთერაპიის მიზანს წარმოადგენს სიმპტომების კონტროლი და გართულებების პრევენცია.
Cochrane-ის ერთი მიმოხილვის თანახმად, პაციენტის თვითაქტივობები, მაგ. სამოქმედო გეგმის ქონა ფქოდ-ის გამწვავებებისათვის, დაკავშირებულია სიცოცხლის ხარისხის გაუმჯობესებასთან და ჰოსპიტალიზაცის ნაკლებ სიხშირესთან რესპირატორული პრობლემების გამო. ექსპლორაციული ანალიზით გამოირკვა, რომ რესპირატორული სიკვდილობის სიხშირე მცირედ უფრო მაღალია დამოუკიდებელი მართვის დროს, ვიდრე სტანდარტულ შემთხვევაში, თუმცა საერთო სიკვდილობის მატება არ აღინიშნა.[146]Lenferink A, Brusse-Keizer M, van der Valk PD, et al. Self-management interventions including action plans for exacerbations versus usual care in patients with chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2017 Aug 4;(8):CD011682.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD011682.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/28777450?tool=bestpractice.com
რანდომიზებული კონტროლირებული კვლევით ვლინდება, რომ ფქოდ-ის გამწვავებების მქონე პაციენტებში, რომლებიც უკანასკნელ პერიოდში გაწერეს კლინიკიდან, საკუთარი თავის მართვის 3-თვიანი პროგრამა ზრდის ფქოდ-თან დაკავშირებული ჰოსპიტალზიაციის და გადაუდებელ სამედიცინო დახმარებაში ვიზიტების სიხშირეს 6 თვეზე ხანგრძლივი დროის განმავლობაში.[147]Aboumatar H, Naqibuddin M, Chung S, et al. Effect of a hospital-initiated program combining transitional care and long-term self-management support on outcomes of patients hospitalized with chronic obstructive pulmonary disease: a randomized clinical trial. JAMA. 2019 Oct 8;322(14):1371-80.
https://jamanetwork.com/journals/jama/fullarticle/2752467
http://www.ncbi.nlm.nih.gov/pubmed/31593271?tool=bestpractice.com
პაციენტის მხრიდან საკუთარი მდგომარეობის მართვის გეგმა უნდა მოიცავდეს პერსონალიზებულ რჩევებს შემდეგის შესახებ: ქოშინი და სტრესის მართვის ტექნიკები; ენერგიის დაზოგვა; დამამძიმებელი ფაქტორების თავიდან აცილება; როგორ უნდა მოხდეს სიმპტომები მონიტორინგი; როგორ ვმართოთ სიმპტომების გაუარესება; და საკონტაქტო ინფორმაცია გამწვავების შემთხვევაში გამოსაყენებლად.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
იდეალურ შემთხვევაში თვითკონტროლში პაციენტების დახმარება ფსიქოსოციალური მხარდაჭერისა და COPD-ის და მისი მართვის შესახებ ინდივიდუალური დამოკიდებულების შექმნისკენ უნდა იყოს მიმართული. ბევრი პაციენტი აღნიშნავს, რომ დაკარგა და შეეზღუდა ცხოვრების წესი და სოციალური ურთიერთობები ფქოდის დიაგნოზის შემდეგ. შეფასებულია, რომ COPD-ით დაავადებული პაციენტები 1.9-ჯერ უფრო ხშირად ასრულებენ ცხოვრებას თვითმკვლელობით, ვიდრე COPD-ის გარეშე და ხშირია შფოთვის, დეპრესიისა და იმედგაცრუების სიმპტომები.[148]Sampaio MS, Vieira WA, Bernardino ÍM, et al. Chronic obstructive pulmonary disease as a risk factor for suicide: a systematic review and meta-analysis. Respir Med. 2019 May;151:11-18.
https://www.resmedjournal.com/article/S0954-6111(19)30093-9/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/31047105?tool=bestpractice.com
[149]Russell S, Ogunbayo OJ, Newham JJ, et al. Qualitative systematic review of barriers and facilitators to self-management of chronic obstructive pulmonary disease: views of patients and healthcare professionals. NPJ Prim Care Respir Med. 2018 Jan 17;28(1):2.
https://www.nature.com/articles/s41533-017-0069-z
http://www.ncbi.nlm.nih.gov/pubmed/29343739?tool=bestpractice.com
კვლევებმა აჩვენა კოგნიტური ქცევითი თერაპიის (CBT) სასარგებლო ეფექტი დეპრესიისა და შფოთვის სიმპტომებზე, ცხოვრების ხარისხზე და გადაუდებელი სამედიცინო დახმარების განყოფილებაში ვიზიტების სიხშირეზე.[150]Pollok J, van Agteren JE, Esterman AJ, et al. Psychological therapies for the treatment of depression in chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2019 Mar 6;(3):CD012347.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD012347.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/30838649?tool=bestpractice.com
[151]Ma RC, Yin YY, Wang YQ, et al. Effectiveness of cognitive behavioural therapy for chronic obstructive pulmonary disease patients: a systematic review and meta-analysis. Complement Ther Clin Pract. 2020 Feb;38:101071.
http://www.ncbi.nlm.nih.gov/pubmed/31743870?tool=bestpractice.com
[152]Williams MT, Johnston KN, Paquet C. Cognitive behavioral therapy for people with chronic obstructive pulmonary disease: rapid review. Int J Chron Obstruct Pulmon Dis. 2020 Apr 23;15:903-19.
https://www.dovepress.com/cognitive-behavioral-therapy-for-people-with-chronic-obstructive-pulmo-peer-reviewed-fulltext-article-COPD
http://www.ncbi.nlm.nih.gov/pubmed/32425516?tool=bestpractice.com
მაღალრესურსინი-ინტენსიური და დაბალრესურსიანი-ინტენსიური CBT-ის ეფექტების შესაფასებლად შემდგომი კვლევებია საჭირო.[152]Williams MT, Johnston KN, Paquet C. Cognitive behavioral therapy for people with chronic obstructive pulmonary disease: rapid review. Int J Chron Obstruct Pulmon Dis. 2020 Apr 23;15:903-19.
https://www.dovepress.com/cognitive-behavioral-therapy-for-people-with-chronic-obstructive-pulmo-peer-reviewed-fulltext-article-COPD
http://www.ncbi.nlm.nih.gov/pubmed/32425516?tool=bestpractice.com
ერთი რანდომიზებული კონტროლირებადი კვლევით აღმოჩნდა, რომ ტელეფონით დახმარება და ქცევითი ცვლილებების ხარდაჭერა მსუბუქი ფქოდ-ის დროს პირველად ჯანდაცვაში იწვევს დამოუკიდებელი აქტივობების გაუმჯობესებას, მაგრამ სიცოცხლის ხარისხზე გავლენა არ აქვს.[153]Jolly K, Sidhu MS, Hewitt CA, et al. Self management of patients with mild COPD in primary care: randomised controlled trial. BMJ. 2018 Jun 13;361:k2241.
https://www.bmj.com/content/361/bmj.k2241.long
http://www.ncbi.nlm.nih.gov/pubmed/29899047?tool=bestpractice.com
მეტა-ანალიზით გამოვლინდა, რომ ჯანმრთელობის შესახებ სწავლება, რომელიც მოიცავდა მიზნების დასახვას, სამოტივაციო ინტერვიუებსა და ფქოდ-თან დაკავშირებულ ცნობიერების ამაღლებას, მნიშვნელოვნად აუმჯობესებდა სიცოცხლის ხარისხს და ამცირებდა ფქოდ-ის გამწვავების მიზეზით ჰოსპიტალიზაციის სიხშირეს, თუმცა არ აქვეითებდა ნებისმიერი მიზეზით ჰოსპიტალიზაციის რაოდენობას.[154]Long H, Howells K, Peters S, et al. Does health coaching improve health-related quality of life and reduce hospital admissions in people with chronic obstructive pulmonary disease? A systematic review and meta-analysis. Br J Health Psychol. 2019 Sep;24(3):515-46.
https://bpspsychub.onlinelibrary.wiley.com/doi/10.1111/bjhp.12366
http://www.ncbi.nlm.nih.gov/pubmed/31033121?tool=bestpractice.com
საინჰალაციო თერაპიაზე მყოფ პაციენტებს სჭირდებათ ტრენინგი საინჰალაციო მოწყობილობის ტექნიკის შესასწავლად. პაციენტების უმრავლესობა უშვებს მინიმუმ ერთ შეცდომას ინჰალატორის გამოყენებისას და ინჰალატორის არასწორი გამოყენება ასოცირდება დაავადების ცუდ კონტროლთან.[155]Cho-Reyes S, Celli BR, Dembek C, et al. Inhalation technique errors with metered-dose inhalers among patients with obstructive lung diseases: a systematic review and meta-analysis of US Studies. Chronic Obstr Pulm Dis. 2019 Jul 24;6(3):267-80.
https://journal.copdfoundation.org/jcopdf/id/1241/Inhalation-Technique-Errors-with-Metered-Dose-Inhalers-Among-Patients-with-Obstructive-Lung-Diseases-A-Systematic-Review-and-Meta-Analysis-of-US-Studies
http://www.ncbi.nlm.nih.gov/pubmed/31342732?tool=bestpractice.com
[156]Melani AS, Bonavia M, Cilenti V, et al. Inhaler mishandling remains common in real life and is associated with reduced disease control. Respir Med. 2011 Jun;105(6):930-8.
https://www.resmedjournal.com/article/S0954-6111(11)00009-6/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/21367593?tool=bestpractice.com
ინჰალატორის არასწორი გამოყენება უფრო ხშირია როცა პაციენტი იყენებს სხვადასხვა მოწყობილობას ან არასდროს უსწავლებიათ ინჰალატორის მოხმარება.[157]Rootmensen GN, van Keimpema AR, Jansen HM, et al. Predictors of incorrect inhalation technique in patients with asthma or COPD: a study using a validated videotaped scoring method. J Aerosol Med Pulm Drug Deliv. 2010 Oct;23(5):323-8.
http://www.ncbi.nlm.nih.gov/pubmed/20804428?tool=bestpractice.com
კლინიცისტის მიერ ინჰალატორის მოხმარების ჩვენება, მოწყობილობის შერჩევა და გადახედვა აუმჯობესებს ინჰალატორის მოხმარების ტექნიკას.[158]Price D, Keininger DL, Viswanad B, et al. Factors associated with appropriate inhaler use in patients with COPD - lessons from the REAL survey. Int J Chron Obstruct Pulmon Dis. 2018 Feb 26;13:695-702. [Erratum in: Int J Chron Obstruct Pulmon Dis. 2018 Jul 25;13:2253-4.]
https://www.dovepress.com/factors-associated-with-appropriate-inhaler-use-in-patients-with-copd--peer-reviewed-fulltext-article-COPD
http://www.ncbi.nlm.nih.gov/pubmed/29520137?tool=bestpractice.com
ინჰალატორის სწორად მოხმარების დემონსტრირება საჩვენებელი მოწყობილობით შეიძლება ყველაზე ეფექტური იყოს ≥65 წლის პაციენტებში.[159]Maricoto T, Monteiro L, Gama JMR, et al. Inhaler technique education and exacerbation risk in older adults with asthma or chronic obstructive pulmonary disease: a meta-analysis. J Am Geriatr Soc. 2019 Jan;67(1):57-66.
http://www.ncbi.nlm.nih.gov/pubmed/30291745?tool=bestpractice.com
პაციენტებს უნდა უთხრათ მოიტანონ ინჰალატორები კლინიკაში, რათა შეაფასოთ რამდენად სწორად იყენებენ.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
ფარმაცევტის მიერ ჩატარებული ინტერვენციები და ტრენინგი ეხმარება ფქოდ-ის მქონე პაციენტს ინჰალატორის გამოყენებაში.[160]Jia X, Zhou S, Luo D, et al. Effect of pharmacist-led interventions on medication adherence and inhalation technique in adult patients with asthma or COPD: a systematic review and meta-analysis. J Clin Pharm Ther. 2020 Oct;45(5):904-17.
https://onlinelibrary.wiley.com/doi/10.1111/jcpt.13126
http://www.ncbi.nlm.nih.gov/pubmed/32107837?tool=bestpractice.com
[161]Willard-Grace R, Chirinos C, Wolf J, et al. Lay health coaching to increase appropriate inhaler use in COPD: a randomized controlled trial. Ann Fam Med. 2020 Jan;18(1):5-14.
https://www.annfammed.org/content/18/1/5
http://www.ncbi.nlm.nih.gov/pubmed/31937527?tool=bestpractice.com
ინჰალატორის მოწყობილობის ისეთი მახასიათებლები, როგორიცაა სიმპტომების სწრაფი შემსუბუქება და მცირე ზომა, კვლევებში პაციენტების მიერ უპირატეს მახასიათებლებადაა დაფიქსირებული.[162]Navaie M, Dembek C, Cho-Reyes S, et al. Inhaler device feature preferences among patients with obstructive lung diseases: a systematic review and meta-analysis. Medicine (Baltimore). 2020 Jun 19;99(25):e20718.
https://journals.lww.com/md-journal/fulltext/2020/06190/inhaler_device_feature_preferences_among_patients.56.aspx
http://www.ncbi.nlm.nih.gov/pubmed/32569208?tool=bestpractice.com
[163]Tervonen T, Hawken N, Hanania NA, et al. Maintenance inhaler therapy preferences of patients with asthma or chronic obstructive pulmonary disease: a discrete choice experiment. Thorax. 2020 Sep;75(9):735-43.
https://thorax.bmj.com/content/75/9/735
http://www.ncbi.nlm.nih.gov/pubmed/32631932?tool=bestpractice.com
მეტრირებული დოზის ინჰალატორიმთავარი ფარმაცევტი აჩვენებს პაციენტს, თუ როგორ გამოიყენოს მეტრირებული დოზის ინჰალატორი და განიხილავს ინჰალატორის ტექნიკის გაუმჯობესების გზებს.
მშრალი ფხვნილის ინჰალატორებიმთავარი ფარმაცცევტი აჩვენებს პაციენტს, თუ როგორ გამოიყენოს მშრალი ფხვნილის ხელსაწყოები და განიხილავს ინჰალატორის ტექნიკის გაუმჯობესების გზებს.
ნაზი აეროზოლის ინჰალატორიმთავარი ფარმაცევტი აჩვენებს პაციენტს, თუ როგორ გამოიყენოს ნაზი აეროზოლის ინჰალატორი და განმარტავს ინჰალატორის ტექნიკის გაუმჯობესების გზებს.
COPD-ის მქონე ყველა პაციენტისთვის რეკომენდებულია ფიზიკური აქტიობა.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
ერთი სისტემური მიმოხილვისა და რანდომიზებული კონტროლირებადი კვლევების მეტა-ანალიზის თანახმად, ვარჯიშით შესაძლებელია ფქოდ-ის დროს ფიზიკური აქტივობის გაუმჯობესება, ხოლო ვარჯიშის კონსულტაციებით კიდევ უფრო ეფექტურია შედეგი.[164]Lahham A, McDonald CF, Holland AE. Exercise training alone or with the addition of activity counseling improves physical activity levels in COPD: a systematic review and meta-analysis of randomized controlled trials. Int J Chron Obstruct Pulmon Dis. 2016 Dec 8;11:3121-36.
https://www.dovepress.com/exercise-training-alone-or-with-the-addition-of-activity-counseling-im-peer-reviewed-fulltext-article-COPD
http://www.ncbi.nlm.nih.gov/pubmed/27994451?tool=bestpractice.com
კიდევ ერთი სისტემური მიმოხილვისა და მეტა-ანალიზის თანახმად, აღმოჩნდა, რომ აერობული ვარჯიშისა და ძალისმიერი ვარჯიშის კომბინაცია უფრო ეფექტურია, ვიდრე მხოლოდ ძალისმიერი, გამძლეობის ვარჯიშები. შედეგები შეფასდა 6 წუთით სიარულისას დაფარული მანძილით.[165]Vooijs M, Siemonsma PC, Heus I, et al. Therapeutic validity and effectiveness of supervised physical exercise training on exercise capacity in patients with chronic obstructive pulmonary disease: a systematic review and meta-analysis. Clin Rehabil. 2016 Nov;30(11):1037-48.
http://www.ncbi.nlm.nih.gov/pubmed/26451006?tool=bestpractice.com
სხვა კვლევებმა აჩვენა გაუმჯობესება ჟანგბადის შეთვისების პიკური მაჩვენებლის, დაღლილობის შეგრძნების და ჯანმრთელობასთან დაკავშირებული ცხოვრების ხარისხის თვალსაზრისით, მეთვალყურეობით და მეთვალყურეობის გარეშე ჩატარებული სავარჯიშო პროგრამების შემდეგ.[166]Ward TJC, Plumptre CD, Dolmage TE, et al. Change in VO2peak in response to aerobic exercise training and the relationship with exercise prescription in people with COPD: a systematic review and meta-analysis. Chest. 2020 Jul;158(1):131-44.
http://www.ncbi.nlm.nih.gov/pubmed/32173489?tool=bestpractice.com
[167]Paneroni M, Vitacca M, Venturelli M, et al. The impact of exercise training on fatigue in patients with chronic obstructive pulmonary disease: a systematic review and meta-analysis. Pulmonology. 2020 Sep - Oct;26(5):304-13.
http://www.ncbi.nlm.nih.gov/pubmed/32184070?tool=bestpractice.com
[168]Taylor D, Jenkins AR, Parrott K, et al. Efficacy of unsupervised exercise in adults with obstructive lung disease: a systematic review and meta-analysis. Thorax. 2021 Jun;76(6):591-600.
http://www.ncbi.nlm.nih.gov/pubmed/33685962?tool=bestpractice.com
Cochrane-ის ერთი მიმოხილვით გამოვლინდა შეზღუდული მტკიცებულება ფიზიკური აქტივობის გაუმჯობესების შესახებ ფიზიკური აქტივობის კონსულტაციის, ვარჯიშის და COPD-ის ფარმაკოლოგიური მართვის პირობებში. ავტორების კომენტარის თანახმად, ხარისხის შეფასება რთული იყო მეთოდოლოგიური დეტალების სიმწირის გამო და სხვადასხვა ტიპის ჩარევები ძირითადად ერთეულ კვლევებში შეფასდა.[169]Burge AT, Cox NS, Abramson MJ, et al. Interventions for promoting physical activity in people with chronic obstructive pulmonary disease (COPD). Cochrane Database Syst Rev. 2020 Apr 16;(4):CD012626.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD012626.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/32297320?tool=bestpractice.com
[  ]
Which interventions lead to increased regular physical activity for people with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.3155/fullShow me the answer ფიზიკური აქტივობის გაუმჯობესების ოპტიმალური დრო, კომპონენტები, ხანგრძლივობა და მოდელები გაურკვეველი რჩება. მეტა-ანალიზის მონაცემებით იოგას, ციგუნის და სახლის პირობებში ჩატარებულ სხვა სუნთქვის ვარჯიშებს შეუძლიათ გააუმჯობესონ ფიზიკური შესაძლებლობები და ფილტვის ფუნქცია COPD-ის მქონე პაციენტებში.[170]Cramer H, Haller H, Klose P, et al. The risks and benefits of yoga for patients with chronic obstructive pulmonary disease: a systematic review and meta-analysis. Clin Rehabil. 2019 Dec;33(12):1847-62.
http://www.ncbi.nlm.nih.gov/pubmed/31353959?tool=bestpractice.com
[171]Tong H, Liu Y, Zhu Y, et al. The therapeutic effects of qigong in patients with chronic obstructive pulmonary disease in the stable stage: a meta-analysis. BMC Complement Altern Med. 2019 Sep 4;19(1):239.
https://bmccomplementmedtherapies.biomedcentral.com/articles/10.1186/s12906-019-2639-9
http://www.ncbi.nlm.nih.gov/pubmed/31484521?tool=bestpractice.com
[172]Lu Y, Li P, Li N, et al. Effects of home-based breathing exercises in subjects with COPD. Respir Care. 2020 Mar;65(3):377-87.
https://rc.rcjournal.com/content/65/3/377
http://www.ncbi.nlm.nih.gov/pubmed/31719191?tool=bestpractice.com
ტაი ჩი აუმჯობესებს ფიზიკურ შესაძლებლობას პაციენტის სტანდარტულ მოვლასთან შედარებით.[173]Liu X, Fu C, Hu W, et al. The effect of Tai Chi on the pulmonary rehabilitation of chronic obstructive pulmonary disease: a systematic review and meta-analysis. Ann Palliat Med. 2021 Apr;10(4):3763-82.
https://apm.amegroups.org/article/view/67333/html
http://www.ncbi.nlm.nih.gov/pubmed/33894710?tool=bestpractice.com
]
Which interventions lead to increased regular physical activity for people with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.3155/fullShow me the answer ფიზიკური აქტივობის გაუმჯობესების ოპტიმალური დრო, კომპონენტები, ხანგრძლივობა და მოდელები გაურკვეველი რჩება. მეტა-ანალიზის მონაცემებით იოგას, ციგუნის და სახლის პირობებში ჩატარებულ სხვა სუნთქვის ვარჯიშებს შეუძლიათ გააუმჯობესონ ფიზიკური შესაძლებლობები და ფილტვის ფუნქცია COPD-ის მქონე პაციენტებში.[170]Cramer H, Haller H, Klose P, et al. The risks and benefits of yoga for patients with chronic obstructive pulmonary disease: a systematic review and meta-analysis. Clin Rehabil. 2019 Dec;33(12):1847-62.
http://www.ncbi.nlm.nih.gov/pubmed/31353959?tool=bestpractice.com
[171]Tong H, Liu Y, Zhu Y, et al. The therapeutic effects of qigong in patients with chronic obstructive pulmonary disease in the stable stage: a meta-analysis. BMC Complement Altern Med. 2019 Sep 4;19(1):239.
https://bmccomplementmedtherapies.biomedcentral.com/articles/10.1186/s12906-019-2639-9
http://www.ncbi.nlm.nih.gov/pubmed/31484521?tool=bestpractice.com
[172]Lu Y, Li P, Li N, et al. Effects of home-based breathing exercises in subjects with COPD. Respir Care. 2020 Mar;65(3):377-87.
https://rc.rcjournal.com/content/65/3/377
http://www.ncbi.nlm.nih.gov/pubmed/31719191?tool=bestpractice.com
ტაი ჩი აუმჯობესებს ფიზიკურ შესაძლებლობას პაციენტის სტანდარტულ მოვლასთან შედარებით.[173]Liu X, Fu C, Hu W, et al. The effect of Tai Chi on the pulmonary rehabilitation of chronic obstructive pulmonary disease: a systematic review and meta-analysis. Ann Palliat Med. 2021 Apr;10(4):3763-82.
https://apm.amegroups.org/article/view/67333/html
http://www.ncbi.nlm.nih.gov/pubmed/33894710?tool=bestpractice.com
დადგინდა, რომ დიეტა და პერორალური დანამატები აუმჯობესებს პაციენტის სხეულის წონას, ცხოვრების ხარისხს, რესპირატორული კუნთების სიძლიერეს და 6 წუთიანი სიარულის ტესტის დისტაციას.[174]Collins PF, Elia M, Stratton RJ. Nutritional support and functional capacity in chronic obstructive pulmonary disease: a systematic review and meta-analysis. Respirology. 2013 May;18(4):616-29.
https://onlinelibrary.wiley.com/doi/10.1111/resp.12070
http://www.ncbi.nlm.nih.gov/pubmed/23432923?tool=bestpractice.com
[175]Ferreira IM, Brooks D, White J, et al. Nutritional supplementation for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2012 Dec 12;(12):CD000998.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD000998.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/23235577?tool=bestpractice.com
თუმცა ვერ დადგინდა, რომ ნუტრიციული მხარდაჭერა აუმჯობესებს ფილტვის ფუნქციას.[175]Ferreira IM, Brooks D, White J, et al. Nutritional supplementation for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2012 Dec 12;(12):CD000998.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD000998.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/23235577?tool=bestpractice.com
მოწევისთვის თავის დანებება
მოწევის შეწყვეტისკენ უნდა მოვუწოდოთ ყველა პაციენტს. ასევე მათ უნდა მიეცეთ მითითება, რომ აირიდონ თავიდან თამბაქოს კვამლით, ოკუპაციური ან ექსპოზიცია სხვა გამღიზიანებლებთან.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
[2]National Institute for Health and Care Excellence. Chronic obstructive pulmonary disease in over 16s: diagnosis and management. Jul 2019 [internet publication].
https://www.nice.org.uk/guidance/ng115
მოწევის შეწყვეტა მნიშვნელოვნად ამცირებს ფქოდ-ის პროგრესირების მაჩვენებელსა და მალიგნიზაციის რისკს. ის ასევე ამცირებს კორონარული და ცერებროვასკულური დაავადებების რისკს. ფქოდ-ის დროს სხვადასხვა თერაპიულ საშუალებებს შორის გადარჩენადობის გაუმჯობესებაზე მხოლოდ ორი ფაქტორი მოქმედებს: მოწევის შეწყვეტა და ხელოვნური ჟანგბადით მომარაგება.
მოწევის შეწყვეტის პროგრამა მოიცავს კონსულტაციებს, მედიკამენტების გამოყენებას და ჯგუფურ შეხვედრებს.[176]Gonzales D, Rennard SI, Nides M, et al; Varenicline Phase 3 Study Group. Varenicline, an alpha4beta2 nicotinic acetylcholine receptor partial agonist, vs sustained-release bupropion and placebo for smoking cessation: a randomized controlled trial. JAMA. 2006 Jul 5;296(1):47-55.
https://jamanetwork.com/journals/jama/fullarticle/211000
http://www.ncbi.nlm.nih.gov/pubmed/16820546?tool=bestpractice.com
ზოგიერთი პაციენტი საჭიროებს ხშირ მიმართვას წარმათების მიღწევამდე. მოწევის შეწყვეტის პროგრამას, რომელიც მოიცავს ფარმაკოთერაპიასა და ინტენსიურ კონსულტაციებს,COPD-ის შემთხვევაში აქვს წარმატების მეტი შანსი და არის ხარჯთეფექტური, ცხოვრების ხარისხზე ორიენტირებულ ყოველწლიურ ხარჯთან მიმართებაში.[177]Hoogendoorn M, Feenstra TL, Hoogenveen RT, et al. Long-term effectiveness and cost-effectiveness of smoking cessation interventions in patients with COPD. Thorax. 2010 Aug;65(8):711-8.
http://www.ncbi.nlm.nih.gov/pubmed/20685746?tool=bestpractice.com
[178]Warnier MJ, van Riet EE, Rutten FH, et al. Smoking cessation strategies in patients with COPD. Eur Respir J. 2013 Mar;41(3):727-34.
http://www.ncbi.nlm.nih.gov/pubmed/22936706?tool=bestpractice.com
[179]van Eerd EA, van der Meer RM, van Schayck OC, et al. Smoking cessation for people with chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2016 Aug 20;(8):CD010744.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD010744.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/27545342?tool=bestpractice.com
ნიკოტინის მიწოდების ელექტრონული სისტემების (ENDS), მათ შორის ელექტრონული სიგარეტის და აორთქლებადი პროდუქტების, როგორც თამბაქოს შეწყვეტის საშუალებების გამოყენება ურთიერთგამომრიცხავია. ობსერვაციული კვლევების მტკიცებულებებით ამჟამად არ დასტურდება, რომ ENDS-ი მოწევაზე თავის დანებების საშუალებად უნდა იყოს გამოყენებული COPD-ით დაავადებულ ადამიანებში.[180]Bowler RP, Hansel NN, Jacobson S, et al; for COPDGene and SPIROMICS Investigators. Electronic cigarette use in US adults at risk for or with COPD: analysis from two observational cohorts. J Gen Intern Med. 2017 Dec;32(12):1315-22.
https://link.springer.com/article/10.1007/s11606-017-4150-7
http://www.ncbi.nlm.nih.gov/pubmed/28884423?tool=bestpractice.com
იხილეთ მოწევის შეწყვეტა (მართვის მიდგომა).
ვაქცინაცია
ადგილობრივი გაიდლაინებიდან გამომდინარე, პაციენტებს უნდა ჩაუტარდეთ ვაქცინაცია გრიპის ვირუსის, Streptococcus pneumoniae, ყივანახველას, ვარიცელა-ზოსტერის ვირუსის (სირსველის), რესპირატორულ-სინციტიური ვირუსის (RSV) და კორონავირუსის (COVID-19) წინააღმდეგ.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
[181]Centers for Disease Control and Prevention. Recommended vaccines for adults: lung disease (including asthma and COPD). Sep 2023 [internet publication].
https://www.cdc.gov/vaccines/adults/rec-vac/health-conditions/lung-disease.html
გრიპის საწინააღმდეგო ვაქცინაცია ასოცირდება COPD-ის ცხელებით მიმდინარე გამწვავებასთან.[182]Walters JA, Tang JN, Poole P, et al. Pneumococcal vaccines for preventing pneumonia in chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2017 Jan 24;(1):CD001390.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001390.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/28116747?tool=bestpractice.com
[183]Kopsaftis Z, Wood-Baker R, Poole P. Influenza vaccine for chronic obstructive pulmonary disease (COPD). Cochrane Database Syst Rev. 2018 Jun 26;(6):CD002733.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD002733.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/29943802?tool=bestpractice.com
[  ]
What are the effects of influenza vaccine in people with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.2235/fullShow me the answer აშშ-ს დაავადებათა კონტროლისა და პრევენციის ცენტრი (CDC) გვთავაზობს პნევმოკოკური 15-ვალენტიანი (PCV15) ან 20-ვალენტიანი PCV (PCV20) ვაქცინის ერთჯერადი დოზის მიღებას COPD-ით დაავადებული ყველა პაციენტისთვის, რომლებსაც ადრე არ მიუღიათ PCV ან ვისი ვაქცინაციის ისტორია უცნობია. პაციენტმა, რომელსაც PCV15-ით ვაქცინაცია ჩაუტარდა, 23-ვალენტიანი პოლისაქარიდის ვაქცინის (PPSV23) ერთჯერადი დოზა უნდა მიიღოს სულ მცირე 1 წლის შემდეგ.[184]Centers for Disease Control and Prevention. Adult immunization schedule by age: recommendations for ages 19 years or older, United States, 2024. Nov 2023 [internet publication].
https://www.cdc.gov/vaccines/schedules/hcp/imz/adult.html
]
What are the effects of influenza vaccine in people with chronic obstructive pulmonary disease (COPD)?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.2235/fullShow me the answer აშშ-ს დაავადებათა კონტროლისა და პრევენციის ცენტრი (CDC) გვთავაზობს პნევმოკოკური 15-ვალენტიანი (PCV15) ან 20-ვალენტიანი PCV (PCV20) ვაქცინის ერთჯერადი დოზის მიღებას COPD-ით დაავადებული ყველა პაციენტისთვის, რომლებსაც ადრე არ მიუღიათ PCV ან ვისი ვაქცინაციის ისტორია უცნობია. პაციენტმა, რომელსაც PCV15-ით ვაქცინაცია ჩაუტარდა, 23-ვალენტიანი პოლისაქარიდის ვაქცინის (PPSV23) ერთჯერადი დოზა უნდა მიიღოს სულ მცირე 1 წლის შემდეგ.[184]Centers for Disease Control and Prevention. Adult immunization schedule by age: recommendations for ages 19 years or older, United States, 2024. Nov 2023 [internet publication].
https://www.cdc.gov/vaccines/schedules/hcp/imz/adult.html
CDC რეკომენდაციას უწევს RSV ვაქცინას COPD-ის მქონე ≥60 წლის და/ან ფილტვების ან გულის ქრონიკული დაავადების მქონე პაციენტებისთვის.[185]Melgar M, Britton A, Roper LE, et al. Use of respiratory syncytial virus vaccines in older adults: recommendations of the Advisory Committee on Immunization Practices - United States, 2023. MMWR Morb Mortal Wkly Rep. 2023 Jul 21;72(29):793-801.
https://www.cdc.gov/mmwr/volumes/72/wr/mm7229a4.htm
http://www.ncbi.nlm.nih.gov/pubmed/37471262?tool=bestpractice.com
CDC ასევე რეკომენდაციას უწევს ტეტანუსის/ დიფტერიის/ყივანახველას ვაქცინას COPD-ით დაავადებულ ადამიანებში, რომლებიც არ იყვნენ ვაქცინირებული მოზარდობისას.[181]Centers for Disease Control and Prevention. Recommended vaccines for adults: lung disease (including asthma and COPD). Sep 2023 [internet publication].
https://www.cdc.gov/vaccines/adults/rec-vac/health-conditions/lung-disease.html
მუკოლიზური საშუალებები
COPD-ის ქრონიკული ბრონქიტით მიმდინარე ფორმის დროს ხშირია სქელი ნახველის პროდუქცია. მიკოლიზური პრეპარატები არ უკავშირდება გვერდითი მოვლენების მატებასთან და შეიძლება სარგებლიანი იყოს დანიშვნ ფქოდის-ის გამწვავების დროს.
[  ]
For people with chronic bronchitis or chronic obstructive pulmonary disease, how do mucolytic agents compare with placebo?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2591/fullShow me the answer შეიძლება მცირედ შეამციროს გამწვავებების სიხშირე და თვის განმავლობაში უნარშეზღუდული დღეების ჯამური რაოდენობა, მაგრამ არ აუმჯობესებს ფილტვის ფუნქციასა და ცხოვრების ხარისხს.[186]Poole P, Sathananthan K, Fortescue R. Mucolytic agents versus placebo for chronic bronchitis or chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2019 May 20;(5):CD001287.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001287.pub6/full
http://www.ncbi.nlm.nih.gov/pubmed/31107966?tool=bestpractice.com
ერთი მეტა-ანალიზის მიხედვით, რომლითაც შედარდა ერდოსტეინი, კარბოცისტეინი და აცეტილცისტეინი, ერდოსტეინს აღმოაჩნდა ყველაზე უსაფრთხო და ეფექტური პროფილი. ერდოსტეინი ამცირებს გამწვავების მიზეზით ჰოსპიტალიზაციის რისკს. ერდოსტეინი და აცეტილცისტეინი ამცირებს გამწვავების ხანგრძლივობას.[187]Rogliani P, Matera MG, Page C, et al. Efficacy and safety profile of mucolytic/antioxidant agents in chronic obstructive pulmonary disease: a comparative analysis across erdosteine, carbocysteine, and N-acetylcysteine. Respir Res. 2019 May 27;20(1):104.
https://respiratory-research.biomedcentral.com/articles/10.1186/s12931-019-1078-y
http://www.ncbi.nlm.nih.gov/pubmed/31133026?tool=bestpractice.com
სხვა მეტა-ანალიზმა აჩვენა, რომ აცეტილცისტეინმა მნიშვნელოვნად შეამცირა გამწვავებების სიხშირე პლაცებოსთან შედარებით, გვერდითი მოვლენების რისკის გაზრდის გარეშე. ავტორებმა დაასკვნეს, რომ 3 თვიანი მკურნალობა დაბალი დოზით ეფექტური იყო.[188]Wei J, Pang CS, Han J, et al. Effect of orally administered N-acetylcysteine on chronic bronchitis: a meta-analysis. Adv Ther. 2019 Dec;36(12):3356-67.
http://www.ncbi.nlm.nih.gov/pubmed/31598901?tool=bestpractice.com
ერდოსტეინი და კარბოცისტეინი არ არის ხელმისაწვდომი აშშ-ში და რამდენიმე სხვა ქვეყანაში. მუკოლიზური საშუალებებით მკურნალობამ, როგორიცაა კარბოცისტეინი და აცეტილცისტეინი, შეიძლება შეამციროს გამწვავებები და ზომიერად გააუმჯობესოს ჯანმრთელობის მდგომარეობა პაციენტებში, რომლებიც არ იღებენ ICS.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
თუმცა, ერდოსტეინს შეუძლია მნიშვნელოვანი გავლენა მოახდინოს მსუბუქ გამწვავებებზე, მიუხედავად იმისა, პაციენტი იღებს თუ არა ICS.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
]
For people with chronic bronchitis or chronic obstructive pulmonary disease, how do mucolytic agents compare with placebo?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2591/fullShow me the answer შეიძლება მცირედ შეამციროს გამწვავებების სიხშირე და თვის განმავლობაში უნარშეზღუდული დღეების ჯამური რაოდენობა, მაგრამ არ აუმჯობესებს ფილტვის ფუნქციასა და ცხოვრების ხარისხს.[186]Poole P, Sathananthan K, Fortescue R. Mucolytic agents versus placebo for chronic bronchitis or chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2019 May 20;(5):CD001287.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001287.pub6/full
http://www.ncbi.nlm.nih.gov/pubmed/31107966?tool=bestpractice.com
ერთი მეტა-ანალიზის მიხედვით, რომლითაც შედარდა ერდოსტეინი, კარბოცისტეინი და აცეტილცისტეინი, ერდოსტეინს აღმოაჩნდა ყველაზე უსაფრთხო და ეფექტური პროფილი. ერდოსტეინი ამცირებს გამწვავების მიზეზით ჰოსპიტალიზაციის რისკს. ერდოსტეინი და აცეტილცისტეინი ამცირებს გამწვავების ხანგრძლივობას.[187]Rogliani P, Matera MG, Page C, et al. Efficacy and safety profile of mucolytic/antioxidant agents in chronic obstructive pulmonary disease: a comparative analysis across erdosteine, carbocysteine, and N-acetylcysteine. Respir Res. 2019 May 27;20(1):104.
https://respiratory-research.biomedcentral.com/articles/10.1186/s12931-019-1078-y
http://www.ncbi.nlm.nih.gov/pubmed/31133026?tool=bestpractice.com
სხვა მეტა-ანალიზმა აჩვენა, რომ აცეტილცისტეინმა მნიშვნელოვნად შეამცირა გამწვავებების სიხშირე პლაცებოსთან შედარებით, გვერდითი მოვლენების რისკის გაზრდის გარეშე. ავტორებმა დაასკვნეს, რომ 3 თვიანი მკურნალობა დაბალი დოზით ეფექტური იყო.[188]Wei J, Pang CS, Han J, et al. Effect of orally administered N-acetylcysteine on chronic bronchitis: a meta-analysis. Adv Ther. 2019 Dec;36(12):3356-67.
http://www.ncbi.nlm.nih.gov/pubmed/31598901?tool=bestpractice.com
ერდოსტეინი და კარბოცისტეინი არ არის ხელმისაწვდომი აშშ-ში და რამდენიმე სხვა ქვეყანაში. მუკოლიზური საშუალებებით მკურნალობამ, როგორიცაა კარბოცისტეინი და აცეტილცისტეინი, შეიძლება შეამციროს გამწვავებები და ზომიერად გააუმჯობესოს ჯანმრთელობის მდგომარეობა პაციენტებში, რომლებიც არ იღებენ ICS.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
თუმცა, ერდოსტეინს შეუძლია მნიშვნელოვანი გავლენა მოახდინოს მსუბუქ გამწვავებებზე, მიუხედავად იმისა, პაციენტი იღებს თუ არა ICS.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
პულმონალური რეაბილიტაცია
ფილტვის რეაბილიტაცია მოიცავს ვარჯიშს და განათლებას. ის უნდა ჩაუტარდეს პაციენტებს, რომლებიც სიმპტომურნი რჩებიან, მიუხედავად ბრონქოდილატატორების გამოყენებისა და რეკომენდებულია დაიწყოს დაავადების ადრეულ ეტაპზე, როგორც კი პაციენტი რუტინული აქტივობისას და სწორ ზედაპირზე სიარულისას სუნთქვის გაძნელებას იგრძნობს.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
[189]Rochester CL, Alison JA, Carlin B, et al. Pulmonary rehabilitation for adults with chronic respiratory disease: an official American Thoracic Society clinical practice guideline. Am J Respir Crit Care Med. 2023 Aug 15;208(4):e7-26.
https://www.atsjournals.org/doi/10.1164/rccm.202306-1066ST
http://www.ncbi.nlm.nih.gov/pubmed/37581410?tool=bestpractice.com
[190]Man W, Chaplin E, Daynes E, et al. British Thoracic Society Clinical Statement on pulmonary rehabilitation. Thorax. 2023 Oct;78(suppl 5):s2-15.
https://thorax.bmj.com/content/78/Suppl_5/s2
http://www.ncbi.nlm.nih.gov/pubmed/37770084?tool=bestpractice.com
GOLD გაიდლაინები რეკომენდაციას უწევს ფილტვების რეაბილიტაციას პაციენტებისთვის, რომლებსაც სიმპტომების მხრივ აქვთ მაღალი ტვირთი და გამწვავების რისკი (ანუ ჯგუფები B და E).[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
ფილტვის რეაბილიტაცია ხსნის დისპნოეს და დაღლილობას, აუმჯობესებს ემოციურ ფონს და იწვევს კონტროლის შეგრძნებას შედარებით ფართო და კლინიკურად მნიშვნელოვანი ეფექტით.[191]McCarthy B, Casey D, Devane D, et al. Pulmonary rehabilitation for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2015 Feb 23;(2):CD003793.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD003793.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/25705944?tool=bestpractice.com
ფილტვების ექსტენსიური რეაბილიტაცია COPD-ის მწვავე გამწვავების შემთხვევაში ჰოსპიტალიზაციის შემდეგ ამცირებს ხელახალი ჰოსპიტალიზაციის რისკს, აუმჯობესებს ჯანმრთელობასთან დაკავშირებულ ცხოვრების ხარისხს და ამცირებს სიკვდილიანობას.
[  ]
What are the effects of pulmonary rehabilitation after exacerbation in people with chronic obstructive pulmonary disease?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1650/fullShow me the answer არსებობს მტკიცებულებები, რომლთა მიხედვითაც პულმონური რეაბილიტაცია უნდა დაიწყოს გამწვავების დაწყებიდან 1 თვის განმავლობაში.[192]Marciniuk DD, Brooks D, Butcher S, et al. Canadian Thoracic Society COPD Committee Expert Working Group. Optimizing pulmonary rehabilitation in chronic obstructive pulmonary disease - practical issues: a Canadian Thoracic Society Clinical Practice Guideline. Can Respir J. 2010 Jul-Aug;17(4):159-68.
http://www.ncbi.nlm.nih.gov/pubmed/20808973?tool=bestpractice.com
[193]Puhan MA, Gimeno-Santos E, Cates CJ, et al. Pulmonary rehabilitation following exacerbations of chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2016 Dec 8;(12):CD005305.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD005305.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/27930803?tool=bestpractice.com
]
What are the effects of pulmonary rehabilitation after exacerbation in people with chronic obstructive pulmonary disease?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1650/fullShow me the answer არსებობს მტკიცებულებები, რომლთა მიხედვითაც პულმონური რეაბილიტაცია უნდა დაიწყოს გამწვავების დაწყებიდან 1 თვის განმავლობაში.[192]Marciniuk DD, Brooks D, Butcher S, et al. Canadian Thoracic Society COPD Committee Expert Working Group. Optimizing pulmonary rehabilitation in chronic obstructive pulmonary disease - practical issues: a Canadian Thoracic Society Clinical Practice Guideline. Can Respir J. 2010 Jul-Aug;17(4):159-68.
http://www.ncbi.nlm.nih.gov/pubmed/20808973?tool=bestpractice.com
[193]Puhan MA, Gimeno-Santos E, Cates CJ, et al. Pulmonary rehabilitation following exacerbations of chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2016 Dec 8;(12):CD005305.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD005305.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/27930803?tool=bestpractice.com
აშშ-ში ჩატარებულმა დიდმა კოჰორტულმა კვლევამ აჩვენა, რომ კლინიკიდან გაწერის შემდეგ 90 დღის განმავლობაში ფილტვის რეაბილიტაციის დაწყება სარწმუნოდ ასოცირდება სიკვდილიანობის დაბალ რისკთან 1 წლის განმავლობაში და ნაკლებ განმეორებით ჰოსპიტალიზაციასთან 1 წლის განმავლობაში.[194]Lindenauer PK, Stefan MS, Pekow PS, et al. Association between initiation of pulmonary rehabilitation after hospitalization for COPD and 1-year survival among medicare beneficiaries. JAMA. 2020 May 12;323(18):1813-23.
https://jamanetwork.com/journals/jama/fullarticle/2765730
http://www.ncbi.nlm.nih.gov/pubmed/32396181?tool=bestpractice.com
[195]Stefan MS, Pekow PS, Priya A, et al. Association between initiation of pulmonary rehabilitation and rehospitalizations in patients hospitalized with chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2021 Nov 1;204(9):1015-23.
https://www.atsjournals.org/doi/10.1164/rccm.202012-4389OC
http://www.ncbi.nlm.nih.gov/pubmed/34283694?tool=bestpractice.com
პაციენტების კოჰორტის 2%-ზე ნაკლებმა დაიწყო რეაბილიტაცია ამ ვადებში, რაც ხაზს უსვამს უფრო ეფექტური სტრატეგიების შემუშავების აუცილებლობას პაციენტის მონაწილეობის წასახალისებლად.[194]Lindenauer PK, Stefan MS, Pekow PS, et al. Association between initiation of pulmonary rehabilitation after hospitalization for COPD and 1-year survival among medicare beneficiaries. JAMA. 2020 May 12;323(18):1813-23.
https://jamanetwork.com/journals/jama/fullarticle/2765730
http://www.ncbi.nlm.nih.gov/pubmed/32396181?tool=bestpractice.com
ამასთანავე, საავადმყოფოდან გაწერამდე ფილტვის რეაბილიტაციის დაწყება შეიძლება 12 თვის განმავლობაში უფრო მაღალ სიკვდილიანობასთან ასოცირდებოდეს, ამიტომაც არ არის რეკომენდებული.[196]Greening NJ, Williams JE, Hussain SF, et al. An early rehabilitation intervention to enhance recovery during hospital admission for an exacerbation of chronic respiratory disease: randomised controlled trial. BMJ. 2014 Jul 8;349:g4315.
https://www.bmj.com/content/349/bmj.g4315
http://www.ncbi.nlm.nih.gov/pubmed/25004917?tool=bestpractice.com
ფილტვის რეაბილიტაცია ასევე ამცირებს COPD-თან დაკავშირებულ დეპრესიას და შფოთვას, და ამცირებს ჰოსპიტალიზაციას.[197]Casaburi R, ZuWallack R. Pulmonary rehabilitation for management of chronic obstructive pulmonary disease. N Engl J Med. 2009 Mar 26;360(13):1329-35.
http://www.ncbi.nlm.nih.gov/pubmed/19321869?tool=bestpractice.com
როგორც ჩანს, ფილტვების რეაბილიტაციის სარგებელი მცირდება კურსის შეწყვეტის შემდეგ, თუ პაციენტები არ დაიცავენ სახლში ვარჯიშის გრაფიკს.[198]Guell R, Casan P, Belda J, et al. Long-term effects of outpatient rehabilitation of COPD: a randomized trial. Chest. 2000 Apr;117(4):976-83.
http://www.ncbi.nlm.nih.gov/pubmed/10767227?tool=bestpractice.com
შემანარჩუნებელი ფილტვის რეაბილიტაციას, რომელიც განისაზღვრება, როგორც მიმდინარე მეთვალყურეობის ქვეშ ვარჯიში უფრო დაბალი სიხშირით, ვიდრე თავდაპირველი სარეაბილიტაციო პროგრამა, შეიძლება ჰქონდეს როლი დროთა განმავლობაში ფილტვის რეაბილიტაციის სარგებელის შენარჩუნებაში. Cochrane-ის ერთი მიმოხილვის დასკვნით, ზედამხედველობის ქვეშ ჩატარებულმა შემანარჩუნებელმა პროგრამებმა შეიძლება გააუმჯობესოს ჯანმრთელობასთან დაკავშირებული ცხოვრების ხარისხი და ფიზიკური დატვირთვის უნარი 6-12 თვით, სტანდარტულ მოვლასთან შედარებით.[199]Malaguti C, Dal Corso S, Janjua S, et al. Supervised maintenance programmes following pulmonary rehabilitation compared to usual care for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2021 Aug 17;(8):CD013569.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD013569.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/34404111?tool=bestpractice.com
[  ]
For people with chronic obstructive pulmonary disease (COPD), what are the effects of a supervised maintenance program after pulmonary rehabilitation?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4228/fullShow me the answer
]
For people with chronic obstructive pulmonary disease (COPD), what are the effects of a supervised maintenance program after pulmonary rehabilitation?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.4228/fullShow me the answer
სახლში ან თემში ჩატარებული ფილტვის რეაბილიტაციის სარგებელი რესპირატორული სიმპტომებსა და ცხოვრების ხარისხზე COPD-ის მქონე პაციენტებში შეიძლება შეესაბამებოდეს კლინიკაში განხორციელებულ სარეაბილიტაციო პროგრამებს.[200]Maltais F, Bourbeau J, Shapiro S, et al. Effects of home-based pulmonary rehabilitation in patients with chronic obstructive pulmonary disease: a randomized trial. Ann Intern Med. 2008 Dec 16;149(12):869-78.
http://www.ncbi.nlm.nih.gov/pubmed/19075206?tool=bestpractice.com
[201]Neves LF, Reis MH, Gonçalves TR. Home or community-based pulmonary rehabilitation for individuals with chronic obstructive pulmonary disease: a systematic review and meta-analysis. Cad Saude Publica. 2016 Jun 20;32(6):S0102-311X2016000602001.
http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0102-311X2016000602001&lng=en&nrm=iso&tlng=en
http://www.ncbi.nlm.nih.gov/pubmed/27333130?tool=bestpractice.com
[202]Holland AE, Mahal A, Hill CJ, et al. Home-based rehabilitation for COPD using minimal resources: a randomised, controlled equivalence trial. Thorax. 2017 Jan;72(1):57-65.
https://thorax.bmj.com/content/72/1/57
http://www.ncbi.nlm.nih.gov/pubmed/27672116?tool=bestpractice.com
Cochrane-ის ერთ-ერთმა მიმოხილვამ დაასკვნა, რომ პირველადი და შემანარჩუნებელი ტელერეაბილიტაცია იდენტურ შედეგებს აღწევს პირის რეაბილიტაციის პროცესში, უსაფრთხოების პრობლემების გარეშე. მიმოხილვის ლიმიტაცია მდგომარეობს პაციენტთა მცირე რაოდენობასა და ტელერეაბილიტაციის მოდელების ჰეტეროგენობაში.[203]Cox NS, Dal Corso S, Hansen H, et al. Telerehabilitation for chronic respiratory disease. Cochrane Database Syst Rev. 2021 Jan 29;(1):CD013040.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD013040.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/33511633?tool=bestpractice.com
ოქსიგენოთერაპია და ვენტილაცია
GOLD გაიდლაინებით ხანგრძლივი ოქსიგენოთერაპია რეკომენდებულია სტაბილურ პაციენტებში, რომელთაც აქვთ:[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
PaO₂ ≤7.3 კპა (55 მმ.ვწყ.სვ.) ან SaO₂ ≤88%, ჰიპერკაპნიით ან მის გარეშე, დასტურდება ორჯერ 3 კვირის განმავლობაში; ან
PaO₂ მერყეობს 7.3 კპა (55 მმ.ვწყ.სვ.) და 8.0 კპა (60 მმ.ვწყ.სვ.) შორის, ან SaO₂ =88%, თუ ვლინდება ფილტვის ჰიპერტენზიის, პერიფერიული ედემის ნიშნები (გულის შეგუბებითი უკმარისობა) ან პოლიციტემია (ჰემატოკრიტი > 55%).
ამერიკის თორაკალური საზოგადოების გაიდლაინების მიხედვით, ფქოდ-ით დაავადებულ ზრდასრულებში, რომელთაც ოთახის ჰაერზე აქვთ მძიმე ქრონიკული ჰიპოქსემია, რეკომენდებულია ხანგრძლივი ოქსიგენოთერაპია სულ მცირე 15 საათი დღეში. საზოგადოება მძიმე ჰიპოქსემიას განმარტავს, როგორც:[204]Jacobs SS, Krishnan JA, Lederer DJ, et al. Home oxygen therapy for adults with chronic lung disease. An official American Thoracic Society clinical practice guideline. Am J Respir Crit Care Med. 2020 Nov 15;202(10):e121-41. [Erratum in: Am J Respir Crit Care Med. 2021 Apr 15;203(8):1045-6.]
https://www.atsjournals.org/doi/10.1164/rccm.202009-3608ST
http://www.ncbi.nlm.nih.gov/pubmed/33185464?tool=bestpractice.com
PaO₂ ≤7.3 კპა (55 მმ.ვწყ.სვ.) ან ჟანგბადის სატურაცია პულსოქსიმეტრიით (SpO₂) ≤88%; ან
PaO2 7.5-დან 7.9 kPa-მდე (56-59 mmHg) ან SpO2 89% პლუს ერთ-ერთი შემდეგი: შეშუპება, ჰემატოკრიტი ≥55%, ან მაღალი P კბილი ეკგ-ზე.
პაციენტებისთვის, რომლებსაც უნიშნავენ სახლში ჟანგბადით თერაპიას, ATS რეკომენდაციას უწევს, რომ პაციენტმა და მათმა მომვლელებმა მიიღონ ინსტრუქციები და გაიარონ ტრენინგები ჟანგბადის აღჭურვილობის გამოყენებისა და მოვლის შესახებ და განათლება ჟანგბადის უსაფრთხოების შესახებ, მათ შორის მოწევის შეწყვეტის, ხანძრის პრევენციისა და დაზიანების საფრთხეების შესახებ.[204]Jacobs SS, Krishnan JA, Lederer DJ, et al. Home oxygen therapy for adults with chronic lung disease. An official American Thoracic Society clinical practice guideline. Am J Respir Crit Care Med. 2020 Nov 15;202(10):e121-41. [Erratum in: Am J Respir Crit Care Med. 2021 Apr 15;203(8):1045-6.]
https://www.atsjournals.org/doi/10.1164/rccm.202009-3608ST
http://www.ncbi.nlm.nih.gov/pubmed/33185464?tool=bestpractice.com
დამატებითი ჟანგბადის ტიტრირება საჭიროა SaO2 ≥90% მაჩვენებლის მისაღწევად.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
60-90 დღის შემდეგ პაციენტი ხელახლა უნდა შეფასდეს, რათა განისაზღვროს ჟანგბადის საჭიროება და თერაპიული ეფექტი.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
ფქოდის დროს სხვადასხვა თერაპიულ საშუალებებს შორის გადარჩენადობის გაუმჯობესებაზე მხოლოდ ორი ფაქტორი მოქმედებს: მოწევის შეწყვეტა და ხელოვნური ჟანგბადით მომარაგება.
ოქსიგენოთერაპია გვეხმარება ფილტვის ჰიპერტენზიის მინიმალიზაციაში, პულმონური არტერიული წნევის შემცირების გზით და აუმჯობესებს ფიზიკური დატვირთვის მიმართ ტოლერანტობასა და ცხოვრების ხარისხს. ასევე მან აჩვენა გაუმჯობესებული გადარჩენადობა.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
[61]Qaseem A, Wilt TJ, Weinberger SE, et al. Diagnosis and management of stable chronic obstructive pulmonary disease: a clinical practice guideline update from the American College of Physicians, American College of Chest Physicians, American Thoracic Society, and European Respiratory Society. Ann Intern Med. 2011 Aug 2;155(3):179-91.
https://www.acpjournals.org/doi/10.7326/0003-4819-155-3-201108020-00008
http://www.ncbi.nlm.nih.gov/pubmed/21810710?tool=bestpractice.com
არსებობს გარკვეული მტკიცებულება, რომ ფქოდ-ის დროს ჟანგბადის ფონზე სუნთქვის უკმარისობა ვარჯიშის დროს მცირდება მსუბუქი ჰიპოქსიის და არაჰიპოქსემიურ პირებში, თუ სხვამხრივ სახლის პირობებში ჟანგბადის თერაპიის კრიტერიუმები არ კმაყოფილდება.[205]Ekström M, Ahmadi Z, Bornefalk-Hermansson A, et al. Oxygen for breathlessness in patients with chronic obstructive pulmonary disease who do not qualify for home oxygen therapy. Cochrane Database Syst Rev. 2016 Nov 25;(11):CD006429.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD006429.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/27886372?tool=bestpractice.com
ამერიკის თორაკალური საზოგადოება რეკომენდაციას უწევს ამბულატორიულად ჟანგბადის მოხმარებას (ჟანგბადი მიეწოდება ვარჯიშის დროს ან ყოველდღიური აქტივობების დროს) იმ ზრდასრულებში, რომელთაც დიაგნოსტირებული აქვთ ფქოდ-ი და ატმოსფერულ ჰაერზე აღენიშნბთ მძიმე ჰიპოქსემია აღენიშნებათ.[204]Jacobs SS, Krishnan JA, Lederer DJ, et al. Home oxygen therapy for adults with chronic lung disease. An official American Thoracic Society clinical practice guideline. Am J Respir Crit Care Med. 2020 Nov 15;202(10):e121-41. [Erratum in: Am J Respir Crit Care Med. 2021 Apr 15;203(8):1045-6.]
https://www.atsjournals.org/doi/10.1164/rccm.202009-3608ST
http://www.ncbi.nlm.nih.gov/pubmed/33185464?tool=bestpractice.com
თუმცა, ATS-ის რეკომენდაციით ხანგრძლივი ჟანგბადით თერაპია არ უნდა დაინიშნოს COPD-ის მქონე მოზრდილებში, რომლებსაც აქვთ ზომიერი ქრონიკული ჰიპოქსია (ოთახის ტემპერატურაზე, მოსვენებულ მდგომარეობაში SpO2 89%-დან 93%-მდეა).[204]Jacobs SS, Krishnan JA, Lederer DJ, et al. Home oxygen therapy for adults with chronic lung disease. An official American Thoracic Society clinical practice guideline. Am J Respir Crit Care Med. 2020 Nov 15;202(10):e121-41. [Erratum in: Am J Respir Crit Care Med. 2021 Apr 15;203(8):1045-6.]
https://www.atsjournals.org/doi/10.1164/rccm.202009-3608ST
http://www.ncbi.nlm.nih.gov/pubmed/33185464?tool=bestpractice.com
თვითმფრინავით მგზავრობა უსაფრთხოა პაციენტების უმეტესობისთვის, ვინც ხანგრძლივ ჟანგბადით თერაპიაზეა, თუმცა პაციენტებს უნდა შეეძლოთ მოკლე პერიოდით ჟანგბადის გარეშე გაძლება, რადგან სავარაუდოა, რომ გარკვეული დროით ის შეიძლება ხელმისაწვდომი არ იყოს.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
[206]British Thoracic Society. Air travel. Mar 2022 [internet publication].
https://www.brit-thoracic.org.uk/quality-improvement/clinical-statements/air-travel
თუ SaO₂ >95% ზღვის დონეზე და SaO₂ ≥84% 6-წუთიანი სიარულის ტესტის შემდეგ, დასაშვებია საჰაერო მგზავრობა დამატებითი შეფასების გარეშე.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
[206]British Thoracic Society. Air travel. Mar 2022 [internet publication].
https://www.brit-thoracic.org.uk/quality-improvement/clinical-statements/air-travel
[207]Edvardsen A, Akerø A, Christensen CC, et al. Air travel and chronic obstructive pulmonary disease: a new algorithm for pre-flight evaluation. Thorax. 2012 Nov;67(11):964-9.
https://thorax.bmj.com/content/67/11/964
http://www.ncbi.nlm.nih.gov/pubmed/22767877?tool=bestpractice.com
დამატებითი ჟანგბადი რეკომენდებულია თუ SaO₂ 92% - 95% ზღვის დონეზე და SaO₂ <84% 6-წუთიანი სიარულის ტესტის შემდეგ, და თუ SaO₂ <92% ზღვის დონეზე[207]Edvardsen A, Akerø A, Christensen CC, et al. Air travel and chronic obstructive pulmonary disease: a new algorithm for pre-flight evaluation. Thorax. 2012 Nov;67(11):964-9.
https://thorax.bmj.com/content/67/11/964
http://www.ncbi.nlm.nih.gov/pubmed/22767877?tool=bestpractice.com
სიმაღლეზე ჰიპოქსიის სიმულაციის ტესტი (ასევე ცნობილი როგორც ჰიპოქსიური ტესტი) უნდა ჩატარდეს სხვა პაციენტებისთვის.[206]British Thoracic Society. Air travel. Mar 2022 [internet publication].
https://www.brit-thoracic.org.uk/quality-improvement/clinical-statements/air-travel
[207]Edvardsen A, Akerø A, Christensen CC, et al. Air travel and chronic obstructive pulmonary disease: a new algorithm for pre-flight evaluation. Thorax. 2012 Nov;67(11):964-9.
https://thorax.bmj.com/content/67/11/964
http://www.ncbi.nlm.nih.gov/pubmed/22767877?tool=bestpractice.com
ხანგრძლივ ჟანგბადით თერაპიაზე მყოფ პაციენტებს ბრიტანეთის გულმკერდის საზოგადოება რეკომენდაციას აძლევს ფრენის დროს გამოიყენონ ჟანგბადი 2 ლ/წთ-ით მეტი ვიდრე პაციენტს ჩვეულებრივ აქვს დანიშნული.[206]British Thoracic Society. Air travel. Mar 2022 [internet publication].
https://www.brit-thoracic.org.uk/quality-improvement/clinical-statements/air-travel
ფქოდ-ის და ძილის ობსტრუქციული აპნოეს დროს ვენტილაციური მხარდაჭერა უწყვეტი დადებითი წნევით (CPAP) აუმჯობესებს გადარჩენადობას და ამცირებს ჰოსპიტალიზაციის საჭიროებას.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
[67]Marin JM, Soriano JB, Carrizo SJ, et al. Outcomes in patients with chronic obstructive pulmonary disease and obstructive sleep apnea: the overlap syndrome. Am J Respir Crit Care Med. 2010 Aug 1;182(3):325-31.
https://www.atsjournals.org/doi/10.1164/rccm.200912-1869OC
http://www.ncbi.nlm.nih.gov/pubmed/20378728?tool=bestpractice.com
არაინვაზიური ვენტილაცია (NIV) ზოგჯერ გამოიყენება პაციენტებში ძალიან მძიმე, მაგრამ სტაბილური COPD, თუმცა დაწყების ოპტიმალური დრო და კანდიდატებისთვის საუკეთესო შერჩევის კრიტერიუმები გაურკვეველია.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
[208]Wilson ME, Dobler CC, Morrow AS, et al. Association of home noninvasive positive pressure ventilation with clinical outcomes in chronic obstructive pulmonary disease: a systematic review and meta-analysis. JAMA. 2020 Feb 4;323(5):455-65.
https://jamanetwork.com/journals/jama/fullarticle/2760390
http://www.ncbi.nlm.nih.gov/pubmed/32016309?tool=bestpractice.com
[209]Raveling T, Vonk J, Struik FM, et al. Chronic non-invasive ventilation for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2021 Aug 9;(8):CD002878.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD002878.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/34368950?tool=bestpractice.com
Cochrane-ის ერთმა მიმოხილვამ დაადგინა, რომ სახის ნიღბის საშუალებით მიწოდებული ხანგრძლივი NIV აუმჯობესებს გადარჩენადობას და ჯანმრთელობასთან დაკავშირებული ცხოვრების ხარისხს ხანმოკლე სარგებელს ანიჭებს სტაბილური COPD-ის მქონე პაციენტებთან. ხანგრძლივი NIV ასევე აუმჯობესებს ჰოსპიტალიზაციის გარეშე გადარჩენის ხანგრძლივობას პაციენტებთან, რომლებსაც აქვთ პერსისტენტული ჰიპერკაპნია გამწვავების შემდეგ.[209]Raveling T, Vonk J, Struik FM, et al. Chronic non-invasive ventilation for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2021 Aug 9;(8):CD002878.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD002878.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/34368950?tool=bestpractice.com
სხვა კვლევით დაფიქსირდა გამწვავების სიხშირის მნიშვნელოვანი შემცირება NIV-ის გამოყენების პირობებში, საკონტროლო თერაპიასთან შედარებით, თუმცა სიკვდილიანობა, PaO2, PaCO2 ან pH არ გაუმჯობესდა.[210]He X, Luo L, Ma Y, et al. Efficacy of domiciliary noninvasive ventilation on clinical outcomes in posthospital chronic obstructive pulmonary disease patients: a meta-analysis of randomized controlled trials. Ann Palliat Med. 2021 May;10(5):5137-45.
http://www.ncbi.nlm.nih.gov/pubmed/33977751?tool=bestpractice.com
ATS-ის გაიდლაინები გვთავაზობს ღამის NIV-ის გამოყენებას სტანდარტულ მოვლაზე დამატებით, ქრონიკული სტაბილური ჰიპერკაპნიური COPD-ის მქონე პაციენტებისთვის.[211]Macrea M, Oczkowski S, Rochwerg B, et al. Long-term noninvasive ventilation in chronic stable hypercapnic chronic obstructive pulmonary disease. An official American Thoracic Society clinical practice fuideline. Am J Respir Crit Care Med. 2020 Aug 15;202(4):e74-87.
https://www.atsjournals.org/doi/10.1164/rccm.202006-2382ST
http://www.ncbi.nlm.nih.gov/pubmed/32795139?tool=bestpractice.com
ევროპის რესპირატორულმა საზოგადოებამ და კანადის თორაკალურმა საზოგადოებამ გამოსცეს იდენტური გაიდლაინები.[212]Ergan B, Oczkowski S, Rochwerg B, et al. European Respiratory Society guidelines on long-term home non-invasive ventilation for management of COPD. Eur Respir J. 2019 Sep 28;54(3):1901003.
https://erj.ersjournals.com/content/54/3/1901003
http://www.ncbi.nlm.nih.gov/pubmed/31467119?tool=bestpractice.com
[213]Kaminska M, Rimmer KP, McKim DA, et al. Long-term non-invasive ventilation in patients with chronic obstructive pulmonary disease (COPD): 2021 Canadian Thoracic Society clinical practice guideline update. Can J Respir Crit Care Sleep Med. 2021 May 7;5(3):160-83.
https://www.tandfonline.com/doi/full/10.1080/24745332.2021.1911218
ქირურგიული ჩარევა
ქირურგიული ჩარევა COPD-ის მართვის ბოლო ნაბიჯია და მოიცავს ბულექტომიას, ფილტვის მოცულობის შემცირების ოპერაციას და ფილტვის ტრანსპლანტაციას.[214]van Agteren JE, Hnin K, Grosser D, et al. Bronchoscopic lung volume reduction procedures for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2017 Feb 23;(2):CD012158.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD012158.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/28230230?tool=bestpractice.com
[215]van Agteren JE, Carson KV, Tiong LU, et al. Lung volume reduction surgery for diffuse emphysema. Cochrane Database Syst Rev. 2016 Oct 14;(10):CD001001.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001001.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/27739074?tool=bestpractice.com
[  ]
How does bronchoscopic lung volume reduction compare with medical therapy in people with chronic obstructive pulmonary disease?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1680/fullShow me the answer ისინი გამოიყენება ფილტვების დინამიკის, ვარჯიშისადმი დამყოლობის და ცხოვრების ხარისხის გასაუმჯობესებლად.[215]van Agteren JE, Carson KV, Tiong LU, et al. Lung volume reduction surgery for diffuse emphysema. Cochrane Database Syst Rev. 2016 Oct 14;(10):CD001001.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001001.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/27739074?tool=bestpractice.com
ფილტვის მოცულობის შემამცირებელი ქირურგიული ჩარევის ჩვენებაა ჰაერის დინების მძიმე შეზღუდვა, განსაკუთრებით პაციენტებში, რომელთაც აღენიშნებათ ზედა წილის ლოკალური დაავადება და ნორმასთან შედარებით ფიზიკური დატვირთვის დაქვეითებული შესაძლებლობა.[214]van Agteren JE, Hnin K, Grosser D, et al. Bronchoscopic lung volume reduction procedures for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2017 Feb 23;(2):CD012158.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD012158.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/28230230?tool=bestpractice.com
[
]
How does bronchoscopic lung volume reduction compare with medical therapy in people with chronic obstructive pulmonary disease?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1680/fullShow me the answer ისინი გამოიყენება ფილტვების დინამიკის, ვარჯიშისადმი დამყოლობის და ცხოვრების ხარისხის გასაუმჯობესებლად.[215]van Agteren JE, Carson KV, Tiong LU, et al. Lung volume reduction surgery for diffuse emphysema. Cochrane Database Syst Rev. 2016 Oct 14;(10):CD001001.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001001.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/27739074?tool=bestpractice.com
ფილტვის მოცულობის შემამცირებელი ქირურგიული ჩარევის ჩვენებაა ჰაერის დინების მძიმე შეზღუდვა, განსაკუთრებით პაციენტებში, რომელთაც აღენიშნებათ ზედა წილის ლოკალური დაავადება და ნორმასთან შედარებით ფიზიკური დატვირთვის დაქვეითებული შესაძლებლობა.[214]van Agteren JE, Hnin K, Grosser D, et al. Bronchoscopic lung volume reduction procedures for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2017 Feb 23;(2):CD012158.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD012158.pub2/full
http://www.ncbi.nlm.nih.gov/pubmed/28230230?tool=bestpractice.com
[  ]
How does bronchoscopic lung volume reduction compare with medical therapy in people with chronic obstructive pulmonary disease?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1680/fullShow me the answer ერთმა მეტაანალიზმა აჩვენა ადრეული სიკვდილიანობის გაზრდილი რისკი იმ პაციენტებში, რომლებმაც გაიარეს ფილტვის მოცულობის შემცირების ოპერაცია სტანდარტულ მკურნალობასთან შედარებით; თუმცა, სიკვდილიანობის საერთო მაჩვენებლის თვალსაზრისით მნიშვნელოვანი განსხვავება არ დაფიქსირებულა.[216]van Geffen WH, Slebos DJ, Herth FJ, et al. Surgical and endoscopic interventions that reduce lung volume for emphysema: a systemic review and meta-analysis. Lancet Respir Med. 2019 Apr;7(4):313-24.
http://www.ncbi.nlm.nih.gov/pubmed/30744937?tool=bestpractice.com
ბულექტომია მკურნალობის ვარიანტია ფქოდ-ის მქონე პაციენტებისთვის, რომელთაც აღენიშნებათ ქოშინი და კტ კვლევით ვლინდება დიდი ბულა, რომელიც იკავებს სულ მცირე ჰემითორაქსის 30%-ს. ძალიან ცუდი ფუნქციური მდგომარეობა და FEV1-ის მკვეთრი შემცირება (<500 მლ) ამ ვარიანტებს ნაკლებად ხელსაყრელს ხდის. ენდობრონქული სარქვლის ჩადგმით კლინიკური მდგომარეობა მნიშვნელოვნად უმჯობესდება შესაბამისად შერჩეულ ფქოდის მქონე პაციენტებთან.[216]van Geffen WH, Slebos DJ, Herth FJ, et al. Surgical and endoscopic interventions that reduce lung volume for emphysema: a systemic review and meta-analysis. Lancet Respir Med. 2019 Apr;7(4):313-24.
http://www.ncbi.nlm.nih.gov/pubmed/30744937?tool=bestpractice.com
[217]Klooster K, Slebos DJ, Zoumot Z, et al. Endobronchial valves for emphysema: an individual patient-level reanalysis of randomised controlled trials. BMJ Open Respir Res. 2017 Nov 2;4(1):e000214.
https://bmjopenrespres.bmj.com/content/4/1/e000214
http://www.ncbi.nlm.nih.gov/pubmed/29441206?tool=bestpractice.com
[218]Labarca G, Uribe JP, Pacheco C, et al. Bronchoscopic lung volume reduction with endobronchial zephyr valves for severe emphysema: a systematic review and meta-analysis. Respiration. 2019 May 22;98(3):268-78.
http://www.ncbi.nlm.nih.gov/pubmed/31117102?tool=bestpractice.com
პროცედურა ყველაზე სასრგებლო შეიძლება იყოს პაციენტებთან, რომელთა ქოშინი ძირითადად გამოწვეულია ჰიპერინფლაციით და ჰაერის შეკავებით ტერმინალური ბრონქიოლების დისტალურ საჰაერო არეებში, რაც ვლინდება ემფიზემის სახით შესამჩნევად გაზრდილი ნარჩენი მოცულობით. უკუჩვენებებია ფილტვის აქტიური ინფექცია და არასრული წილოვანი ნაპრალები (<80%).[219]Abia-Trujillo D, Johnson MM, Patel NM, et al. Bronchoscopic lung volume reduction: a new hope for patients with severe emphysema and air trapping. Mayo Clin Proc. 2021 Feb;96(2):464-72.
http://www.ncbi.nlm.nih.gov/pubmed/32829903?tool=bestpractice.com
ყველაზე გავრცელებული გვერდითი მოვლენები, რომლებიც დაკავშირებულია ენდობრონქული სარქვლის ჩადგმასთან არის პნევმოთორაქსი და გამწვავება.[216]van Geffen WH, Slebos DJ, Herth FJ, et al. Surgical and endoscopic interventions that reduce lung volume for emphysema: a systemic review and meta-analysis. Lancet Respir Med. 2019 Apr;7(4):313-24.
http://www.ncbi.nlm.nih.gov/pubmed/30744937?tool=bestpractice.com
]
How does bronchoscopic lung volume reduction compare with medical therapy in people with chronic obstructive pulmonary disease?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1680/fullShow me the answer ერთმა მეტაანალიზმა აჩვენა ადრეული სიკვდილიანობის გაზრდილი რისკი იმ პაციენტებში, რომლებმაც გაიარეს ფილტვის მოცულობის შემცირების ოპერაცია სტანდარტულ მკურნალობასთან შედარებით; თუმცა, სიკვდილიანობის საერთო მაჩვენებლის თვალსაზრისით მნიშვნელოვანი განსხვავება არ დაფიქსირებულა.[216]van Geffen WH, Slebos DJ, Herth FJ, et al. Surgical and endoscopic interventions that reduce lung volume for emphysema: a systemic review and meta-analysis. Lancet Respir Med. 2019 Apr;7(4):313-24.
http://www.ncbi.nlm.nih.gov/pubmed/30744937?tool=bestpractice.com
ბულექტომია მკურნალობის ვარიანტია ფქოდ-ის მქონე პაციენტებისთვის, რომელთაც აღენიშნებათ ქოშინი და კტ კვლევით ვლინდება დიდი ბულა, რომელიც იკავებს სულ მცირე ჰემითორაქსის 30%-ს. ძალიან ცუდი ფუნქციური მდგომარეობა და FEV1-ის მკვეთრი შემცირება (<500 მლ) ამ ვარიანტებს ნაკლებად ხელსაყრელს ხდის. ენდობრონქული სარქვლის ჩადგმით კლინიკური მდგომარეობა მნიშვნელოვნად უმჯობესდება შესაბამისად შერჩეულ ფქოდის მქონე პაციენტებთან.[216]van Geffen WH, Slebos DJ, Herth FJ, et al. Surgical and endoscopic interventions that reduce lung volume for emphysema: a systemic review and meta-analysis. Lancet Respir Med. 2019 Apr;7(4):313-24.
http://www.ncbi.nlm.nih.gov/pubmed/30744937?tool=bestpractice.com
[217]Klooster K, Slebos DJ, Zoumot Z, et al. Endobronchial valves for emphysema: an individual patient-level reanalysis of randomised controlled trials. BMJ Open Respir Res. 2017 Nov 2;4(1):e000214.
https://bmjopenrespres.bmj.com/content/4/1/e000214
http://www.ncbi.nlm.nih.gov/pubmed/29441206?tool=bestpractice.com
[218]Labarca G, Uribe JP, Pacheco C, et al. Bronchoscopic lung volume reduction with endobronchial zephyr valves for severe emphysema: a systematic review and meta-analysis. Respiration. 2019 May 22;98(3):268-78.
http://www.ncbi.nlm.nih.gov/pubmed/31117102?tool=bestpractice.com
პროცედურა ყველაზე სასრგებლო შეიძლება იყოს პაციენტებთან, რომელთა ქოშინი ძირითადად გამოწვეულია ჰიპერინფლაციით და ჰაერის შეკავებით ტერმინალური ბრონქიოლების დისტალურ საჰაერო არეებში, რაც ვლინდება ემფიზემის სახით შესამჩნევად გაზრდილი ნარჩენი მოცულობით. უკუჩვენებებია ფილტვის აქტიური ინფექცია და არასრული წილოვანი ნაპრალები (<80%).[219]Abia-Trujillo D, Johnson MM, Patel NM, et al. Bronchoscopic lung volume reduction: a new hope for patients with severe emphysema and air trapping. Mayo Clin Proc. 2021 Feb;96(2):464-72.
http://www.ncbi.nlm.nih.gov/pubmed/32829903?tool=bestpractice.com
ყველაზე გავრცელებული გვერდითი მოვლენები, რომლებიც დაკავშირებულია ენდობრონქული სარქვლის ჩადგმასთან არის პნევმოთორაქსი და გამწვავება.[216]van Geffen WH, Slebos DJ, Herth FJ, et al. Surgical and endoscopic interventions that reduce lung volume for emphysema: a systemic review and meta-analysis. Lancet Respir Med. 2019 Apr;7(4):313-24.
http://www.ncbi.nlm.nih.gov/pubmed/30744937?tool=bestpractice.com
ფილტვის გადანერგვაზე მიმართვის კრიტერიუმები:[220]Leard LE, Holm AM, Valapour M, et al. Consensus document for the selection of lung transplant candidates: an update from the International Society for Heart and Lung Transplantation. J Heart Lung Transplant. 2021 Nov;40(11):1349-79.
https://www.jhltonline.org/article/S1053-2498(21)02407-4/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/34419372?tool=bestpractice.com
სხეულის მასის ინდექსი, ჰაერგამტარი გზების ობსტრუქცია, ქოშინი და ვარჯიშის (BODE) ქულა 5-6 დამატებითი ფაქტორ(ებ)ით, მიუთითებს სიკვდილიანობის გაზრდილ რისკზე:
ხშირი მწვავე გამწვავებები
BODE ქულის გაზრდა >1 ბოლო 24 თვის განმავლობაში
ფილტვის არტერიიის დიამეტრი აორტასთან მიმართებით >1 CT სკანირებაზე
FEV1 სავარაუდოს 20%-დან 25%-მდე
კლინიკური გაუარესება მიუხედავად მაქსიმალური მკურნალობისა, მ.შ. მედიკამენტების გამოყენებით, ფილტვების რეაბილიტაციით, ოქსიგენოთერაპიით და, საჭიროების შემთხვევაში, ღამის არაინვაზიური დადებითი წნევის ვენტილაციით.
პაციენტისთვის მიუღებელია ცხოვრების ცუდი ხარისხი
პაციენტისთვის, რომელიც ბრონქოსკოპულად ან ქირურგიული ოპერაციის გზით ფილტვის მოცულობის შემცირების კანდიდატია (LVR), მიზანშეწონილია ერთდროული მიმართვა როგორც ფილტვის ტრანსპლანტაციისთვის, ასევე LVR-ზე შეფასებისთვის
[
BODE ინდექსი ფქოდ გადარჩენადობის პროგნოზირებისთვის
Opens in new window
]
ფილტვის ტრანსპლანტაცი აუმჯობესებს ცხოვრების ხარისხს და ფუნქციონირების შესაძლებლობას.[215]van Agteren JE, Carson KV, Tiong LU, et al. Lung volume reduction surgery for diffuse emphysema. Cochrane Database Syst Rev. 2016 Oct 14;(10):CD001001.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001001.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/27739074?tool=bestpractice.com
თუმცა ტრანსპლანტაციის ბენეფიტს არ წარმოადგენს გადარჩენა.[221]Stavem K, Bjørtuft Ø, Borgan Ø, et al. Lung transplantation in patients with chronic obstructive pulmonary disease in a national cohort is without obvious survival benefit. J Heart Lung Transplant. 2006 Jan;25(1):75-84.
http://www.ncbi.nlm.nih.gov/pubmed/16399534?tool=bestpractice.com
პალიატიური მკურნალობა
პალიატიური თერაპია დისპნოეს სიმპტომების გასაუმჯობესებლად, ნუტრიციული მხარდაჭერის შემდეგ, მოიცავს შფოთვის და დეპრესიის მართვას, დაღლილობის მოხსნას. ეს შეიძლება სარგებლიანი იყოს ფქოდ-ის დროს იმ პაციენტებთან, რომელთაც ოპტიმალური სამედიცინო მკურნალობის მიუხედავად აღნიშნული პრობლემები აქვთ. "საბოლოო მოვლა" ჰოსპისში განსახილველია ძალიან მძიმე, შორსწასული დაავადების შემთხვევებში. პაციენტი და ოჯახის წევრები ინფორმირებულნი უნდა იყვნენ პროცესის მიმდინარეობის შესახებ და ეს თემა უნდა განიხილოთ დაავადების ადრეულ ეტაპზევე, სანამ გამოვლინდება სუნთქვის მწვავე უკმარისობა.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
[222]Janssen DJA, Bajwah S, Boon MH, et al. European Respiratory Society clinical practice guideline: palliative care for people with COPD or interstitial lung disease. Eur Respir J. 2023 Aug;62(2):2202014.
https://erj.ersjournals.com/content/62/2/2202014
http://www.ncbi.nlm.nih.gov/pubmed/37290789?tool=bestpractice.com
ოპიოიდურმა ანალგეტიკებმა, ვენტილაციამ, ნერვ-კუნთოვანმა ელექტროსტიმულაციამ და გულმკერდის კედლის ვიბრაციამ შეიძლება მოხსნას ქოშინი.[1]Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: 2024 report. 2024 [internet publication].
https://goldcopd.org/2024-gold-report
ერთ-ერთი კვლევის მიხედვით, ოპიოიდებისა და ბეზოდიაზეპამის დაბალი დოზები უსაფრთხოა და არ ასოცირდება ჰოსპიტალიზაციის ან სიკვდილობის ზრდასთან.[223]Ekström MP, Bornefalk-Hermansson A, Abernethy AP, et al. Safety of benzodiazepines and opioids in very severe respiratory disease: national prospective study. BMJ. 2014 Jan 30;348:g445.
https://www.bmj.com/content/348/bmj.g445.long
http://www.ncbi.nlm.nih.gov/pubmed/24482539?tool=bestpractice.com
სხვა კვლევამ აჩვენა, რომ რეგულარულად, დაბალი დოზით, პერორალური მორფინის 4 კვირის განმავლობაში მიღება აუმჯობესებს დაავადებისთვის სპეციფიურ ჯანმრთელობის სტატუსს COPD-ის და მოსვენებულ მდგომარეობაში ან მცირე დატვირთვაზე ქოშინის მქონე პაციენტებთან.[224]Verberkt CA, van den Beuken-van Everdingen MHJ, Schols JMGA, et al. Effect of sustained-release morphine for refractory breathlessness in chronic obstructive pulmonary disease on health status: a randomized clinical trial. JAMA Intern Med. 2020 Oct 1;180(10):1306-14.
https://jamanetwork.com/journals/jamainternalmedicine/fullarticle/2769373
http://www.ncbi.nlm.nih.gov/pubmed/32804188?tool=bestpractice.com
Cochrane-ს ერთი მიმოხილვის მიხედვით, არ არსებობს მტკიცებულება ბენზოდიაზეპინების მხარდასაჭერად ან წინააღმდეგ შორსწასული კიბოს და ფქოდ-ის შემთხვევაში სუნთქვის უკმარისობის შესამსუბუქებლად.[225]Simon ST, Higginson IJ, Booth S, et al. Benzodiazepines for the relief of breathlessness in advanced malignant and non-malignant diseases in adults. Cochrane Database Syst Rev. 2016 Oct 20;(10):CD007354.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD007354.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/27764523?tool=bestpractice.com
აკუპუნქტურა და აკუ-წნევა შეიძლება ასევე აუმჯობესებდეს სუნთქვას და ცხოვრების ხარისხს პაციენტებში, რომლებსაც აქვთ შორსწასული ფქოდ.[226]von Trott P, Oei SL, Ramsenthaler C. Acupuncture for breathlessness in advanced diseases: a systematic review and meta-analysis. J Pain Symptom Manage. 2020 Feb;59(2):327-38.e3.
http://www.ncbi.nlm.nih.gov/pubmed/31539602?tool=bestpractice.com
 ]
[Evidence A]
]
[Evidence A]

 ]
უახლეს LAMA-ებს, როგორიცაა აკლიდინიუმი, გლიკოპირონიუმი და უმეკლიდინიუმი, აქვთ სულ მცირე თიოტროპიუმთან შედარებითი ეფექტურობა, FEV1-ის საწყისი მაჩვენებლის ცვლილების, გარდამავალი ქოშინის ინდექსის ქულის, სენტ-ჯორჯის რესპირატორული კითხვარის ქულის და მედიკამენტების გამოყენების კუთხით.[94] რევეფენაცინი არის ნებულიზირებული ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტი, რომელიც დამტკიცებულია საშუალო-მძიმე ფქოდ-ის შემანარჩუნებელ თერაპიად. ზოგიერთი კვლევის მიხედვით, არსებობს მოსაზრება, რომ ხანმოკლე და ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტების ფონზე გულსისხლძარღვთა გართულებებთან დაკავშირებული სიკვდილობა გაზრდილია.[95][96] ერთმა კვლევამ დაასკვნა, რომ აკლიდინიუმი ძირითად გულ-სისხლძარღვთა გვერდით მოვლენების მზარდ გამოვლენასთან არ ასოცირდება, პლაცებოსთან შედარებით.[97] პოპულაციური-კოჰორტული კვლევის თანახმად, ფქოდ-ის მქონე ხანდაზმულ მამაკაცებში ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტების დაწყების შემთხვევაში იმატებს საშარდე ტრაქტის ინფექციების რისკი.[98]
]
უახლეს LAMA-ებს, როგორიცაა აკლიდინიუმი, გლიკოპირონიუმი და უმეკლიდინიუმი, აქვთ სულ მცირე თიოტროპიუმთან შედარებითი ეფექტურობა, FEV1-ის საწყისი მაჩვენებლის ცვლილების, გარდამავალი ქოშინის ინდექსის ქულის, სენტ-ჯორჯის რესპირატორული კითხვარის ქულის და მედიკამენტების გამოყენების კუთხით.[94] რევეფენაცინი არის ნებულიზირებული ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტი, რომელიც დამტკიცებულია საშუალო-მძიმე ფქოდ-ის შემანარჩუნებელ თერაპიად. ზოგიერთი კვლევის მიხედვით, არსებობს მოსაზრება, რომ ხანმოკლე და ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტების ფონზე გულსისხლძარღვთა გართულებებთან დაკავშირებული სიკვდილობა გაზრდილია.[95][96] ერთმა კვლევამ დაასკვნა, რომ აკლიდინიუმი ძირითად გულ-სისხლძარღვთა გვერდით მოვლენების მზარდ გამოვლენასთან არ ასოცირდება, პლაცებოსთან შედარებით.[97] პოპულაციური-კოჰორტული კვლევის თანახმად, ფქოდ-ის მქონე ხანდაზმულ მამაკაცებში ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტების დაწყების შემთხვევაში იმატებს საშარდე ტრაქტის ინფექციების რისკი.[98] ]
[Evidence A] სტაბილური COPD-ის შემთხვევაში, თუ მონოთერაპიის შესახებ გადაწყვეტილების მიღებაა საჭირო, უპირატესობა LAMA-ს უნდა მიენიჭოს LABA აგენტებთან შედარებით.[99] ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტები უფრო მეტად ამსუბუქებს გამწვავებებს საშუალო-მძიმე ფქოდ-ის დროს, ვიდრე ხანგრძლივი მოქმედების ბეტა-2 აგონისტები.[100][101] LAMA-ს გრძელვადიანი უსაფრთხოება გამოვლინდა UPLIFT კვლევაში.[102]
]
[Evidence A] სტაბილური COPD-ის შემთხვევაში, თუ მონოთერაპიის შესახებ გადაწყვეტილების მიღებაა საჭირო, უპირატესობა LAMA-ს უნდა მიენიჭოს LABA აგენტებთან შედარებით.[99] ხანგრძლივი მოქმედების მუსკარინული ანტაგონისტები უფრო მეტად ამსუბუქებს გამწვავებებს საშუალო-მძიმე ფქოდ-ის დროს, ვიდრე ხანგრძლივი მოქმედების ბეტა-2 აგონისტები.[100][101] LAMA-ს გრძელვადიანი უსაფრთხოება გამოვლინდა UPLIFT კვლევაში.[102] ]
]
 ]
]
 ]
ერთმა სისტემატურმა მიმოხილვამ და ქსელის მეტა-ანალიზმა აჩვენა, რომ ყველა LABA/LAMA ფიქსირებული დოზის კომბინაციას მსგავსი ეფექტურობა და უსაფრთხოება ჰქონდა.[109]
]
ერთმა სისტემატურმა მიმოხილვამ და ქსელის მეტა-ანალიზმა აჩვენა, რომ ყველა LABA/LAMA ფიქსირებული დოზის კომბინაციას მსგავსი ეფექტურობა და უსაფრთხოება ჰქონდა.[109] ]
ეს რისკი უფრო მაღალია ფლუტიკაზონისთვის ბუდესონიდთან შედარებით.[116][117][118] დანიელ პაციენტთა დიდ ჯგუფში ჩატარებულმა კვლევამ აჩვენა, რომ Pseudomonas aeruginosa-ს, ჰოსპიტალური პნევმონიის ხშირი გამომწვევის, შეძენის რისკი დამოკიდებულია დოზაზე, და ყველაზე მაღალი რისკი ICS-ის მაღალ დოზასთან ასოცირდება. კვლევამ ასევე აჩვენა, რომ P aeruginosa-ს მქონე პაციენტებს უფრო დაბალი BMI და FEV1 აქვთ ვიდრე P aeruginosa-ს არმქონე პაციენტებს.[119] ერთმა სისტემურმა მიმოხილვამ და მეტა-ანალიზმა აჩვენა, რომ, მიუხედავად ICS-ისთან ასოცირებული პნევმონიის დაუკორექტირებელი რისკის მნიშვნელოვანი ზრდისა, პნევმონიით სიკვდილიანობა და საერთო სიკვდილიანობა არ გაიზარდა რანდომიზებულ კონტროლირებად კვლევებში და შემცირდა ობსერვაციულ კვლევებში.[120] ამგვარად, საჭიროა მკურნალობის დანიშვნის დროს ინდივიდუალური მიდგომა, რომლის მიხედვითაც შეფასდება პნევმონიის რისკს მკურნალობის სარგებლთან, გამწვავებების შემცირებასთან, შედარებით.[79][121][122] ასევე შემაშფოთებელია ტუბერკულოზისა და გრიპის განვითარების გაზრდილი რისკი COPD-ით დაავადებულ მოზრდილ პაციენტებთან, რომლებიც ICS თერაპიაზე იმყოფებიან, თუმცა ერთმა მეტა-ანალიზმა აჩვენა, რომ ყველა შეფასებული ტუბერკულოზის შემთხვევის 1%-ზე ნაკლები უკავშირდებოდა ICS-ის ექსპოზიციას.[123][124] ICS-მ ასევე შეიძლება გამოიწვიოს ოროფარინგიალური კანდიდოზი და დისფონია.[79]
[
]
ეს რისკი უფრო მაღალია ფლუტიკაზონისთვის ბუდესონიდთან შედარებით.[116][117][118] დანიელ პაციენტთა დიდ ჯგუფში ჩატარებულმა კვლევამ აჩვენა, რომ Pseudomonas aeruginosa-ს, ჰოსპიტალური პნევმონიის ხშირი გამომწვევის, შეძენის რისკი დამოკიდებულია დოზაზე, და ყველაზე მაღალი რისკი ICS-ის მაღალ დოზასთან ასოცირდება. კვლევამ ასევე აჩვენა, რომ P aeruginosa-ს მქონე პაციენტებს უფრო დაბალი BMI და FEV1 აქვთ ვიდრე P aeruginosa-ს არმქონე პაციენტებს.[119] ერთმა სისტემურმა მიმოხილვამ და მეტა-ანალიზმა აჩვენა, რომ, მიუხედავად ICS-ისთან ასოცირებული პნევმონიის დაუკორექტირებელი რისკის მნიშვნელოვანი ზრდისა, პნევმონიით სიკვდილიანობა და საერთო სიკვდილიანობა არ გაიზარდა რანდომიზებულ კონტროლირებად კვლევებში და შემცირდა ობსერვაციულ კვლევებში.[120] ამგვარად, საჭიროა მკურნალობის დანიშვნის დროს ინდივიდუალური მიდგომა, რომლის მიხედვითაც შეფასდება პნევმონიის რისკს მკურნალობის სარგებლთან, გამწვავებების შემცირებასთან, შედარებით.[79][121][122] ასევე შემაშფოთებელია ტუბერკულოზისა და გრიპის განვითარების გაზრდილი რისკი COPD-ით დაავადებულ მოზრდილ პაციენტებთან, რომლებიც ICS თერაპიაზე იმყოფებიან, თუმცა ერთმა მეტა-ანალიზმა აჩვენა, რომ ყველა შეფასებული ტუბერკულოზის შემთხვევის 1%-ზე ნაკლები უკავშირდებოდა ICS-ის ექსპოზიციას.[123][124] ICS-მ ასევე შეიძლება გამოიწვიოს ოროფარინგიალური კანდიდოზი და დისფონია.[79]
[  ]
]
 ]
ასეთი მიდგომა ზოგჯერ მოსახერხებელია და გვეხმარება ზოგიერთი პაციენტის დაყოლიებაში. ამ კლასში პრეპარატების არჩევა ხელმისაწვდომობას და ინდივიდუალურ დამყოლობას ეფუძნება.[127] კომბინაცია შეიძლება სხვადახვა ინჰალატორით ან ერთი კობინირებუი ინჰალატორით.
]
ასეთი მიდგომა ზოგჯერ მოსახერხებელია და გვეხმარება ზოგიერთი პაციენტის დაყოლიებაში. ამ კლასში პრეპარატების არჩევა ხელმისაწვდომობას და ინდივიდუალურ დამყოლობას ეფუძნება.[127] კომბინაცია შეიძლება სხვადახვა ინჰალატორით ან ერთი კობინირებუი ინჰალატორით. ]
]
 ]
არ არსებობს მტკიცებულებები აზითრომიცინით მკურნალობის ეფექტიანობის შესახებ 1 წელზე ხანგრძლივად.
]
არ არსებობს მტკიცებულებები აზითრომიცინით მკურნალობის ეფექტიანობის შესახებ 1 წელზე ხანგრძლივად. ]
ფიზიკური აქტივობის გაუმჯობესების ოპტიმალური დრო, კომპონენტები, ხანგრძლივობა და მოდელები გაურკვეველი რჩება. მეტა-ანალიზის მონაცემებით იოგას, ციგუნის და სახლის პირობებში ჩატარებულ სხვა სუნთქვის ვარჯიშებს შეუძლიათ გააუმჯობესონ ფიზიკური შესაძლებლობები და ფილტვის ფუნქცია COPD-ის მქონე პაციენტებში.[170][171][172] ტაი ჩი აუმჯობესებს ფიზიკურ შესაძლებლობას პაციენტის სტანდარტულ მოვლასთან შედარებით.[173]
]
ფიზიკური აქტივობის გაუმჯობესების ოპტიმალური დრო, კომპონენტები, ხანგრძლივობა და მოდელები გაურკვეველი რჩება. მეტა-ანალიზის მონაცემებით იოგას, ციგუნის და სახლის პირობებში ჩატარებულ სხვა სუნთქვის ვარჯიშებს შეუძლიათ გააუმჯობესონ ფიზიკური შესაძლებლობები და ფილტვის ფუნქცია COPD-ის მქონე პაციენტებში.[170][171][172] ტაი ჩი აუმჯობესებს ფიზიკურ შესაძლებლობას პაციენტის სტანდარტულ მოვლასთან შედარებით.[173] ]
აშშ-ს დაავადებათა კონტროლისა და პრევენციის ცენტრი (CDC) გვთავაზობს პნევმოკოკური 15-ვალენტიანი (PCV15) ან 20-ვალენტიანი PCV (PCV20) ვაქცინის ერთჯერადი დოზის მიღებას COPD-ით დაავადებული ყველა პაციენტისთვის, რომლებსაც ადრე არ მიუღიათ PCV ან ვისი ვაქცინაციის ისტორია უცნობია. პაციენტმა, რომელსაც PCV15-ით ვაქცინაცია ჩაუტარდა, 23-ვალენტიანი პოლისაქარიდის ვაქცინის (PPSV23) ერთჯერადი დოზა უნდა მიიღოს სულ მცირე 1 წლის შემდეგ.[184]
]
აშშ-ს დაავადებათა კონტროლისა და პრევენციის ცენტრი (CDC) გვთავაზობს პნევმოკოკური 15-ვალენტიანი (PCV15) ან 20-ვალენტიანი PCV (PCV20) ვაქცინის ერთჯერადი დოზის მიღებას COPD-ით დაავადებული ყველა პაციენტისთვის, რომლებსაც ადრე არ მიუღიათ PCV ან ვისი ვაქცინაციის ისტორია უცნობია. პაციენტმა, რომელსაც PCV15-ით ვაქცინაცია ჩაუტარდა, 23-ვალენტიანი პოლისაქარიდის ვაქცინის (PPSV23) ერთჯერადი დოზა უნდა მიიღოს სულ მცირე 1 წლის შემდეგ.[184] ]
შეიძლება მცირედ შეამციროს გამწვავებების სიხშირე და თვის განმავლობაში უნარშეზღუდული დღეების ჯამური რაოდენობა, მაგრამ არ აუმჯობესებს ფილტვის ფუნქციასა და ცხოვრების ხარისხს.[186] ერთი მეტა-ანალიზის მიხედვით, რომლითაც შედარდა ერდოსტეინი, კარბოცისტეინი და აცეტილცისტეინი, ერდოსტეინს აღმოაჩნდა ყველაზე უსაფრთხო და ეფექტური პროფილი. ერდოსტეინი ამცირებს გამწვავების მიზეზით ჰოსპიტალიზაციის რისკს. ერდოსტეინი და აცეტილცისტეინი ამცირებს გამწვავების ხანგრძლივობას.[187] სხვა მეტა-ანალიზმა აჩვენა, რომ აცეტილცისტეინმა მნიშვნელოვნად შეამცირა გამწვავებების სიხშირე პლაცებოსთან შედარებით, გვერდითი მოვლენების რისკის გაზრდის გარეშე. ავტორებმა დაასკვნეს, რომ 3 თვიანი მკურნალობა დაბალი დოზით ეფექტური იყო.[188] ერდოსტეინი და კარბოცისტეინი არ არის ხელმისაწვდომი აშშ-ში და რამდენიმე სხვა ქვეყანაში. მუკოლიზური საშუალებებით მკურნალობამ, როგორიცაა კარბოცისტეინი და აცეტილცისტეინი, შეიძლება შეამციროს გამწვავებები და ზომიერად გააუმჯობესოს ჯანმრთელობის მდგომარეობა პაციენტებში, რომლებიც არ იღებენ ICS.[1] თუმცა, ერდოსტეინს შეუძლია მნიშვნელოვანი გავლენა მოახდინოს მსუბუქ გამწვავებებზე, მიუხედავად იმისა, პაციენტი იღებს თუ არა ICS.[1]
]
შეიძლება მცირედ შეამციროს გამწვავებების სიხშირე და თვის განმავლობაში უნარშეზღუდული დღეების ჯამური რაოდენობა, მაგრამ არ აუმჯობესებს ფილტვის ფუნქციასა და ცხოვრების ხარისხს.[186] ერთი მეტა-ანალიზის მიხედვით, რომლითაც შედარდა ერდოსტეინი, კარბოცისტეინი და აცეტილცისტეინი, ერდოსტეინს აღმოაჩნდა ყველაზე უსაფრთხო და ეფექტური პროფილი. ერდოსტეინი ამცირებს გამწვავების მიზეზით ჰოსპიტალიზაციის რისკს. ერდოსტეინი და აცეტილცისტეინი ამცირებს გამწვავების ხანგრძლივობას.[187] სხვა მეტა-ანალიზმა აჩვენა, რომ აცეტილცისტეინმა მნიშვნელოვნად შეამცირა გამწვავებების სიხშირე პლაცებოსთან შედარებით, გვერდითი მოვლენების რისკის გაზრდის გარეშე. ავტორებმა დაასკვნეს, რომ 3 თვიანი მკურნალობა დაბალი დოზით ეფექტური იყო.[188] ერდოსტეინი და კარბოცისტეინი არ არის ხელმისაწვდომი აშშ-ში და რამდენიმე სხვა ქვეყანაში. მუკოლიზური საშუალებებით მკურნალობამ, როგორიცაა კარბოცისტეინი და აცეტილცისტეინი, შეიძლება შეამციროს გამწვავებები და ზომიერად გააუმჯობესოს ჯანმრთელობის მდგომარეობა პაციენტებში, რომლებიც არ იღებენ ICS.[1] თუმცა, ერდოსტეინს შეუძლია მნიშვნელოვანი გავლენა მოახდინოს მსუბუქ გამწვავებებზე, მიუხედავად იმისა, პაციენტი იღებს თუ არა ICS.[1] ]
არსებობს მტკიცებულებები, რომლთა მიხედვითაც პულმონური რეაბილიტაცია უნდა დაიწყოს გამწვავების დაწყებიდან 1 თვის განმავლობაში.[192][193]
]
არსებობს მტკიცებულებები, რომლთა მიხედვითაც პულმონური რეაბილიტაცია უნდა დაიწყოს გამწვავების დაწყებიდან 1 თვის განმავლობაში.[192][193] ]
]
 ]
ისინი გამოიყენება ფილტვების დინამიკის, ვარჯიშისადმი დამყოლობის და ცხოვრების ხარისხის გასაუმჯობესებლად.[215] ფილტვის მოცულობის შემამცირებელი ქირურგიული ჩარევის ჩვენებაა ჰაერის დინების მძიმე შეზღუდვა, განსაკუთრებით პაციენტებში, რომელთაც აღენიშნებათ ზედა წილის ლოკალური დაავადება და ნორმასთან შედარებით ფიზიკური დატვირთვის დაქვეითებული შესაძლებლობა.[214]
[
]
ისინი გამოიყენება ფილტვების დინამიკის, ვარჯიშისადმი დამყოლობის და ცხოვრების ხარისხის გასაუმჯობესებლად.[215] ფილტვის მოცულობის შემამცირებელი ქირურგიული ჩარევის ჩვენებაა ჰაერის დინების მძიმე შეზღუდვა, განსაკუთრებით პაციენტებში, რომელთაც აღენიშნებათ ზედა წილის ლოკალური დაავადება და ნორმასთან შედარებით ფიზიკური დატვირთვის დაქვეითებული შესაძლებლობა.[214]
[  ]
ერთმა მეტაანალიზმა აჩვენა ადრეული სიკვდილიანობის გაზრდილი რისკი იმ პაციენტებში, რომლებმაც გაიარეს ფილტვის მოცულობის შემცირების ოპერაცია სტანდარტულ მკურნალობასთან შედარებით; თუმცა, სიკვდილიანობის საერთო მაჩვენებლის თვალსაზრისით მნიშვნელოვანი განსხვავება არ დაფიქსირებულა.[216] ბულექტომია მკურნალობის ვარიანტია ფქოდ-ის მქონე პაციენტებისთვის, რომელთაც აღენიშნებათ ქოშინი და კტ კვლევით ვლინდება დიდი ბულა, რომელიც იკავებს სულ მცირე ჰემითორაქსის 30%-ს. ძალიან ცუდი ფუნქციური მდგომარეობა და FEV1-ის მკვეთრი შემცირება (<500 მლ) ამ ვარიანტებს ნაკლებად ხელსაყრელს ხდის. ენდობრონქული სარქვლის ჩადგმით კლინიკური მდგომარეობა მნიშვნელოვნად უმჯობესდება შესაბამისად შერჩეულ ფქოდის მქონე პაციენტებთან.[216][217][218] პროცედურა ყველაზე სასრგებლო შეიძლება იყოს პაციენტებთან, რომელთა ქოშინი ძირითადად გამოწვეულია ჰიპერინფლაციით და ჰაერის შეკავებით ტერმინალური ბრონქიოლების დისტალურ საჰაერო არეებში, რაც ვლინდება ემფიზემის სახით შესამჩნევად გაზრდილი ნარჩენი მოცულობით. უკუჩვენებებია ფილტვის აქტიური ინფექცია და არასრული წილოვანი ნაპრალები (<80%).[219] ყველაზე გავრცელებული გვერდითი მოვლენები, რომლებიც დაკავშირებულია ენდობრონქული სარქვლის ჩადგმასთან არის პნევმოთორაქსი და გამწვავება.[216]
]
ერთმა მეტაანალიზმა აჩვენა ადრეული სიკვდილიანობის გაზრდილი რისკი იმ პაციენტებში, რომლებმაც გაიარეს ფილტვის მოცულობის შემცირების ოპერაცია სტანდარტულ მკურნალობასთან შედარებით; თუმცა, სიკვდილიანობის საერთო მაჩვენებლის თვალსაზრისით მნიშვნელოვანი განსხვავება არ დაფიქსირებულა.[216] ბულექტომია მკურნალობის ვარიანტია ფქოდ-ის მქონე პაციენტებისთვის, რომელთაც აღენიშნებათ ქოშინი და კტ კვლევით ვლინდება დიდი ბულა, რომელიც იკავებს სულ მცირე ჰემითორაქსის 30%-ს. ძალიან ცუდი ფუნქციური მდგომარეობა და FEV1-ის მკვეთრი შემცირება (<500 მლ) ამ ვარიანტებს ნაკლებად ხელსაყრელს ხდის. ენდობრონქული სარქვლის ჩადგმით კლინიკური მდგომარეობა მნიშვნელოვნად უმჯობესდება შესაბამისად შერჩეულ ფქოდის მქონე პაციენტებთან.[216][217][218] პროცედურა ყველაზე სასრგებლო შეიძლება იყოს პაციენტებთან, რომელთა ქოშინი ძირითადად გამოწვეულია ჰიპერინფლაციით და ჰაერის შეკავებით ტერმინალური ბრონქიოლების დისტალურ საჰაერო არეებში, რაც ვლინდება ემფიზემის სახით შესამჩნევად გაზრდილი ნარჩენი მოცულობით. უკუჩვენებებია ფილტვის აქტიური ინფექცია და არასრული წილოვანი ნაპრალები (<80%).[219] ყველაზე გავრცელებული გვერდითი მოვლენები, რომლებიც დაკავშირებულია ენდობრონქული სარქვლის ჩადგმასთან არის პნევმოთორაქსი და გამწვავება.[216]






