Recomendações
Urgente
Pense: “ Isso poderia ser sepse?" com base na deterioração aguda em um paciente adulto no qual há evidência clínica ou forte suspeita de infecção.[66][67][68] Consulte Sepse em adultos.
Use uma abordagem sistemática, juntamente com seu julgamento clínico, para avaliação; consulte urgentemente um tomador de decisão clínica sênior (por exemplo, médico de nível ST4 no Reino Unido) se suspeitar de sepse.[67][68][69][70]
Consulte as diretrizes locais para a abordagem recomendada em sua instituição para avaliação e tratamento do paciente com suspeita de sepse.
A pneumonia é uma das principais fontes de sepse.[80]
Durante a pandemia de COVID-19, para pacientes com suspeita ou confirmação de pneumonia por COVID-19, consulte Doença por coronavírus 2019 (COVID-19). Considere que todos os pacientes com tosse, febre ou outros sintomas sugestivos têm COVID-19 até prova em contrário.
A pneumonia devida à COVID-19 não é abordada neste tópico.
Urgente: no hospital
Estratifique pacientes com pneumonia confirmada por radiografia de tórax de acordo com o risco de mortalidade e a gravidade da doença usando a pontuação CURB-65 e seu julgamento clínico . [ Escore CURB-65 de gravidade de uma pneumonia. Opens in new window ] Use a pontuação para ajudar a informar seu plano de tratamento.
Pontuação de 3-5: alta gravidade.
Pontuação 2: trate como pneumonia de gravidade moderada.
Pontuação 0 ou 1: trate como pneumonia de baixa gravidade.
Administre antibióticos empíricos imediatamente a todos os pacientes com PAC confirmada por radiografia torácica. Os pacientes devem receber antibióticos dentro de 4 horas após a apresentação ao hospital.[1][65][117]
PAC de alta gravidade: administre antibióticos intravenosos de amplo espectro – consulte seu protocolo local.
PAC de gravidade moderada e baixa: administre antibióticos orais (ou intravenosos se a terapia oral for contra-indicada) – consulte seu protocolo local.
Administre antibióticos empíricos a pacientes com doenças potencialmente fatais com base em um diagnóstico clínico presuntivo e, em seguida, solicite uma radiografia torácica imediata para confirmar o diagnóstico.[1][65]
Siga seu protocolo local para investigação e tratamento de todos os pacientes com suspeita de sepse ou aqueles em risco. Inicie o tratamento imediatamente. Determine a urgência do tratamento de acordo com a probabilidade de infecção e a gravidade da doença, ou de acordo com o protocolo local.[70][81]
Avalie as necessidades de oxigênio. Prescreva oxigênio se a saturação de oxigênio for <94% e mantenha-se na faixa alvo.[1][65] Em pacientes com risco de hipercapnia, prescreva oxigênio se a saturação de oxigênio for <88%.[71]
Monitore a oxigenoterapia controlada. Um limite superior de SpO 2 de 96% é razoável quando se administra oxigênio suplementar à maioria dos pacientes com doenças agudas que não correm risco de hipercapnia.
As evidências sugerem que o uso liberal de oxigênio suplementar (SpO 2 > 96% alvo) em adultos com doenças agudas está associado a maior mortalidade do que a oxigenoterapia mais conservadora.[72]
Uma meta de SpO 2 mais baixa de 88% a 92% é apropriada se o paciente estiver em risco de insuficiência respiratória hipercápnica.[71]
Meça e registre observações pelo menos duas vezes ao dia e com mais frequência (por exemplo, a cada hora) em pessoas internadas em uma unidade de terapia intensiva para informar seu plano de manejo.[1][65]
Revise todos os pacientes com PAC de alta gravidade (alto risco de morte) pelo menos a cada 12 horas até a melhora.[1] Isso deve ser feito por um colega sênior e pela equipe médica.[1][65]
Urgente: na comunidade
Estratifique os pacientes de acordo com o risco de mortalidade e a gravidade da doença usando o escore CRB-65 (consulte nossa seção Diagnóstico – recomendações para obter mais informações) e seu julgamento clínico.[1][65]
Pontuação 3 ou mais (alta gravidade): interne o paciente no hospital imediatamente.[1][63][65]
Pontuação de 1 ou 2 (gravidade moderada): encaminhe ao hospital. Esses pacientes têm maior risco de morte, particularmente aqueles com uma pontuação de 2.[1][63][65]
Pontuação 0 (baixa gravidade): trata a maioria dos pacientes em casa.[1][63][65]
Considere o tratamento em casa para pacientes com uma pontuação CRB-65 de 0 (baixa gravidade) ou uma pontuação CRB-65 de 1 ou 2 (gravidade média) se eles desejarem ser tratados em casa e atenderem a todos os seguintes critérios:[1][63][65]
Eles são capazes de tomar medicamentos orais de forma segura e confiável
Suas circunstâncias sociais os tornam adequados para tratamento em casa
Eles não têm comorbidades instáveis.
Adote uma abordagem cautelosa ao decidir se é seguro tratar qualquer paciente com PAC de gravidade moderada (pontuação CRB-65 de 1 ou 2) na comunidade.
Administre antibióticos empíricos antes da transferência hospitalar (geralmente em ambulância de luz azul no Reino Unido) a pacientes com suspeita de PAC considerados com risco de vida.[1][65] Siga seu protocolo local.
Considere administrar antibióticos antes da transferência para o hospital (geralmente em ambulância de luz azul no Reino Unido) a pacientes com suspeita de PAC, onde é provável que haja atrasos de mais de 6 horas na internação hospitalar e tratamento.[1][65] Siga seu protocolo local.
Key Recommendations
Avaliação do risco e manejo da PAC nas primeiras 4 horas: ambiente hospitalar[Figure caption and citation for the preceding image starts]: Avaliação do risco e manejo da PAC nas primeiras 4 horas: ambiente hospitalarAdaptado de Lim WS, et al. Thorax. Outubro de 2009; 64 (suplemento 3) :iii1-55 [Citation ends].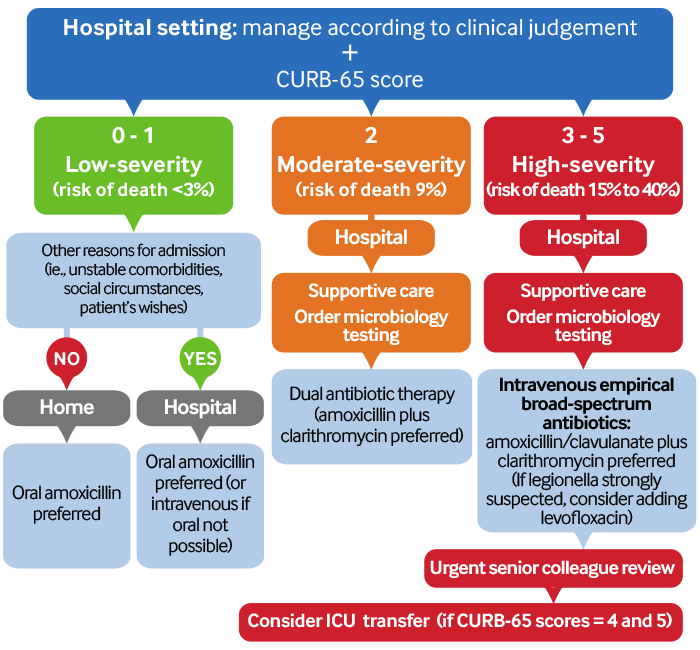
Avaliação do risco e manejo da PAC nas primeiras 4 horas: cenário comunitário[Figure caption and citation for the preceding image starts]: Avaliação do risco e manejo da PAC nas primeiras 4 horas: cenário comunitário. * Considere as circunstâncias sociais, comorbidades instáveis, a capacidade de fazer tratamento oral com segurança e confiabilidade e os desejos do paciente ao decidir se deseja tratá-los em casa. **A maioria dos pacientes com PAC de gravidade moderada deve ser encaminhada ao hospital. No entanto, você deve considerar as circunstâncias sociais, a capacidade de fazer o tratamento oral com segurança, as comorbidades instáveis e os desejos do paciente ao decidir sobre o tratamento domiciliarAdaptado de Lim WS, et al. Thorax. Outubro de 2009; 64 (suplemento 3) :iii1-55 [Citation ends].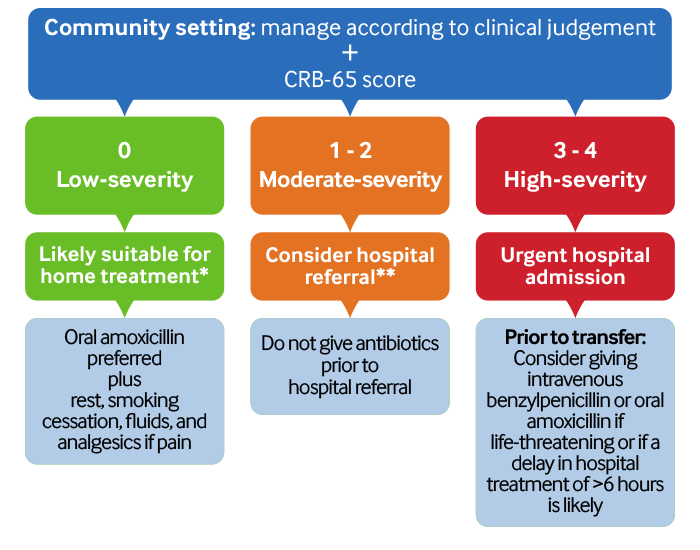
Cuidados de suporte
Administre fluidoterapia intravenosa a pacientes com depleção de volume.[1][65]
Providencie que pacientes com pontuações CURB-65 de 4 e 5 e uma indicação para internação na unidade de terapia intensiva (UTI) sejam transferidos para a UTI e tratados por especialistas da UTI junto com médicos respiratórios. [ Escore CURB-65 de gravidade de uma pneumonia. Opens in new window ] [1][65]
Pacientes com insuficiência respiratória, apesar da oxigenoterapia adequada, necessitam de manejo urgente das vias aéreas e possível intubação.
Não ofereça suporte rotineiro de ventilação não invasiva (VNI) ou pressão positiva contínua nas vias aéreas (CPAP) em pacientes com insuficiência respiratória devido à PAC.[1][65]
Se indicado, você deve realizar um teste de suporte não invasivo somente em uma área de cuidados intensivos onde haja experiência imediata disponível para permitir uma transição rápida para a ventilação invasiva.[1]
Administre analgesia simples (por exemplo, paracetamol) conforme apropriado (por exemplo, para dor pleurítica).[1][65]
Outros tratamentos
Não administre corticosteroides rotineiramente a pacientes com PAC de qualquer gravidade.[1][63][65]
Discuta com um colega sênior pacientes com comorbidades para as quais os corticosteroides são indicados.[63]
Falha em melhorar
Discuta com um colega sênior qualquer paciente que não melhore conforme o esperado.[1][65]
Considere repetir a radiografia torácica, proteína C reativa, contagem de leucócitos e outras amostras para microbiologia em pacientes que não estão progredindo satisfatoriamente após 3 dias de tratamento.[1][65]
Prognóstico
Para pacientes hospitalizados, a taxa de mortalidade varia de 5% a 15%, mas aumenta para entre 20% e 50% em pacientes que necessitam de internação na UTI.[6][118] Os pacientes tratados na comunidade geralmente têm um bom prognóstico.[1]
Determine a gravidade da doença em pacientes com diagnóstico prático de PAC, pois a pneumonia grave está associada a um alto risco de complicações e morte.[64]
Estratifique os pacientes em pacientes com doença de baixa, moderada ou alta gravidade (veja abaixo).[1][63][65]
A identificação precoce da gravidade permite o início da antibioticoterapia apropriada, além de confirmar se o paciente pode ser tratado na comunidade ou precisa ser internado em um hospital onde a ventilação assistida em um ambiente de terapia intensiva pode ser necessária.[1][63][65]
Practical tip
Pense: “ Isso poderia ser sepse?" com base na deterioração aguda em um paciente adulto no qual há evidência clínica ou forte suspeita de infecção.[66][67][68] Consulte Sepse em adultos.
O paciente pode apresentar sintomas inespecíficos ou não localizados (por exemplo, mal-estar agudo com temperatura normal) ou pode haver sinais graves com evidência de disfunção em múltiplos órgãos e choque.[66][67][68]
Lembre-se de que a sepse representa o fim grave e potencialmente fatal da infecção.[79]
A pneumonia é uma das principais fontes de sepse.[80]
Use uma abordagem sistemática (por exemplo, National Early Warning Score 2 [NEWS2]), juntamente com seu julgamento clínico, para avaliar o risco de deterioração devido à sepse.[66][68][69][81] Consulte as diretrizes locais para obter a abordagem recomendada em sua instituição.
Organize uma revisão urgente por um tomador de decisão clínica sênior (por exemplo, médico de nível ST4 no Reino Unido) se você suspeitar de sepse:[70]
Dentro de 30 minutos para um paciente que está gravemente doente (por exemplo, pontuação NEWS2 de 7 ou mais, evidência de choque séptico ou outros problemas clínicos significativos).
Dentro de 1 hora para um paciente gravemente doente (por exemplo, pontuação NEWS2 de 5 ou 6).
Siga seu protocolo local para investigação e tratamento de todos os pacientes com suspeita de sepse ou aqueles em risco. Inicie o tratamento imediatamente. Determine a urgência do tratamento de acordo com a probabilidade de infecção e a gravidade da doença, ou de acordo com seu protocolo local.[70][81]
Na comunidade: encaminhe para atendimento médico de emergência no hospital (geralmente por ambulância de luz azul no Reino Unido) qualquer paciente que esteja gravemente doente com suspeita de infecção e seja:[67]
Considerado de alto risco de deterioração devido à disfunção orgânica (conforme medido pela estratificação de risco)
Com risco de sepse neutropênica.
Use seu julgamento clínico em conjunto com um escore:[1][63][65]
CURB-65 no hospital [ Escore CURB-65 de gravidade de uma pneumonia. Opens in new window ]
CRB-65 na comunidade.
Debate: a importância do julgamento clínico
Seu julgamento clínico é fundamental ao avaliar a gravidade da PAC usando um escore.
Por exemplo, considere um jovem com pressão arterial e nível de ureia normais, mas com baixa saturação de oxigênio, apesar do oxigênio suplementar. Essa pessoa pode ter pneumonia grave, mas você pode não perceber se usar apenas um escore em sua avaliação.[64]
Você deve usar ferramentas de predição de mortalidade, como CURB-65 e CRB-65, para complementar, em vez de substituir, o julgamento clínico ao avaliar a gravidade da PAC.
Consulte um colega sênior sobre a decisão de iniciar antibióticos na primeira oportunidade.[1]
no hospital
Avalie a gravidade usando a pontuação CURB-65 e seu julgamento clínico para identificar pacientes com suspeita de PAC com alto risco de morte, para que você possa priorizar o tratamento imediato e considerar se o paciente deve ser internado.[1][63][65]
Avalie a gravidade regularmente em todos os pacientes com PAC após a internação hospitalar.[1][65]
Uma oportunidade antecipada para isso é dada por um colega sênior e pela equipe médica durante o tempo na enfermaria após a internação.[1]
Pontuação CURB-65: ambiente hospitalar |
|---|
Marque 1 ponto para cada característica presente:
|
|
Discuta pacientes com uma pontuação CURB-65 de 3 ou mais com um colega sênior na primeira oportunidade e trate-os como pneumonia de alta gravidade (veja abaixo).[1][63][65]
Realize uma avaliação emergencial de pacientes com uma pontuação CURB-65 de 4 ou 5 por um especialista em cuidados intensivos.[1][65]
Avaliação do risco e manejo da PAC nas primeiras 4 horas: ambiente hospitalar[Figure caption and citation for the preceding image starts]: Avaliação do risco e manejo da PAC nas primeiras 4 horas: ambiente hospitalarAdaptado de Lim WS, et al. Thorax. Outubro de 2009; 64 (suplemento 3) :iii1-55 [Citation ends].
Siga seu protocolo local ao prescrever antibióticos.As recomendações dadas aqui são baseadas nas diretrizes da British Thoracic Society (BTS).[1][65] Consulte nossa seção Tratamento hospitalar abaixo para obter mais detalhes sobre os esquemas de antibioticoterapia.
Evidências: eficácia do escore de risco de mortalidade CURB-65
O CURB-65 é uma ferramenta prognóstica precisa para prever a mortalidade em pacientes com PAC e é recomendado pela British Thoracic Society (BTS) e pelo National Institute for Health and Care Excellence (NICE) juntamente com o julgamento clínico.[1][63][65]
Foi desenvolvido a partir de três estudos prospectivos no Reino Unido, Nova Zelândia e Holanda, que incluíram mais de 1000 pacientes com PAC.[115]
Estudos de validação foram realizados em vários países (incluindo mais de 3000 pacientes no total). Eles mostraram aumento da mortalidade com o aumento dos escores do CURB-65, variando de 0% a 1.1% (pontuação CURB-65 = 0) a 17% a 60% (pontuação CURB-65 = 5),[119][120][121][122] e aumento da necessidade de ventilação mecânica com o aumento dos escores CURB-65, variando de 0% (pontuação CURB-65 = 0) a 11% (pontuação CURB-65 = 5).[122]
Em um estudo comparando o CURB-65 com o índice de gravidade da pneumonia (PSI), o CURB-65 mostrou igual sensibilidade e maior especificidade (74.6% no CURB-65 vs. 52.2% no PSI) na previsão da mortalidade por PAC.[119]
Outro estudo sugere que o PSI pode ser mais preciso do que o CURB-65 (e o CRB-65) na previsão da mortalidade em 30 dias em pacientes com PAC.[123]
Apesar das evidências emergentes de alguns benefícios do PSI, tanto o NICE quanto a BTS consideram a simplicidade do cálculo da pontuação CURB-65 uma vantagem sobre o PSI.[1][63][65]
Na comunidade
Avalie a gravidade usando o escore CRB-65 junto com seu julgamento clínico para decidir se deve tratar pacientes com suspeita de PAC em casa ou encaminhá-los ao hospital para avaliação ou internação hospitalar.[1][63][65]
Pontuação CRB-65: cenário comunitário |
|---|
Marque 1 ponto para cada característica presente:
|
*Use o Teste Mental Abreviado para avaliar a confusão. Abbreviated Mental Test Score Opens in new window
|
Avaliação de risco e manejo da PAC: cenário comunitário[Figure caption and citation for the preceding image starts]: Avaliação do risco e manejo da PAC nas primeiras 4 horas: cenário comunitário. * Considere as circunstâncias sociais, comorbidades instáveis, a capacidade de fazer tratamento oral com segurança e confiabilidade e os desejos do paciente ao decidir se deseja tratá-los em casa. **A maioria dos pacientes com PAC de gravidade moderada deve ser encaminhada ao hospital. No entanto, você deve considerar as circunstâncias sociais, a capacidade de fazer o tratamento oral com segurança, as comorbidades instáveis e os desejos do paciente ao decidir sobre o tratamento domiciliarAdaptado de Lim WS, et al. Thorax. Outubro de 2009; 64 (suplemento 3) :iii1-55 [Citation ends].
Siga seu protocolo local ao prescrever antibióticos.As recomendações fornecidas aqui são baseadas nas diretrizes da BTS e do NICE.[1][65][117] Consulte nossa seção Tratamento na comunidade abaixo para obter mais detalhes sobre os esquemas de antibioticoterapia.
A - antibióticos
Administre antibióticos empíricos a todos os pacientes com PAC confirmada por radiografia torácica imediatamente após o diagnóstico e dentro de 4 horas após a apresentação ao hospital.[1][65][117]
Procure administrar antibióticos a todos os pacientes com PAC confirmada antes que eles deixem a área de avaliação inicial.[1][65]
Administre antibióticos empíricos a pacientes com doenças que representam risco de vida com base em um diagnóstico clínico presuntivo de PAC e, em seguida, solicite uma radiografia torácica imediata para confirmar o diagnóstico.[1][65]
Para esses pacientes, siga seu protocolo local para investigação e tratamento de todos os pacientes com suspeita de sepse ou aqueles em risco. Inicie o tratamento imediatamente. Determine a urgência do tratamento de acordo com a probabilidade de infecção e a gravidade da doença, ou de acordo com seu protocolo local.[70][81] Consulte Sepse em adultos.
A pneumonia é uma das principais fontes de sepse.[80]
É importante fazer um diagnóstico precoce e preciso da infecção e usar antibióticos adequadamente.
Consulte um colega sênior sobre sua decisão de iniciar antibióticos na primeira oportunidade.[1][65]
Documente claramente a indicação para prescrição de antibióticos nas notas médicas.[1]
Reduza o tratamento assim que apropriado, incluindo a mudança da antibioticoterapia intravenosa para a oral.[1] Ao tomar essa decisão, considere a resposta ao tratamento (veja a dica prática), a mudança na gravidade da doença e as contraindicações à administração oral, como:[1][65]
O paciente é incapaz de engolir (por exemplo, reflexo de deglutição prejudicado, comprometimento da consciência)
Má absorção gastrointestinal por razões funcionais ou anatômicas.
Revise a via de administração inicialmente na enfermaria após a internação e, a seguir, diariamente.[1][65]
Practical tip
Indicadores para a melhora clínica
As seguintes características clínicas devem levar você a considerar a mudança da antibioticoterapia intravenosa para a oral:[1][65]
Frequência de pulso <100 batimentos/minuto
Resolução da taquipneia
Clinicamente hidratado e tomando fluidos orais
Resolução da febre por >24 horas
Resolução da hipotensão
Ausência de hipóxia
Melhorando a contagem de leucócitos
Infecção não bacteriêmica
Nenhuma evidência microbiológica de infecção por legionela, estafilococos ou bacilos entéricos gram-negativos
Nenhuma preocupação com a absorção gastrointestinal.
Considere estreitar o espectro de antibióticos ou mudar para antibióticos direcionados ao patógeno assim que um patógeno causador for identificado.[1][65]
Antibióticos empíricos
Trate a maioria dos pacientes empiricamente, pois o patógeno causador raramente é identificado na avaliação inicial.[1][65]
Prescreva um esquema de antibioticoterapia adequada, de acordo com seu protocolo local para ajudar a reduzir o desenvolvimento de resistência a antibióticos e a infecção por Clostridium difficile.[1][65] Para ajudar na administração de antibióticos, a British Thoracic Society (BTS) recomenda:[1][65]
Administre antibióticos intravenosos empíricos de amplo espectro somente a pacientes com PAC de alta gravidade e reduza o uso de antibióticos de espectro estreito assim que clinicamente apropriado, com base nos resultados de investigações microbiológicas iniciais.[1][65]
Esse grupo compreende aproximadamente um terço de todos os pacientes internados no hospital com PAC confirmada.[1]
Dê antibióticos empíricos a todos os outros pacientes e mude para antibióticos direcionados a patógenos assim que patógenos específicos forem identificados.
Consulte um infectologista sobre a antibioticoterapia apropriada.[1][65]
Consulte os protocolos locais de antibióticos para determinar a escolha mais apropriada com base na prevalência local de patógenos e nos padrões de resistência a antibióticos.
Considere se um diagnóstico correto de PAC foi feito se o pacientenão responder aos antibióticos empíricos iniciais. [1][65]
Considere a revisão clínica e radiográfica para procurar diagnósticos secundários ou complicações da PAC, como derrame pleural/empiema, abscesso pulmonar ou agravamento do sombreamento pneumônico.[1]
Considere mudar os antibióticos empíricos iniciais, mas primeiro considere a adesão e a absorção adequada de um esquema oral.[1]
As recomendações a seguir são baseadas nas diretrizes da BTS e do National Institute for Health and Care Excellence (NICE).[1][65][117]
PAC de alta gravidade (pontuação CURB-65: 3 ou mais)
Sempre trate pacientes com PAC de alta gravidade no hospital.[1]
Administre antibióticos intravenosos empíricos de amplo espectro imediatamente após o diagnóstico e até 4 horas após a apresentação ao hospital.[1][65][117]
Evidência: tempo até o primeiro antibiótico dentro de 4 horas após a apresentação
O estudo do pacote de cuidados da BTS para PAC foi realizado em 2013 em 16 fundos hospitalares do Reino Unido.
O pacote de cuidados para PAC consistia em quatro elementos:
Uma radiografia torácica obtida dentro de 4 horas da internação hospitalar em todos os adultos com suspeita de PAC
Avaliação e prescrição de oxigênio de acordo com a diretriz de oxigênio da BTS[71]
Avaliação de gravidade suportada pela pontuação CURB-65
Antibióticos oportunos e direcionados administrados de acordo com a gravidade da PAC dentro de 4 horas após a internação.
O estudo comparou pacientes com PAC que receberam o pacote de tratamento para PAC com aqueles que receberam o padrão de cuidados. A análise de dados de 2118 adultos (idade média de 75.3 anos) mostrou que significativamente mais pacientes no grupo do pacote de tratamento para PAC receberam antibióticos dentro de 4 horas após a internação (razão de chances [RC] ajustada 1.52, IC de 95% 1.08 a 2.14, P = 0.016) e que a mortalidade hospitalar em 30 dias foi menor nesse grupo (8.8% versus 13.6%; razão de chances [RC] ajustada 0.59, IC de 95% 0.37 a 0.95, P = 0.03).[124]
Administre uma penicilina resistente à betalactamase de amplo espectro (por exemplo, amoxicilina/clavulanato) associada a um macrolídeo(por exemplo, claritromicina).[1][65]
A diretriz da BTS recomenda adicionar uma fluoroquinolona ao esquema empírico existente (ou seja, terapia tripla) se o paciente não responder ou se houver forte suspeita de pneumonia por legionella.[1][65] No entanto, na prática, existem preocupações sobre o risco de usar um macrolídeo e uma fluoroquinolona juntos, pois ambos podem prolongar o intervalo QT. Alguns médicos, portanto, substituem o macrolídeo no esquema empírico original por uma fluoroquinolona (ou seja, terapia dupla). Considere as questões de segurança associadas ao uso de fluoroquinolona. Consulte um microbiologista e um colega sênior antes de tratar esses pacientes.
Diretrizes mais recentes (2019) do NICE sobre prescrição de antimicrobianos em adultos também recomendam amoxicilina/clavulanato associado a claritromicina (ou eritromicina) como primeira linha em pessoas com PAC de alta gravidade. Essas recomendações são baseadas principalmente na opinião de especialistas, pois as evidências são limitadas.[117]
Para pacientes alérgicos à penicilina, administre uma cefalosporina de segunda geração (por exemplo, cefuroxima) ou uma cefalosporina de terceira geração (por exemplo, cefotaxima ou ceftriaxona) associada a um macrolídeo (por exemplo, claritromicina).[1][65]
Um pequeno número de pacientes é alérgico tanto às penicilinas quanto às cefalosporinas; consulte um especialista em doenças infecciosas para selecionar os antibióticos apropriados para esses pacientes.
As diretrizes do NICE sobre prescrição de antimicrobianos em adultos recomendam a levofloxacina (após considerar as questões de segurança associadas ao uso de fluoroquinolona) como um antibiótico alternativo para pacientes com PAC de alta gravidade que são alérgicos à penicilina.[117]
Analise a necessidade de antibióticos intravenosos inicialmente durante o tempo na enfermaria após a internação e depois todos os dias.[1][65]
As diretrizes do NICE sobre prescrição de antimicrobianos em adultos recomendam revisar os antibióticos intravenosos em 48 horas e considerar a mudança para o tratamento oral, se possível.[117] A melhor prática é revisar os antibióticos intravenosos todos os dias; a maioria dos antibióticos intravenosos pode ser interrompida e transferida para tratamento oral em 24 horas.
Mude para antibióticos orais assim que ocorrer melhora clínica (veja a dica prática acima para obter dicas de melhora clínica) e desde que não haja contraindicações à administração oral, como:[1][65]
O paciente é incapaz de engolir (por exemplo, reflexo de deglutição prejudicado, comprometimento da consciência)
Má absorção gastrointestinal por razões funcionais ou anatômicas.
Administre antibioticoterapia por 5 dias.[117][125] O NICE recomenda:[117]
Prescrever o ciclo mais curto que provavelmente seja eficaz para reduzir o risco de resistência antimicrobiana e minimizar o risco de efeitos adversos[117]
Interromper o tratamento após 5 dias, a menos que os resultados microbiológicos sugiram um ciclo mais longo ou que o paciente não esteja clinicamente estável.Isso deve ser baseado em seu julgamento clínico e nos seguintes critérios:[117][126]
Febre nas últimas 48 horas ou mais de um sinal de instabilidade clínica:
Pressão arterial sistólica <90 mmHg
Frequência cardíaca >100/minuto
Frequência respiratória >24/minuto
Saturação de oxigênio no sangue arterial <90% ou PaO 2 <60 mmHg no ar ambiente.
Em algumas pessoas, ciclos mais longos podem ser necessários devido a circunstâncias individuais. No Reino Unido, alguns hospitais precisam consultar a equipe de microbiologia se considerarem estender a duração do tratamento com antibióticos para além de 5 dias na PAC de alta gravidade.Siga seu protocolo local.
As diretrizes do NICE não fornecem um limite máximo para a duração do ciclo de antibióticos. Isso será determinado em circunstâncias individuais, com base no tempo necessário para alcançar a estabilidade clínica.[117]
PAC de gravidade moderada (pontuação CURB-65: 2)
Administre antibióticos o mais rápido possível após o diagnóstico e dentro de 4 horas após a apresentação ao hospital.[1][65][117]
Considere pacientes com PAC de gravidade moderada para tratamento hospitalar de curta duração ou tratamento ambulatorial supervisionado por hospital.[1][65]
Evidência: tempo até o primeiro antibiótico dentro de 4 horas após a apresentação
O estudo do pacote de cuidados da BTS para PAC foi realizado em 2013 em 16 fundos hospitalares do Reino Unido.
O pacote de cuidados para PAC consistia em quatro elementos:
Uma radiografia torácica obtida dentro de 4 horas da internação hospitalar em todos os adultos com suspeita de PAC.
Avaliação e prescrição de oxigênio de acordo com a diretriz de oxigênio da BTS[71]
Avaliação de gravidade suportada pela pontuação CURB-65
Antibióticos oportunos e direcionados administrados de acordo com a gravidade da PAC dentro de 4 horas após a internação.
O estudo comparou pacientes com PAC que receberam o pacote de tratamento para PAC com aqueles que receberam o padrão de cuidados. A análise de dados de 2118 adultos (idade média de 75.3 anos) mostrou que significativamente mais pacientes no grupo do pacote de tratamento para PAC receberam antibióticos ≤4 horas após a internação (RC ajustada 1.52, IC de 95% 1.08 a 2.14, P = 0.016) e que a mortalidade hospitalar em 30 dias foi menor nesse grupo (8.8% versus 13.6%; RC ajustada 0.59, IC de 95% 0.37 a 0.95, P = 0.03).[124]
A maioria dos pacientes com PAC de gravidade moderada pode ser tratada com antibioticoterapia oral dupla. A escolha preferida é a amoxicilina associada a um macrolídeo (por exemplo, claritromicina).[1][65]
As diretrizes NICE sobre prescrição de antimicrobianos em adultos recomendam a monoterapia com amoxicilina em pessoas com PAC de gravidade moderada, com a adição de claritromicina (ou eritromicina) somente se houver suspeita de um patógeno atípico. Essas recomendações são baseadas principalmente na opinião de especialistas, pois as evidências são limitadas.[117]
Considere a monoterapia com um macrolídeo para pacientes que foram tratados na comunidade e que não responderam a um ciclo adequado de amoxicilina antes da internação hospitalar.[1][65]
Decidir se o ciclo da amoxicilina foi adequado é complicado e envolve julgamento clínico. Consulte um médico sênior antes de prescrever a monoterapia nas primeiras 24 horas após a internação.[1][65]
Se os antibióticos orais forem contraindicados (por exemplo, o paciente não consegue engolir ou tem má absorção gastrointestinal por razões funcionais ou anatômicas), administre amoxicilina ou benzilpenicilina intravenosa, associada a claritromicina.[1][65]
Para pacientes alérgicos à penicilina ou macrolídeos, considere a doxiciclina oral.[1][65] As opções alternativas incluem levofloxacina ou moxifloxacina oral (após considerar as questões de segurança associadas ao uso de fluoroquinolona).[1][65]
As diretrizes NICE sobre prescrição de antimicrobianos em adultos com PAC recomendam doxiciclina ou claritromicina em pessoas alérgicas à penicilina.[117]
Para pacientes alérgicos à penicilina nos quais antibióticos orais são contraindicados, administre uma cefalosporina de segunda geração (por exemplo, cefuroxima) ou uma cefalosporina de terceira geração (por exemplo, cefotaxima ou ceftriaxona) associada a claritromicina ou levofloxacina intravenosa como monoterapia.[1][65]
Se o paciente não responder a uma combinação de amoxicilina e claritromicina, considere mudar o tratamento para doxiciclina ou uma fluoroquinolona com cobertura pneumocócica eficaz.[1][65]
Mais informações: restrições da EMA e da MHRA ao uso de antibióticos fluoroquinolonas
Em novembro de 2018, a European Medicines Agency (EMA) concluiu uma revisão dos efeitos adversos graves, incapacitantes e potencialmente irreversíveis associados aos antibióticos da classe de fluoroquinolonas sistêmicos e por via inalatória. Entre os efeitos adversos estão tendinite, ruptura de tendão, artralgia, neuropatias e outros efeitos sobre os sistemas musculoesquelético ou nervoso.
Como consequência desta revisão, a EMA agora recomenda que os antibióticos fluoroquinolonas sejam restritos para uso apenas em infecções bacterianas graves e potencialmente fatais. Além disso, ela recomenda que a fluoroquinolona não seja usada para infecções leves a moderadas, a menos que outros antibióticos adequados à infecção específica não possam ser usados; e que também não seja usada para tratar infecções não graves, não bacterianas ou autolimitadas. Pacientes idosos e os que apresentam comprometimento renal ou tenham sofrido transplante de órgãos sólidos e aqueles tratados com corticosteroides têm maior risco de danos nos tendões. Deve-se evitar a coadministração de uma fluoroquinolona e um corticosteroide.[127] A Medicines and Healthcare Products Regulatory Agency (MHRA), sediada no Reino Unido, apoia essas recomendações.[128]
Por esse motivo, as fluoroquinolonas só devem ser consideradas na PAC de gravidade moderada quando for considerado inadequado o uso de outros antibióticos comumente recomendados para o tratamento da PAC.Consulte um infectologista para saber se uma fluoroquinolona é uma opção apropriada para seu paciente.
Analise a necessidade de antibióticos intravenosos inicialmente na enfermaria após a internação e depois todos os dias.[1][65]
As diretrizes do NICE sobre prescrição de antimicrobianos em adultos recomendam revisar os antibióticos intravenosos em 48 horas e considerar a mudança para o tratamento oral, se possível.[117] A melhor prática é revisar os antibióticos intravenosos todos os dias; a maioria dos antibióticos intravenosos pode ser interrompida e transferida para tratamento oral em 24 horas.
Mude para antibióticos orais assim que ocorrer melhora clínica (veja dica prática) e desde que não haja contraindicações à administração oral, como:[1][65]
O paciente é incapaz de engolir (por exemplo, reflexo de deglutição prejudicado, comprometimento da consciência)
Má absorção gastrointestinal por razões funcionais ou anatômicas.
Practical tip
Indicadores para a melhora clínica
As seguintes características clínicas devem levar você a considerar a mudança da antibioticoterapia intravenosa para a oral:[1][65]
Frequência de pulso <100 batimentos/minuto
Resolução da taquipneia
Clinicamente hidratado e tomando fluidos orais
Resolução da febre por >24 horas
Resolução da hipotensão
Ausência de hipóxia
Melhorando a contagem de leucócitos
Infecção não bacteriêmica
Nenhuma evidência microbiológica de infecção por legionela, estafilococos ou bacilos entéricos gram-negativos
Nenhuma preocupação com a absorção gastrointestinal.
Administre antibioticoterapia por 5 dias.[117][125] O NICE recomenda:[117]
Prescrever o ciclo mais curto que provavelmente seja eficaz para reduzir o risco de resistência antimicrobiana e minimizar o risco de efeitos adversos
Interromper o tratamento após 5 dias, a menos que os resultados microbiológicos sugiram um ciclo mais longo ou que o paciente não esteja clinicamente estável. Isso deve ser baseado em seu julgamento clínico e nos seguintes critérios:[117][126]
Febre nas últimas 48 horas ou mais de um sinal de instabilidade clínica:
Pressão arterial sistólica <90 mmHg
Frequência cardíaca >100/minuto
Frequência respiratória >24/minuto
Saturação de oxigênio no sangue arterial <90% ou PaO 2 <60 mmHg no ar ambiente.
Um ECRC constatou que, em pacientes com PAC moderadamente grave que atendem aos critérios de estabilidade clínica, a descontinuação do tratamento com betalactâmicos após 3 dias não foi inferior ao tratamento de 8 dias; isso sugere que 3 dias de antibióticos podem ser suficientes em pacientes imunocompetentes sem doença grave que apresentam melhora clínica no dia 3.[129]
Em algumas pessoas, ciclos mais longos podem ser necessários devido a circunstâncias individuais. No Reino Unido, alguns hospitais precisam consultar a equipe de infectologia se considerarem estender a duração do tratamento com antibióticos para além de 5 dias na PAC de gravidade moderada.Siga seu protocolo local.
As diretrizes do NICE não fornecem um limite máximo para a duração do ciclo de antibióticos. Isso será determinado em circunstâncias individuais, com base no tempo necessário para alcançar a estabilidade clínica.[117]
PAC de baixa gravidade (pontuação CURB-65: 0-1)
Administre antibióticos o mais rápido possível e dentro de 4 horas após a apresentação ao hospital.[1][65][117]
Evidência: tempo até o primeiro antibiótico dentro de 4 horas após a apresentação
O estudo do pacote de cuidados da BTS para PAC foi realizado em 2013 em 16 fundos hospitalares do Reino Unido.
O pacote de cuidados para PAC consistia em quatro elementos:
Uma radiografia torácica obtida dentro de 4 horas da internação hospitalar em todos os adultos com suspeita de PAC
Avaliação e prescrição de oxigênio de acordo com a diretriz de oxigênio da BTS[71]
Avaliação de gravidade suportada pela pontuação CURB-65
Antibióticos oportunos e direcionados administrados de acordo com a gravidade da PAC dentro de 4 horas após a internação.
O estudo comparou pacientes com PAC que receberam o pacote de tratamento para PAC com aqueles que receberam o padrão de cuidados. A análise de dados de 2118 adultos (idade média de 75.3 anos) mostrou que significativamente mais pacientes no grupo do pacote de tratamento para PAC receberam antibióticos ≤4 horas após a internação (RC ajustada 1.52, IC de 95% 1.08 a 2.14, P = 0.016) e que a mortalidade hospitalar em 30 dias foi menor nesse grupo (8.8% versus 13.6%; RC ajustada 0.59, IC de 95% 0.37 a 0.95, P = 0.03).[124]
A maioria dos pacientes com PAC de baixa gravidade que são tratados no hospital pode ser tratada com antibióticos orais.[1][65] A escolha preferida é a amoxicilina.[1][65] Considere um macrolídeo (por exemplo, claritromicina) ou uma tetraciclina (por exemplo, doxiciclina) para pacientes alérgicos à penicilina.[1][65]
O NICE recomenda claritromicina (ou eritromicina) ou doxiciclina como alternativas à amoxicilina para pacientes alérgicos à penicilina e para pacientes nos quais a amoxicilina é inadequada (por exemplo, se houver suspeita de pneumonia atípica). As recomendações do NICE são baseadas principalmente na opinião de especialistas, pois as evidências são limitadas.[117]
Se a via oral for contraindicada (por exemplo, comprometimento do reflexo de deglutição, comprometimento da consciência, má absorção gastrointestinal), considere amoxicilina intravenosa, benzilpenicilina ou claritromicina.[1][65]
Analise a necessidade de antibióticos intravenosos inicialmente durante o tempo na enfermaria após a internação e depois todos os dias.[1][65] As diretrizes do NICE sobre prescrição de antimicrobianos em adultos recomendam revisar os antibióticos intravenosos em 48 horas e considerar a mudança para o tratamento oral, se possível.[117] A melhor prática é revisar os antibióticos intravenosos todos os dias; a maioria dos antibióticos intravenosos pode ser interrompida e transferida para tratamento oral em 24 horas.
Mude para antibióticos orais assim que ocorrer melhora clínica (ver dica prática) e desde que não haja contraindicações à administração oral.[1][117][65]
Practical tip
Indicadores para a melhora clínica
As seguintes características clínicas devem levar você a considerar a mudança da antibioticoterapia intravenosa para a oral:[1][65]
Frequência de pulso <100 batimentos/minuto
Resolução da taquipneia
Clinicamente hidratado e tomando fluidos orais
Resolução da febre por >24 horas
Resolução da hipotensão
Ausência de hipóxia
Melhorando a contagem de leucócitos
Infecção não bacteriêmica
Nenhuma evidência microbiológica de infecção por legionela, estafilococos ou bacilos entéricos gram-negativos
Nenhuma preocupação com a absorção gastrointestinal.
Se o paciente não responderà monoterapia com amoxicilina, considere mudar ou adicionar um macrolídeo (por exemplo, claritromicina).[1][65]
Administre antibioticoterapia por 5 dias.[117][125] O NICE recomenda:[117]
Prescrever o ciclo mais curto que provavelmente seja eficaz para reduzir o risco de resistência antimicrobiana e minimizar o risco de efeitos adversos
Interromper o tratamento após 5 dias, a menos que os resultados microbiológicos sugiram um ciclo mais longo ou que o paciente não esteja clinicamente estável.Isso deve ser baseado em seu julgamento clínico e nos seguintes critérios:[117][126]
Febre nas últimas 48 horas ou mais de um sinal de instabilidade clínica:
Pressão arterial sistólica <90 mmHg
Frequência cardíaca >100/minuto
Saturação de oxigênio no sangue arterial <90% ou PaO 2 <60 mmHg no ar ambiente.
Tratamento antibiótico direcionado a patógenos
Mude de antibióticos empíricos para antibióticos direcionados a patógenos assim que patógenos específicos forem identificados (a menos que haja preocupações legítimas sobre a infecção por patógenos duplos).[1][65]
Consulte um infectologista sobre a antibioticoterapia apropriada.[1][65]
Apenas cerca de um terço a um quarto dos pacientes com PAC internados no hospital terão sua pneumonia definida microbiologicamente.[1] Entre esses pacientes:
Cerca de 14% têm um patógeno atípico, dos quais:[21]
7% têm Mycoplasma pneumoniae
4% têm Chlamydophila pneumoniae
3% têm Legionella pneumophila
Aqueles com infecções causadas por organismos como Mycoplasma, Chlamydophila e Coxiella burnetii serão diagnosticados com a doença mais avançada, com base na soroconversão, reduzindo a oportunidade de terapia direcionada precoce.[1] Entre os pacientes tratados na comunidade, muito poucos serão definidos microbiologicamente.[1]
Considere trocar o tratamento assim que os resultados do teste de sensibilidade estiverem disponíveis ou após consulta com um microbiologista, intensivista ou médico respiratório.[1]
Recomendações da BTS para antibióticos direcionados a patógenos[1][65]
Patógeno | Antibiótico preferido | antibiótico alternativo |
|---|---|---|
Pneumonia por micoplasma Chlamydophila pneumoniae | Claritromicina (por via oral ou intravenosa) | Doxiciclina (por via oral) ou uma fluoroquinolona (por via oral ou intravenosa) |
Espécies de Legionella | Fluoroquinolona (por via oral ou intravenosa) | Claritromicina (por via oral ou intravenosa) ou azitromicina (em países onde é usada para controlar a pneumonia) |
Streptococcus pneumoniae | Amoxicilina (por via oral) ou benzilpenicilina (por via intravenosa) | Claritromicina (por via oral) ou cefuroxima ou cefotaxima ou ceftriaxona (por via intravenosa) |
Chlamydia psittaci Coxiella burnetii | Doxiciclina (por via oral) | Claritromicina (por via oral ou intravenosa) |
Haemophilus influenzae | Não produtor de betalactamase: amoxicilina (por via oral ou intravenosa) Produtor de betalactamase: amoxicilina/ácido clavulânico (por via oral ou intravenosa) | Cefuroxima ou cefotaxima ou ceftriaxona (por via intravenosa) ou uma fluoroquinolona (por via oral ou intravenosa) |
Bacilos entéricos gram-negativos | Cefuroxima ou cefotaxima ou ceftriaxona (por via intravenosa) | Fluoroquinolona (por via intravenosa) ou imipenem/cilastatina (por via intravenosa) ou meropenem (por via intravenosa) |
Pseudomonas aeruginosa | Ceftazidima (por via intravenosa) associado a Gentamicina ou tobramicina (é necessário monitorar a dose) | Ciprofloxacino (por via intravenosa) ou piperacilina/tazobactam (por via intravenosa) associado a Gentamicina ou tobramicina (é necessário monitorar a dose) |
Staphylococcus aureus: não MRSA | Flucloxacilina (por via intravenosa) com ou sem Rifampicina (por via oral ou intravenosa) | |
Staphylococcus aureus: MRSA | Vancomicina (por via intravenosa; é necessário monitorar a dose) ou linezolida (por via intravenosa) ou teicoplanina (por via intravenosa) com ou sem Rifampicina (por via oral ou intravenosa) |
Cuidados de suporte
Ofereça cuidados de suporte aos pacientes tratados no hospital.Isso pode incluir as seguintes medidas.[1][65]
Oxigênio
Avalie a saturação de oxigênio em todos os pacientes por oximetria de pulso (preferencialmente em ar ambiente).
Forneça oxigênio se a saturação de oxigênio estiver <94% e mantenha-na na faixa alvo.[1][65] Nos pacientes com risco de retenção de CO2, administre oxigênio se a saturação de oxigênio estiver <88%. Uma avaliação precoce do oxigênio está associada a um melhor prognóstico.[71]
Monitore a oxigenoterapia controlada. Um limite superior de 96% para a SpO2 é razoável quando se administra oxigênio suplementar à maioria dos pacientes com uma doença aguda que não tem risco de hipercapnia.
As evidências sugerem que o uso liberal de oxigênio suplementar (SpO2 alvo >96%) em adultos com uma doença aguda está associado a maior mortalidade do que uma oxigenoterapia mais conservadora.[72]
Uma meta de SpO2 mais baixa, de 88% a 92%, é apropriada se o paciente estiver em risco de insuficiência respiratória hipercápnica.[71]
Evidência: Saturação alvo de oxigênio em adultos com doenças agudas
Oxigênio suplementar em excesso aumenta a mortalidade.
As evidências de uma grande revisão sistemática e meta-análise apoiam a oxigenoterapia conservadora/controlada versus a oxigenoterapia liberal nos adultos com uma doença aguda que não tiverem risco de hipercapnia.
As diretrizes diferem em suas recomendações sobre a saturação alvo de oxigênio nos adultos agudamente doentes que estiverem recebendo oxigênio suplementar.
A diretriz da British Thoracic Society (BTS) de 2017 recomenda uma faixa alvo de 94% a 98% para a SpO2 para os pacientes sem risco de hipercapnia, enquanto a diretriz da Thoracic Society of Australia and New Zealand (TSANZ) de 2022 recomenda 92% a 96%.[71][130]
As diretrizes da Global Initiative for Asthma (GINA) de 2022 recomendam uma faixa alvo de 93% a 96% para a SpO2 no contexto de exacerbações agudas da asma.[131]
Uma revisão sistemática, incluindo uma metanálise de dados de 25 ensaios clínicos randomizados publicada em 2018, descobriu que em adultos com uma doença aguda, a oxigenoterapia liberal (geralmente equivalente a uma saturação alvo >96%) está associada a uma mortalidade maior do que a oxigenoterapia conservadora (geralmente equivalente a uma saturação alvo ≤96%).[72] A mortalidade hospitalar foi 11 por 1000 maior para o grupo da oxigenoterapia liberal versus o grupo da terapia conservadora (IC de 95%: 2 a 22 por 1000 a mais). A mortalidade em 30 dias também foi maior no grupo que recebeu oxigênio liberal (RR 1,14, IC 95% 1,01 a 1,29). Os ensaios incluíram adultos com sepse, doença crítica, derrame, trauma, infarto do miocárdio, parada cardíaca e pacientes submetidos a cirurgia de emergência. Os estudos foram limitados porque as pessoas com doenças respiratórias crônicas ou psiquiátricas, ou pacientes em suporte extracorpóreo à vida, recebendo oxigenoterapia hiperbárica ou submetidos a cirurgia eletiva, foram todos excluídos da revisão.
Portanto, um limite superior de 96% para a SpO2 é razoável ao se administrar oxigênio suplementar aos pacientes com doença aguda que não têm risco de hipercapnia. No entanto, um alvo mais alto pode ser apropriado para algumas condições específicas (por exemplo, pneumotórax, intoxicação por monóxido de carbono, cefaleia em salvas e crise falciforme).[132]
Em 2019, o BTS revisou sua orientação em resposta a essa revisão sistemática e metanálise e decidiu que uma atualização provisória não era necessária.[113]
O comitê observou que a revisão sistemática apoiou o uso da oxigenoterapia controlada até uma meta.
Embora a revisão sistemática tenha mostrado uma associação entre maiores saturações de oxigênio e maior mortalidade, o comitê do BTS considerou que a revisão não foi definitiva sobre qual deveria ser a faixa alvo ideal. O intervalo sugerido de 94% a 96% na revisão foi baseado no menor intervalo de confiança de 95% e na mediana da SpO2 basal dos grupos do oxigênio liberal, juntamente com a recomendação anterior da diretriz TSANZ de 2015.
Posteriormente, a experiência durante a pandemia de COVID-19 também tornou os médicos mais conscientes da viabilidade de uma hipoxemia permissiva.[133]
O manejo da oxigenoterapia nos pacientes em terapia intensiva é especializado e informado por evidências adicionais que são mais específicas para esse cenário.[134][135][136]
Meça a gasometria arterial nas pessoas com SpO2 <94%, naqueles com risco de insuficiência ventilatória hipercápnica (retenção de CO2) e em todos os pacientes com PAC de alta gravidade.[1][65]
Practical tip
Sempre registre claramente a concentração de oxigênio inspirado, pois isso é essencial para interpretar os resultados da gasometria.
Cuidados de suporte padrão na unidade de terapia intensiva (UTI)
Providencie que os pacientes com escores CURB-65 de 4 e 5 e uma indicação de internação em UTI sejam transferidos para a UTI e tratados por especialistas em terapia intensiva juntamente com pneumologistas.[1][65]
Pacientes com insuficiência respiratória, apesar da oxigenoterapia adequada, necessitam de manejo urgente das vias aéreas e possível intubação.
Não ofereça suporte com ventilação não invasiva (VNI) ou pressão positiva contínua nas vias aéreas (CPAP) de maneira rotineira nos pacientes com insuficiência respiratória devida a uma PAC.[1][65]
Se indicado, você deve realizar um teste de suporte não invasivo somente em uma área de cuidados intensivos onde haja experiência imediata disponível para permitir uma transição rápida para a ventilação invasiva.[1][65]
Vasopressores
Inicie vasopressores se o paciente estiver hipotenso durante ou após a ressuscitação fluídica para manter um nível médio da pressão arterial ≥65 mmHg.[137]
Fluidoterapia intravenosa
Avalie todos os pacientes quanto a depleção de volume e administre fluidoterapia intravenosa, se necessária.[1][65]
Profilaxia para tromboembolismo venoso
Considere a profilaxia para tromboembolismo venoso com heparina de baixo peso molecular para todos os pacientes que não tiverem mobilidade total.[1][65]
Suporte nutricional
Providencie suporte nutricional(seja enteral, parenteral ou via alimentação nasogástrica) para os pacientes com PAC grave que necessitarem de uma internação hospitalar prolongada.[1][65]
Desobstrução das vias aéreas
Não trate as pessoas com pneumonia não complicada com técnicas tradicionais de desobstrução das vias aéreas de maneira rotineira. Se necessário, ofereça conselhos a esses pacientes sobre a expectoração do escarro.[1][65]
Considere técnicas de desobstrução das vias aéreas se o paciente tiver dificuldade em expectorar o escarro ou tiver uma doença pulmonar preexistente.[1][65]
Analgesia
Administre analgesia simples (por exemplo, paracetamol) conforme apropriado (por exemplo, para uma dor pleurítica).[1][65]
Practical tip
Incentive os pacientes com PAC não complicada (ou seja, não complicada pela presença de derrame parapneumônico, empiema, abscesso, pneumotórax, pneumonia necrosante ou fístula broncopleural), cujo quadro clínico lhes permitir a sentarem-se fora do leito. Inicialmente, almeje pelo menos 20 minutos nas primeiras 24 horas e, em seguida, aumente a mobilidade a cada dia subsequente de hospitalização.
Outros tratamentos
Corticosteroides
Não administre corticosteroides aos pacientes com PAC de qualquer gravidade de maneira rotineira.[1][63][65]
Discuta com um colega experiente os pacientes com comorbidades para os quais os corticosteroides são indicados.[63]
Debate: Tratamento com corticosteroides na PAC
As evidências mais recentes sugerem que os corticosteroides administrados como adjuvantes do tratamento com antibióticos melhoram os desfechos em adultos com PAC, mas aumentam o risco de hiperglicemia. A recomendação do NICE de não administrar corticosteroides rotineiramente permanece válida até que mais evidências estejam disponíveis.
Uma revisão Cochrane, incluindo 17 estudos, avaliou a segurança e a eficácia dos corticosteroides administrados como adjuvantes ao tratamento com antibióticos em adultos e crianças com pneumonia (PAC, pneumonia hospitalar e pneumonia associada a ventilação mecânica). A intervenção incluiu prednisolona oral em 3 ensaios e dexametasona, hidrocortisona ou metilprednisolona intravenosas em 13 ensaios. Os resultados sugerem que os corticosteroides reduziram significativamente a mortalidade e a morbidade nos pacientes com PAC de alta gravidade. Eles também reduziram a morbidade, embora não a mortalidade, nos pacientes com PAC de gravidade moderada ou baixa. A hiperglicemia foi o evento adverso mais comum nos adultos tratados com corticosteroides; no entanto, os autores concluíram que, em geral, os benefícios superam os danos.[138]
Duas revisões sistemáticas (publicadas antes da revisão Cochrane) também analisaram a segurança e a eficácia dos glicocorticoides adjuvantes para os pacientes com PAC.[139][140] Elas não mostraram nenhuma diferença significativa na mortalidade por todas as causas, e relataram reduções significativas no tempo de permanência na UTI,[139] na duração da internação hospitalar,[139][140] e no período de tempo até a estabilidade clínica nos grupos dos corticosteroides.[139][140] Uma das revisões relatou um aumento do risco de hiperglicemia nos pacientes tratados com corticosteroides.[140]
O NICE deve revisar essa área quando os resultados de dois ensaios em andamento forem publicados. Por enquanto, a recomendação de não administrar corticosteroides rotineiramente permanece válida.[63]
Monitoramento
Medições para observação inicialmente pelo menos duas vezes ao dia e com mais frequência (por exemplo, a cada hora) nas pessoas internadas em uma unidade para pacientes críticos (unidade de alta dependência ou UTI).[1][65] Monitore:
Pulso
Pressão arterial
Frequência respiratória
Temperatura
Saturação de oxigênio (com um registro da saturação de oxigênio inspirado ao mesmo tempo)
Estado mental.
Considere medir a concentração de proteína C reativa basal nos pacientes com PAC à admissão hospitalar, e repita o teste se a evolução clínica for incerta após 48 a 72 horas.[1][63][65]
Revise todos os pacientes com PAC de alta gravidade pelo menos a cada 12 horas até que ocorra melhora clínica.[1][65] Isso deve ser feito por um colega sênior e pela equipe médica.[1][65]
Practical tip
Indicadores para a melhora clínica
As seguintes características clínicas devem levar você a considerar a mudança da antibioticoterapia intravenosa para a oral:[1][65]
Frequência de pulso <100 batimentos/minuto
Resolução da taquipneia
Clinicamente hidratado e tomando fluidos orais
Resolução da febre por >24 horas
Resolução da hipotensão
Ausência de hipóxia
Melhorando a contagem de leucócitos
Infecção não bacteriêmica
Nenhuma evidência microbiológica de infecção por legionela, estafilococos ou bacilos entéricos gram-negativos
Nenhuma preocupação com a absorção gastrointestinal.
Avalie a gravidade regularmente em todos os pacientes com PAC após a admissão hospitalar.[1][65] Uma oportunidade inicial para isso é a visita logo após a admissão por um colega sênior e pela equipe médica.[1][65]
Para obter mais informações sobre complicações relacionadas à PAC, consulte nossa seção separada de Complicações.
Falha em melhorar
Discuta com um colega sênior qualquer paciente que não melhore conforme o esperado.[1][65]
Considere repetir a radiografia torácica, a proteína C-reativa, a contagem leucocitária e outras amostras para microbiologia nos pacientes que não evoluírem satisfatoriamente após 3 dias de tratamento.[1][65]
Practical tip
Os principais motivos pelos quais os pacientes não melhoram conforme o esperado incluem:[1][65]
Diagnóstico incorreto ou condição complicadora (por exemplo, embolia pulmonar, carcinoma brônquico, bronquiectasia)
Patógeno inesperado ou patógenos não cobertos pela escolha de antibióticos (por exemplo, patógenos “atípicos”, patógenos resistentes a antibióticos comumente usados, como Haemophilus influenzae resistente à ampicilina)
Antibiótico inefetivo ou causador de reação alérgica (por exemplo, má absorção do antibiótico oral, dose inadequada, hipersensibilidade ao antibiótico)
Defesas locais (por exemplo, bronquiectasia, obstrução endobrônquica, aspiração) ou sistêmicas (por exemplo, infecção por HIV, mieloma) prejudicadas
Complicações locais (por exemplo, derrame parapneumônico, empiema, abscesso pulmonar) ou distantes (por exemplo, infecção metastática, septicemia, flebite no local da cânula intravenosa) da PAC
Infecção avassaladora
Melhora esperada prematuramente (por exemplo, nos pacientes idosos).
Alta hospitalar
Não dê rotineiramente alta aos pacientes se eles tiverem 2* ou mais dos seguintes achados presentes nas últimas 24 horas:[63]
Temperatura >37.5°C (>99.5°F)
Frequência cardíaca >100/minuto
Frequência respiratória ≥24/minuto
Pressão arterial sistólica ≤90 mmHg
Saturação de oxigênio <90% em ar ambiente
Incapacidade de manter a ingestão oral
Estado mental anormal.
(*A BTS recomenda basear sua decisão de dar alta aos pacientes com PAC em 1 ou mais das descobertas listadas [a menos que representem o estado basal usual desse paciente] e usa um limiar de temperatura de 37.8° C [100.04° F]. Veja +Debate abaixo.[1][65])
Considere adiar a alta dos pacientes com PAC se a temperatura estiver superior a 37.5° C (99.5° F).[63]
Debate: Temperatura de corte para uma alta segura
A BTS considera uma temperatura >37.8°C (>100.04°F), em vez do limiar de >37.5°C (>99.5°F) recomendado pelo NICE, como um achado levá-lo a considerar o adiamento da alta em um paciente com PAC.[1][65]
O limiar >37.5°C (>99.5°F) recomendado pelo NICE é baseado nas conclusões de um estudo de coorte prospectivo que analisou o valor de variáveis clínicas simples para prever desfechos de curto prazo em pacientes com pneumonia.[63][141]
Ele descobriu que um ponto de corte de 37.5° C (99.5° F) está fortemente associado a risco de mortalidade em 30 dias.
Por esse motivo, baseamos nossa recomendação nas orientações do NICE.
Na alta ou no acompanhamento, ofereça aos pacientes acesso a informações sobre PAC, como um folheto informativo.[1][65]
Agende uma visita de acompanhamento em cerca de 6 semanas com o clínico geral do paciente, ou em uma clínica hospitalar.[1][65]
Acompanhamento após a alta
Solicite uma radiografia torácica repetida durante a recuperação após cerca de 6 semanas para os pacientes (independentemente de terem sido hospitalizados):[1][65]
Comsintomas persistentes ou sinais físicos
Que correrem maior risco de malignidade subjacente (especialmente fumantes e pessoas com idade >50 anos).
Considere uma broncoscopia durante a recuperação nos pacientes com sinais, sintomas e anormalidades radiológicas persistentes por volta de 6 semanas após o término do tratamento.[1][65]
Use a ferramenta de risco de mortalidade CRB-65 e seu discernimento clínico para determinar quais pacientes são adequados para tratamento na comunidade (consulte nossa seção acima sobre Estratificação de risco).
Considere o tratamento domiciliar para os pacientes com um escore CRB-65 de 0 (baixa gravidade) ou um escore CRB-65 de 1 ou 2 (gravidade média) se eles desejarem ser tratados em casa e atenderem a todos os seguintes critérios:[1][63][65]
Eles são capazes de tomar medicamentos orais de forma segura e confiável
Suas circunstâncias sociais os tornam adequados para tratamento em casa
Eles não têm comorbidades instáveis.
No entanto, adote uma abordagem cautelosa ao decidir se é seguro tratar qualquer paciente com PAC de gravidade moderada (escore CRB-65 de 1 ou 2) na comunidade. Esses pacientes têm maior risco de morte, particularmente aqueles com um escore CRB-65 de 2.Você deve encaminhar a maioria para tratamento hospitalar.[1][63][65]
Se você decidir tratar o paciente na comunidade, siga as mesmas recomendações de tratamento fornecidas abaixo para pacientes com suspeita de PAC presentes na comunidade (baixa gravidade).
Encaminhe qualquer paciente que se apresente na comunidade com um escore CRB-65 de 3 ou mais para internação hospitalar imediata (geralmente em uma ambulância de luz azul no Reino Unido).[1][63][65]
Practical tip
Se você precisar encaminhar um paciente para atendimento médico de emergência no hospital, é importante informar à equipe clínica do hospital que o paciente está a caminho. Isso permitirá que o hospital inicie o tratamento adequado assim que o paciente chegar.
A - antibióticos
As recomendações a seguir são baseadas nas diretrizes da British Thoracic Society (BTS) e do National Institute for Health and Care Excellence (NICE).[1][65][117]
Administrar antibióticos antes da transferência hospitalar
CAP de alta gravidade (escore CRB-65 de 3 ou 4 )
Administre antibióticos empíricos antes da transferência hospitalar (geralmente em ambulância de luz azul no Reino Unido) aos pacientes com suspeita de PAC com risco à vida.[1][65] Siga seu protocolo local.
A escolha de primeira linha é benzilpenicilina intravenosa ou amoxicilina oral. A claritromicina é uma alternativa para as pessoas alérgicas à penicilina.[1]
Diretrizes mais recentes (2019) do NICE sobre prescrição de antimicrobianos em adultos recomendam amoxicilina/ácido clavulânico associada a claritromicina (ou eritromicina) como primeira linha nas pessoas com PAC de alta gravidade. Essas recomendações são baseadas principalmente na opinião de especialistas, pois as evidências são limitadas.[117]
Considere administrar antibióticos antes da transferência hospitalar nos pacientes com suspeita de PAC de alta gravidade, onde for provável que haja atrasos de mais de 6 horas na admissão hospitalar e no tratamento.[1][65]
Os antibióticos pré-internação podem influenciar negativamente os resultados das investigações microbiológicas subsequentes, mas isso não é visto como uma razão para não tomar antibióticos se um clínico geral considerar que é indicado.[1]
PAC de gravidade moderada (escore CRB-65 de 1 ou 2) e PAC de baixa gravidade (escore CRB-65 de 0)
Não administre antibióticos aos pacientes com PAC de gravidade moderada ou PAC de baixa gravidade antes do encaminhamento hospitalar.[1][65]
Antibióticos empíricos para tratamento domiciliar
Administre antibióticos orais empíricos aos pacientes tratados na comunidade.
As opções alternativas para os pacientes alérgicos à penicilina são um macrolídeo (por exemplo, claritromicina) ou uma tetraciclina (por exemplo, doxiciclina).[1][65]
O NICE recomenda claritromicina (ou eritromicina) ou doxiciclina como alternativas à amoxicilina para pacientes alérgicos à penicilina e para pacientes nos quais a amoxicilina é inadequada (por exemplo, se houver suspeita de pneumonia atípica). As recomendações do NICE são baseadas principalmente na opinião de especialistas, pois as evidências são limitadas.[117]
Considere adicionar ou mudar para um macrolídeo se o paciente não responder à amoxicilina.[1][65]
Considere se um diagnóstico correto de PAC foi feito se o paciente não responder aos antibióticos empíricos iniciais.[1]
Considere a revisão clínica e radiográfica para procurar diagnósticos secundários ou complicações da PAC, como derrame pleural/empiema, abscesso pulmonar ou agravamento do sombreamento pneumônico.[1]
Considere mudar os antibióticos empíricos iniciais, mas primeiro considere a adesão e a absorção adequada de um esquema oral.[1]
Administre antibioticoterapia por 5 dias.[117][125] O NICE recomenda:[117]
Prescrever o ciclo mais curto que provavelmente seja eficaz para reduzir o risco de resistência antimicrobiana e minimizar o risco de efeitos adversos
Interromper o tratamento após 5 dias, a menos que os resultados microbiológicos sugiram um ciclo mais longo ou que o paciente não esteja clinicamente estável. Isso deve ser baseado em seu julgamento clínico e nos seguintes critérios:[117][126]
Febre nas últimas 48 horas ou mais de um sinal de instabilidade clínica:
Pressão arterial sistólica <90 mmHg
Frequência cardíaca >100/minuto
Frequência respiratória >24/minuto
Saturação de oxigênio no sangue arterial <90% ou PaO 2 <60 mmHg no ar ambiente.
Manejo geral
Aconselhe os pacientes a descansar, beber bastante líquido e não fumar.[1]
Falha na resposta
Aconselhe os pacientes (e seus cuidadores) a procurarem orientação médica se:[117]
Os sintomas se agravarem rápida ou significativamente
Os sintomas não começarem a melhorar em 3 dias
A pessoa ficar sistemicamente muito mal.
Cerca de 10% dos pacientes tratados na comunidade não respondem à antibioticoterapia e precisam de hospitalização.[142]
Interne urgentemente no hospital qualquer paciente em tratamento com antibióticos com características de infecção de gravidade moderada ou alta.[1][65]
Solicite uma radiografia torácica durante a recuperação após cerca de 6 semanas para os pacientes (independentemente de terem sido internados em um hospital):[1][65]
Comsintomas persistentes ou sinais físicos
Que correm maior risco de malignidade subjacente (especialmente pessoas que fumam e pessoas com idade >50 anos).
Considere a broncoscopia durante a recuperação nos pacientes com sinais, sintomas e anormalidades radiológicas persistentes por volta de 6 semanas após o término do tratamento.[1][65]
Nos pacientes hospitalizados, a taxa de mortalidade varia de 5% a 15%, mas aumenta para 20% a 50% nos pacientes que necessitam de internação em uma unidade de terapia intensiva (UTI).[6][118]
Os fatores de risco associados ao aumento da mortalidade a 30 dias incluem bacteremia, internação na UTI, comorbidades (especialmente doenças neurológicas) e infecção por um patógeno potencialmente multirresistente (por exemplo, Staphylococcus aureus, Pseudomonas aeruginosa, Enterobacteriaceae).[34][143][144][145]
Os pacientes tratados na comunidade geralmente têm um bom prognóstico.[1][65]
Use of this content is subject to our disclaimer
