Esta página compila nosso conteúdo relacionado a Visão geral dos distúrbios do equilíbrio hidroeletrolítico e do equilíbrio ácido-básico. Para obter mais informações sobre o diagnóstico e o tratamento, siga os links abaixo para nossos tópicos completos do BMJ Best Practice sobre as doenças e sintomas relevantes.
Introdução
Condições de saúde relevantes
Avaliação da acidose respiratória | ir para nosso tópico completo sobre Avaliação da acidose respiratória A acidose respiratória ocorre quando os níveis de pressão parcial de dióxido de carbono arterial (PCO₂) aumentam para acima da faixa normal de 4.7 a 6.0 kPa (35-45 mmHg), devido à eliminação ineficiente do CO₂. Isso leva ao acúmulo de íons hidrogênio, fazendo com que o potencial hidrogeniônico (pH) arterial fique abaixo de 7.35. Ela pode ser aguda ou crônica, e a falha em se reconhecer e tratar a causa subjacente pode causar insuficiência respiratória e morte. As causas de acidose respiratória incluem DPOC, pneumonia multilobar, aspiração de corpo estranho, uso de substâncias (como sedativos, anestésicos, bebidas alcoólicas, narcóticos), e oxigenoterapia em pacientes com DPOC. A acidose respiratória crônica é comumente causada por obesidade e pela DPOC. As características clínicas da acidose respiratória incluem depressão respiratória (hipoventilação), obnubilação, instabilidade hemodinâmica e fadiga dos músculos respiratórios (uso de músculos acessórios, dispneia, taquipneia). |
|---|---|
Avaliação de alcalose respiratória | ir para nosso tópico completo sobre Avaliação de alcalose respiratória A alcalose respiratória é um distúrbio ácido-básico caracterizado por uma redução primária na PCO₂ arterial para abaixo da faixa normal de 4.7 a 6.0 kPa (35-45 mmHg), causando aumento do potencial hidrogeniônico (pH) acima de 7.45 e subsequente redução do bicarbonato a partir do valor normal de 24 mmol/L (24 mEq/L). A diminuição da PCO₂ geralmente ocorre como consequência de uma hiperventilação alveolar, com excesso de excreção do CO₂ em comparação com a produção.[3] As etiologias da alcalose respiratória são múltiplas, e incluem embolia pulmonar, sepse e síndrome da resposta inflamatória sistêmica, síndrome do desconforto respiratório agudo, pneumonia e síndrome de hiperventilação.[3] A alcalose respiratória pode ser de natureza aguda ou crônica. |
Avaliação da acidose metabólica | ir para nosso tópico completo sobre Avaliação da acidose metabólica A acidose metabólica é indicada por um potencial hidrogeniônico (pH) arterial de menos de 7.35, uma diminuição no nível de bicarbonato plasmático, e/ou um aumento acentuado do anion gap (calculado subtraindo-se a soma dos principais ânions medidos, o cloreto e o bicarbonato, do principal cátion medido, o sódio). Quando o anion gap está normal (6-12 mmol/L [6-12 mEq/L]), são comuns as causas gastrointestinais ou renais.[4] Isso também é chamado de acidose metabólica hiperclorêmica, ou sem anion gap. Se o anion gap estiver aumentado, as causas incluem cetoacidose diabética, cetoacidose alcoólica, acidose láctica, doença renal ou ingestão de metanol, etanol, etilenoglicol, propilenoglicol, 5-oxoprolina (por exemplo, em pacientes com ingestão crônica de paracetamol) ou ácido salicílico. Na acidose metabólica simples, a compensação respiratória normal diminuirá a PCO₂ arterial em 1 a 1.5 vez a diminuição do bicarbonato sérico.[5] A acidose metabólica aguda está associada a maiores morbidade e mortalidade devido aos seus efeitos depressivos sobre a função cardiovascular, o risco aumentado de arritmias cardíacas, a estimulação da inflamação e a supressão da resposta imunológica.[6] |
Avaliação da alcalose metabólica | ir para nosso tópico completo sobre Avaliação da alcalose metabólica A alcalose metabólica é um potencial hidrogeniônico (pH) arterial elevado acima de 7.45, e é consequência de distúrbios que causam a perda de íons hidrogênio do corpo ou de aumento do bicarbonato plasmático a partir de um valor normal de 24 mmol/L (24 mEq/L). As causas incluem perda de secreção gástrica (por exemplo, vômitos) e excesso de mineralocorticoides. Os pacientes podem apresentar parestesia, cãibras musculares, fraqueza, arritmias e/ou convulsões.[7][8] Alguns sintomas podem ser devidos ao aumento do cálcio na circulação, que ocorre quando o pH estiver alto. Os pacientes podem desenvolver arritmias graves ou fatais e/ou convulsões sem sintomas precedentes. A alcalose metabólica compensatória pode ser um achado acidental em pacientes com acidose respiratória crônica. |
Avaliação da hiponatremia | ir para nosso tópico completo sobre Avaliação da hiponatremia Definida por níveis de sódio sérico <135 mmol/L (<135 mEq/L); a hiponatremia grave é definida por níveis de sódio sérico <120 mmol/L (<120 mEq/L). A hiponatremia é um distúrbio eletrolítico comum e estima-se que ocorre em 15% de todos os pacientes hospitalizados.[9][10] Os pacientes com hiponatremia têm maiores morbidade e mortalidade.[11] Com algumas poucas exceções, quando o nível de sódio sérico estiver baixo, a osmolalidade do plasma também fica baixa (hiponatremia hipotônica). Mesmo sendo definida pelo nível de sódio, a hiponatremia hipotônica é, na verdade, um distúrbio do equilíbrio de água. A hiponatremia é muitas vezes iatrogênica e evitável. Causas comuns são a administração de fluidos hipotônicos em pacientes e o uso de diuréticos tiazídicos (maior probabilidade de afetar idosos).[12] A hiponatremia também pode ser uma pista para a presença de distúrbios clínicos graves subjacentes. Os pacientes que desenvolvem a hiponatremia como resultado de traumatismo cranioencefálico, cirurgia intracraniana, hemorragia subaracnoide, acidente vascular cerebral (AVC) ou tumores cerebrais podem ter a síndrome cerebral perdedora de sal, ou síndrome de secreção inapropriada de hormônio antidiurético (SIHAD). Uma redução na produção de aldosterona (por exemplo, doença de Addison) causa aumento da perda de sódio pelos rins e hiponatremia. |
Avaliação da hipernatremia | ir para nosso tópico completo sobre Avaliação da hipernatremia A hipernatremia é definida como uma concentração plasmática de sódio >145 mmol/L (>145 mEq/L). A hipernatremia é um estado de hiperosmolalidade, sendo, principalmente, um resultado de deficit de água ou de ganho de sódio. Normalmente, níveis de sódio persistentemente altos desencadeiam a liberação de hormônio antidiurético, estimulando mecanismos de sede, de modo que raramente ocorre o desenvolvimento de hipernatremia. Os pacientes hospitalizados muitas vezes têm mecanismos de sede deficientes, restrição do acesso a água e aumento do risco de perda de água (por exemplo, devido a vômitos ou febre). Eles também têm um risco de reposição de fluidos inadequada iatrogênica. Anormalidades endócrinas, como o diabetes insípido e o excesso de mineralocorticoides, também podem causar hipernatremia. O exame físico deve se concentrar na volemia. |
Avaliação da hipocalemia | ir para nosso tópico completo sobre Avaliação da hipocalemia A hipocalemia é um nível de potássio sérico <3.5 mmol/L (<3.5 mEq/L). As manifestações clínicas são normalmente observadas apenas se o nível de potássio sérico for <3.0 mmol/L (<3.0 mEq/L) e incluem fraqueza muscular, alterações no ECG, arritmias cardíacas, rabdomiólise e anormalidades renais. A hipocalemia pode ser resultado de redução na ingestão de potássio, aumento da entrada de potássio nas células, aumento da excreção de potássio (por exemplo, pelo trato gastrointestinal ou através da urina ou do suor), diálise ou plasmaférese. Existem várias causas de hipocalemia, incluindo vômitos, diarreia grave, uso de laxante e agente de limpeza intestinal na bulimia nervosa, alcoolismo crônico, anorexia nervosa,[13] acidose tubular renal,[14] aldosteronismo primário, nefropatias perdedoras de sal,[15] e fibrose cística.[16] Alguns medicamentos podem causar hipocalemia, incluindo diuréticos, tratamento com insulina para cetoacidose diabética, hiperglicinemia não cetótica, agonistas beta-adrenérgicos, como salbutamol ou terbutalina, teofilina, cloroquina, abuso de laxantes ou uso de agentes de limpeza intestinal e administração de vitamina B12 ou ácido fólico na anemia megaloblástica.[14] |
Avaliação da hipercalemia | ir para nosso tópico completo sobre Avaliação da hipercalemia A hipercalemia significativa é definida como um valor de potássio sérico >6.0 mmol/L (>6.0 mEq/L). A hipercalemia moderada é definida como valores de potássio sérico na faixa de 5.0 a 6.0 mmol/L (5.0 a 6.0 mEq/L). A hipercalemia pode apresentar risco de vida e causar arritmias cardíacas (fibrilação ventricular), afetando o potencial de ação cardíacp. Muitas vezes, a hipercalemia é multifatorial quanto à etiologia. Pode resultar da depleção efetiva do volume circulante por uma insuficiência cardíaca combinada com inibidores da enzima conversora da angiotensina (ECA), ou do aumento da ingestão de potássio alimentar com insuficiência renal crônica. É essencial obter uma história profunda das comorbidades e medicamentos que podem aumentar a liberação de potássio celular ou reduzir a excreção urinária. A redução da excreção de potássio ocorre na insuficiência renal, na depleção de volume e no hipoaldosteronismo.[17] Os fatores alimentares (por exemplo, excesso de consumo de alimentos ricos em potássio) ou medicamentos podem causar rapidamente hipercalemia em pacientes com comorbidades. |
Avaliação da hipocalcemia | ir para nosso tópico completo sobre Avaliação da hipocalcemia A hipocalcemia é um estado de desequilíbrio eletrolítico em que o nível de cálcio sérico circulante é baixo. A hipocalcemia surge principalmente da entrada insuficiente de cálcio na circulação ou de um aumento da perda de cálcio da circulação. Existem múltiplas causas, incluindo hipoparatireoidismo iatrogênico pós-cirúrgico (geralmente transitório), deficiência de vitamina D, hipomagnesemia, hiperventilação, hipoparatireoidismo, pseudo-hipoparatireoidismo, hiperfosfatemia, síndrome do osso faminto (influxo rápido de cálcio para os ossos, causando hipocalcemia mais prolongada após uma paratireoidectomia), pancreatite aguda, e pode ser induzida por medicamentos. Também é observada em pacientes críticos. A hipocalcemia varia de uma leve anormalidade bioquímica assintomática até um distúrbio que pode colocar a vida do paciente em risco. A hipocalcemia aguda pode causar parestesia, tetania e convulsões. Podem ser observados sinais físicos, incluindo o sinal de Chvostek (espasmos dos músculos inervados pelo nervo facial). |
Avaliação de hipercalcemia | ir para nosso tópico completo sobre Avaliação de hipercalcemia Normalmente não são encontrados sintomas da elevação do cálcio, a menos que o nível esteja acima de 3 mmol/L (12 mg/dL). Há maior probabilidade de sintomas de hipercalcemia grave quando o cálcio está >3.2 mmol/L (>13 mg/dL). A hipercalcemia é prejudicial à função das membranas excitáveis, acarretando fadiga dos músculos esqueléticos e da musculatura lisa do trato gastrointestinal. Os efeitos sobre o músculo cardíaco incluem o encurtamento do intervalo QT e o aumento do risco de parada cardíaca a níveis muito elevados de cálcio. As sequelas neurológicas incluem depressão, irritabilidade e, com níveis suficientemente elevados, coma. Níveis altos de cálcio podem ocasionar a precipitação em tecidos moles, como os rins, cuja função pode ser gravemente prejudicada. As causas mais comuns de hipercalcemia são o hiperparatireoidismo primário e neoplasias malignas (por exemplo, mieloma múltiplo, leucemia, câncer de pulmão e câncer de mama). Os sintomas crônicos são mais consistentes com hiperparatireoidismo, enquanto o início recente de sintomas sugere neoplasia maligna (o tumor geralmente está bem avançado). Os sinais e sintomas incluem nefrolitíases (típico do hiperparatireoidismo), letargia, fadiga constante, depressão, irritabilidade, constipação, sintomas gastrointestinais (por exemplo, náuseas, vômitos, dor abdominal, úlcera péptica, pancreatite), poliúria, polidipsia, confusão e coma. A hipercalcemia pode ser assintomática.[18] |
Avaliação da deficiência de magnésio | ir para nosso tópico completo sobre Avaliação da deficiência de magnésio A hipomagnesemia é definida por um nível de magnésio sérico <0.9 mmol/L (<1.8 mEq/L). O nível de magnésio sérico é um mau indicador do conteúdo total de magnésio e de sua disponibilidade no corpo, porque apenas 1% do magnésio é encontrado no líquido extracelular. Não há um teste laboratorial preciso, rápido e simples para estabelecer a concentração total de magnésio no corpo em humanos. A deficiência de magnésio pode ser causada por uma diminuição da ingestão de magnésio na dieta, pela diminuição da absorção de magnésio, ou pelo aumento da excreção renal de magnésio (perda renal de magnésio). As causas incluem desnutrição, deficiência isolada de magnésio alimentar, induzida por medicamentos, abuso de álcool e pancreatite. Os sintomas são inespecíficos e incluem: irritabilidade neuromuscular semelhantes à produzida pela hipocalcemia, manifestando-se com reflexos plantares extensores, sinais de Chvostek e de Trousseau positivos, e, em casos graves, tetania; características cardiovasculares, como batimentos cardíacos rápidos e pressão arterial elevada, taquicardia e/ou arritmias ventriculares; sintomas relacionados ao sistema nervoso central, como vertigem, ataxia, depressão e atividade convulsiva. |
Hiperparatireoidismo primário | ir para nosso tópico completo sobre Hiperparatireoidismo primário Endocrinopatia na qual a superprodução autônoma de paratormônio (PTH) resulta em desequilíbrio no metabolismo do cálcio. Adenomas paratireóideos únicos são a etiologia mais comum (aproximadamente 80% dos casos), e as formas familiares também são bem definidas.[19] Adenomas múltiplos e hipertrofia das 4 glândulas são menos comuns. O diagnóstico ocorre através de exames para verificar um nível de cálcio sérico elevado concomitante a um nível de PTH intacto sérico elevado de modo inadequado. Formas hereditárias, que afetam 10% a 20% dos pacientes,[20] causam hiperfuncionamento das glândulas paratireoides. É importante ressaltar que <1% dos casos de hiperparatireoidismo são causados por carcinoma das paratireoides. Em 2017, foi reconhecido o hiperparatireoidismo primário normocalcêmico. Nele, os níveis de PTH são altos, mas os níveis de cálcio sérico e ionizado são normais. Alguns pacientes, mas não todos, desenvolverão hiperparatireoidismo primário.[21] As complicações devidas à PTH primária são incomuns e incluem osteoporose e fratura óssea devido à lixiviação de cálcio dos ossos, e cálculos renais devido ao cálcio urinário e sérico elevados. |
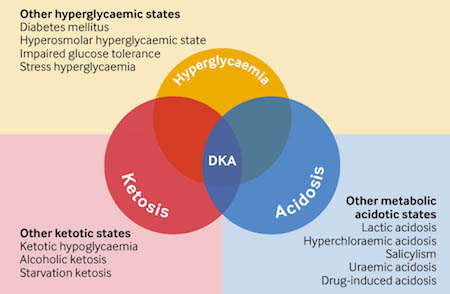
Cetoacidose diabética | ir para nosso tópico completo sobre Cetoacidose diabética Uma complicação metabólica aguda do diabetes mellitus que é potencialmente fatal e requer atendimento médico imediato para que o tratamento tenha sucesso. A cetoacidose diabética (CAD) é caracterizada por uma tríade bioquímica de hiperglicemia, cetonemia e acidose metabólica, com início rápido dos sintomas. A CAD pode ser a primeira apresentação do diabetes. Na cetoacidose diabética (CAD), há uma redução na concentração final efetiva de insulina circulante juntamente com uma elevação dos hormônios contrarreguladores (glucagon, catecolaminas, cortisol e hormônio do crescimento). A CAD geralmente é caracterizada por glicose plasmática >13.9 mmol/L (>250 mg/dL), pH arterial que varia de 7.0 a <7.3, e a presença de cetonemia e/ou cetonúria. O sódio, o cloreto, o magnésio e o cálcio séricos geralmente estão baixos; o anion gap sérico está elevado; e o potássio, ureia e creatinina séricos geralmente estão elevados. O bicarbonato arterial varia de <5 mmol/L (<10 mEq/L), na CAD grave, até <15 mmol/L (<15 mEq/L), na CAD leve. O pH venoso é recomendado para se monitorar o tratamento. Raramente, os pacientes apresentam CAD euglicêmica e têm um nível glicêmico normal. [Figure caption and citation for the preceding image starts]: Tríade de cetoacidose diabética (CAD)Adaptado com permissão de Kitabchi AE, Wall BM. Diabetic ketoacidosis. Med Clin North Am. 1995;79:9-37. [Citation ends]. |
Estado hiperosmolar hiperglicêmico | ir para nosso tópico completo sobre Estado hiperosmolar hiperglicêmico Complicação metabólica grave do diabetes mellitus caracterizada por hiperglicemia profunda (glicose >33 mmol/L [>600 mg/dL]), hiperosmolalidade (osmolalidade sérica efetiva >320 mmol/kg [>320 mOsm/kg]), e depleção de volume na ausência de cetoacidose significativa (pH >7.3 e bicarbonato >15 mmol/L [>15 mEq/L]).[22] É mais comum em pacientes idosos com diabetes mellitus do tipo 2. Ele contribui com menos de 1% de todas as internações relacionadas ao diabetes. No entanto, a mortalidade é alta, em aproximadamente 15%.[23] Infecções são o principal fator desencadeante, ocorrendo em 30% a 60% dos pacientes. Infecções do trato urinário e pneumonia são as infecções mais comuns reportadas.[22][24] O comprometimento cognitivo agudo (letargia, desorientação, estupor) é comum e se correlaciona melhor com a osmolalidade sérica efetiva. O coma é raro e, se observado, é geralmente associado a uma osmolalidade sérica >340 mOsm/kg (>340 mmol/kg).[23] |
Acidose tubular renal | ir para nosso tópico completo sobre Acidose tubular renal O termo acidose tubular renal (ATR) refere-se a um grupo de doenças renais em que ocorrem distúrbios na reabsorção de bicarbonato ou na excreção de íons hidrogênio, ou ambos. A retenção do ácido ou a perda do bicarbonato resulta no desenvolvimento de uma acidose metabólica hiperclorêmica. Portanto, as síndromes do tipo ATR são caracterizadas por uma taxa de filtração glomerular relativamente normal e acidose metabólica acompanhada por hipercloremia e um anion gap normal.[25] Pacientes adultos com ATR são frequentemente assintomáticos, mas podem apresentar fraqueza muscular relacionada a hipocalemia, nefrocalcinose ou nefrolitíase recorrente associadas. A ATR distal clássica e a ATR proximal são caracterizadas por hipocalemia.[25][26] A hipercalemia na ATR distal indica que a deficiência ou a resistência à aldosterona é a causa do problema.[25] O íon amônio está ausente ou presente em quantidades mínimas na ATR distal hipercalêmica. O sódio sérico geralmente é normal. A ATR raramente é sintomática. Os pacientes com acidemia grave podem apresentar hiperventilação ou respiração de Kussmaul decorrente de compensação respiratória. O pH urinário excede 5.5 na ATR distal clássica, mas é inferior a 5.0 em pacientes com ATR proximal não tratada. |
Aldosteronismo primário | ir para nosso tópico completo sobre Aldosteronismo primário A função primária da aldosterona é regular a absorção do sódio e a excreção do potássio no túbulo distal. No aldosteronismo primário, a produção de aldosterona excede as necessidades corporais e é relativamente autônoma em relação ao seu regulador crônico normal, o sistema renina-angiotensina II (AII).[27][28] Isso resulta em reabsorção excessiva de sódio pelo néfron distal, levando a um aumento no volume de água captado pelo néfron, contribuindo para o desenvolvimento de hipertensão e supressão da renina-AII. A perda urinária de íons potássio e hidrogênio, trocados por sódio no néfron distal, pode resultar em hipocalemia e alcalose metabólica caso seja grave e prolongada; no entanto, a maioria dos pacientes é normocalêmica.[27][28] O aldosteronismo primário é a forma de hipertensão especificamente tratada e possivelmente curável mais comum, sendo responsável por pelo menos 5% dos pacientes hipertensos.' Aproximadamente 30% das pessoas com AP têm formas unilaterais, e 70% têm formas bilaterais.[29] |
Insuficiência adrenal primária (doença de Addison) | ir para nosso tópico completo sobre Insuficiência adrenal primária (doença de Addison) Um distúrbio que resulta de doenças intrínsecas que afetam o córtex das glândulas adrenais, causando o comprometimento da síntese e secreção de todos os esteroides (glicocorticoides e/ou mineralocorticoides) normalmente secretados pelas três camadas corticais.[30] Aproximadamente 90% do córtex adrenal precisa ser destruído para resultar em insuficiência adrenal. A insuficiência adrenal primária (IAP) é uma doença rara com prevalência global de cerca de 100 a 140 casos por milhão de pessoas e incidência de 4:1,000,000 ao ano nos países desenvolvidos.[31] Pode ser aguda (crise adrenal) ou insidiosa. A IAP se apresenta com fadiga intensa e fraqueza generalizada associadas a hiperpigmentação mucocutânea, hipotensão e/ou hipotensão postural e fissura por sal. O achado de níveis séricos de sódio baixo e potássio alto é típico. Se não tratada, é uma condição de potencial risco à vida. O teste de estímulo com hormônio adrenocorticotrófico é realizado para se confirmar ou descartar o diagnóstico de IAP. |
Síndrome de secreção inapropriada de hormônio antidiurético | ir para nosso tópico completo sobre Síndrome de secreção inapropriada de hormônio antidiurético A síndrome do hormônio antidiurético inadequado (SIHAD) é definida como hiponatremia hipotônica e euvolêmica secundária à excreção de água livre comprometida, geralmente por secreção excessiva de hormônio antidiurético (HAD) pela hipófise ou, mais comumente, por uma fonte não hipofisária que pode incluir medicamentos ou câncer (a neoplasia maligna do pulmão é a mais comum). O HAD, também conhecido como arginina-vasopressina, facilita a absorção de água livre no túbulo coletor. Em condições patológicas, a hipófise e outras células podem sintetizar e secretar HAD, independentemente da osmolalidade sérica ou do volume circulante.[9] A SIHAD é identificada principalmente por níveis séricos de sódio anormais nos exames laboratoriais, mas os pacientes podem apresentar sinais de edema cerebral, incluindo náuseas, vômitos, cefaleia, alterações do estado mental, aumento da sonolência ou coma, e parecerem euvolêmicos. |
Colaboradores
Autores
Editorial Team
BMJ Publishing Group
Declarações
This overview has been compiled using the information in existing sub-topics.
Referências
Principais artigos
Berend K, de Vries AP, Gans RO. Physiological approach to assessment of acid-base disturbances. N Engl J Med. 2014 Oct 9;371(15):1434-45. Resumo
Seifter JL. Integration of acid-base and electrolyte disorders. N Engl J Med. 2014 Nov 6;371(19):1821-31. Resumo
Artigos de referência
Uma lista completa das fontes referenciadas neste tópico está disponível para os usuários com acesso total ao BMJ Best Practice.
O uso deste conteúdo está sujeito ao nosso aviso legal