Recomendaciones
Urgente
Piense en "¿Podría ser sepsis?" basado en el deterioro agudo en un paciente adulto en el que hay evidencia clínica o una fuerte sospecha de infección.[66][67][68] Ver Sepsis en adultos.
Utilice un enfoque sistemático, junto con su juicio clínico, para la evaluación; consulte urgentemente a un responsable de la toma de decisiones clínicas (p. ej., un médico de nivel ST4 en el Reino Unido) si sospecha sepsis.[67][68][69][70]
Consulte las guías de práctica clínica locales para conocer el enfoque recomendado en su institución para la evaluación y el manejo del paciente con sospecha de sepsis.
La neumonía es una de las principales fuentes de sepsis.[80]
Durante la pandemia de COVID-19, para pacientes con neumonía por COVID-19 presunta o confirmada, consulte Enfermedad por coronavirus 2019 (COVID-19). Considere que todos los pacientes con tos, fiebre u otros síntomas sugestivos tienen COVID-19 hasta que se demuestre lo contrario.
La neumonía debida a COVID-19 no se cubre en este tema.
Urgente: en el hospital
Estratifique a los pacientes con neumonía confirmada por radiografía de tórax de acuerdo con el riesgo de mortalidad y la gravedad de la enfermedad utilizando la puntuación CURB-65 y su juicio clínico . [ Índice de gravedad de la neumonía CURB-65 Opens in new window ] Utilice la puntuación para ayudar a informar su plan de manejo.
Puntuación de 3-5: gravedad alta.
Puntuación de 2: manejar como neumonía de gravedad moderada.
Puntuación de 0 o 1: manejar como neumonía de baja gravedad.
Administre antibióticos empíricos de inmediato a todos los pacientes con NAC confirmada por radiografía de tórax. Los pacientes deben recibir antibióticos dentro de las 4 horas posteriores a la presentación en el hospital.[1][65][117]
NAC de alta gravedad: administre antibióticos intravenosos de amplio espectro: consulte su protocolo local.
NAC de gravedad moderada y baja: administre antibióticos orales (o intravenosos si el tratamiento oral está contraindicada): consulte su protocolo local.
Administre antibióticos empíricos a pacientes con enfermedades potencialmente mortales según un diagnóstico clínico presuntivo, y después solicite una radiografía de tórax inmediata para confirmar el diagnóstico.[1][65]
Siga su protocolo local para la prueba diagnóstica y el tratamiento de todos los pacientes con sospecha de sepsis o aquellos en riesgo. Comience el tratamiento de inmediato. Determine la urgencia del tratamiento de acuerdo con la probabilidad de infección y la gravedad de la enfermedad, o de acuerdo con su protocolo local.[70][81]
Evalúe los requisitos de oxígeno. Prescriba oxígeno si la saturación de oxígeno <94% y manténgalo en el rango objetivo.[1][65] En pacientes con riesgo de hipercapnia, prescribir oxígeno si la saturación de oxígeno <88%.[71]
Monitorear la oxigenoterapia controlada. Un límite superior de SpO 2 del 96% es razonable cuando se administra oxígeno suplementario a la mayoría de los pacientes con enfermedad aguda que no están en riesgo de hipercapnia.
La evidencia indica que el uso liberal de oxígeno suplementario (SpO objetivo 2 >96%) en adultos gravemente enfermos se asocia con una mayor mortalidad que la oxigenoterapia más conservadora.[72]
Un objetivo más bajo de SpO 2 del 88% al 92% es adecuado si el paciente se encuentra en riesgo de insuficiencia respiratoria hipercápnica.[71]
Mida y registre las observaciones al menos dos veces al día y con más frecuencia (p. ej., cada hora) en pacientes ingresados en una unidad de cuidados intensivos para informar su plan de manejo.[1][65]
Revise a todos los pacientes con NAC de gravedad alta (alto riesgo de muerte) al menos cada 12 horas hasta que mejore.[1] Esto se debe llevar a cabo por un colega veterano y el equipo médico.[1][65]
Urgente: en el entorno comunitario
Estratifique a los pacientes según el riesgo de mortalidad y la gravedad de la enfermedad utilizando la puntuación CRB-65 (consulte nuestra sección Diagnóstico - recomendaciones para obtener más información) y su juicio clínico.[1][65]
Puntuación de 3 o más (alta gravedad): admitir al paciente en el hospital de inmediato.[1][63][65]
Puntuación de 1 o 2 (gravedad moderada): derive al hospital. Estos pacientes presentan un mayor riesgo de muerte, particularmente aquellos con una puntuación de 2.[1][63][65]
Puntuación de 0 (gravedad baja): tratar a la mayoría de los pacientes en casa.[1][63][65]
Considere el tratamiento en el hogar para pacientes con una puntuación CRB-65 de 0 (gravedad baja) o una puntuación CRB-65 de 1 o 2 (gravedad media) si desean tratamiento en domicilio y cumplen con todos los siguientes criterios:[1][63][65]
Pueden recibir medicamentos orales de manera segura y confiable
Sus circunstancias sociales los hacen aptos para el tratamiento en el hogar
No presentan comorbilidades inestables.
Adopte un enfoque cauteloso al decidir si es seguro tratar a cualquier paciente con NAC de gravedad moderada (puntuación CRB-65 de 1 o 2) en la comunidad.
Administre antibióticos empíricos antes del traslado al hospital (generalmente en ambulancia de urgencia en el Reino Unido) a pacientes con sospecha de NAC considerada potencialmente mortal.[1][65] Siga su protocolo local.
Considere la posibilidad de administrar antibióticos antes del traslado al hospital (generalmente en ambulancia de urgencia en el Reino Unido) a pacientes con sospecha de NAC donde es probable que se produzcan retrasos de más de 6 horas en el ingreso y el tratamiento hospitalarios.[1][65] Siga su protocolo local.
Principales recomendaciones
Evaluación de riesgos y manejo de la NAC en las primeras 4 horas: ámbito hospitalario[Figure caption and citation for the preceding image starts]: Evaluación de riesgos y manejo de la NAC en las primeras 4 horas: ámbito hospitalarioAdaptado de Lim WS, et al. Thorax. Octubre de 2009; 64 (Supl 3): iii1-55 [Citation ends].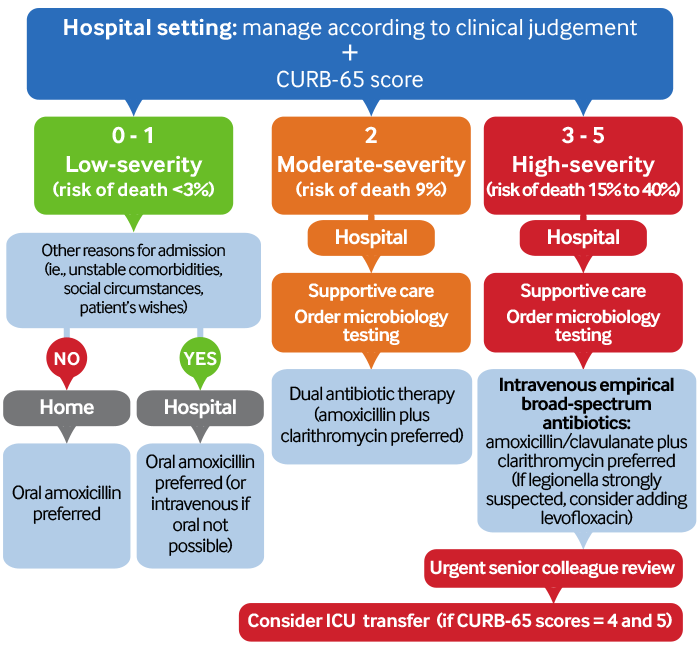
Evaluación de riesgos y gestión de la NAC en las primeras 4 horas: entorno comunitario[Figure caption and citation for the preceding image starts]: Evaluación de riesgos y manejo de la NAC en las primeras 4 horas: entorno comunitario. *Tenga en cuenta las circunstancias sociales, las comorbilidades inestables, la capacidad de tomar el tratamiento oral de manera segura y confiable, y los deseos del paciente al decidir si tratar a los pacientes en casa. **La mayoría de los pacientes con NAC de gravedad moderada deben ser derivados al hospital. Sin embargo, debe considerar las circunstancias sociales, la capacidad de tomar el tratamiento oral de manera segura, las comorbilidades inestables y los deseos del paciente al decidir sobre el tratamiento en el hogarAdaptado de Lim WS, et al. Thorax. Octubre de 2009; 64 (Supl 3): iii1-55 [Citation ends].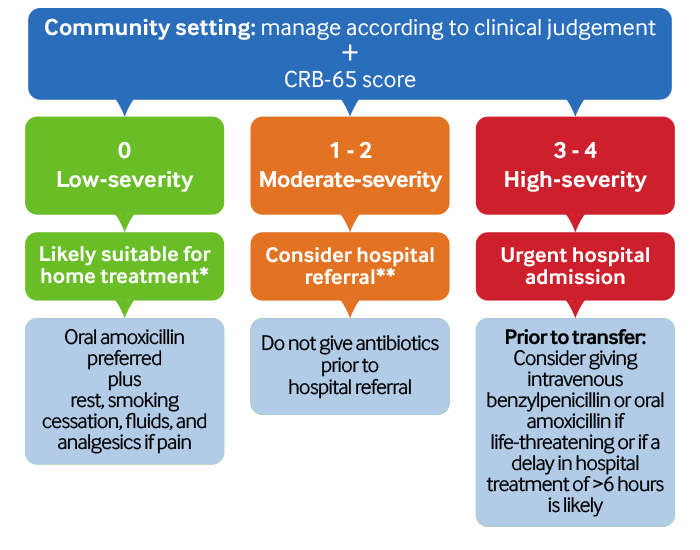
Cuidados de soporte
Administre fluidoterapia intravenosa a pacientes con depleción de volumen.[1][65]
Organice que los pacientes con puntuaciones CURB-65 de 4 y 5 y una indicación de ingreso en la unidad de cuidados intensivos (UCI) sean trasladados a la UCI y manejados por especialistas de la UCI junto con médicos respiratorios. [ Índice de gravedad de la neumonía CURB-65 Opens in new window ] [1][65]
Los pacientes con insuficiencia respiratoria a pesar de la oxigenoterapia adecuada requieren un manejo urgente de las vías respiratorias y una posible intubación.
No administre de forma rutinaria soporte de ventilación no invasiva (VNI) o presión positiva continua en las vías respiratorias (CPAP) en pacientes con insuficiencia respiratoria debido a NAC.[1][65]
Si está indicado, debe realizar un ensayo de soporte no invasivo solo en un área de cuidados intensivos donde se disponga de experiencia inmediata para permitir una transición rápida a la ventilación invasiva.[1]
Administre analgesia simple (p. ej., paracetamol) según corresponda (p. ej., para el dolor pleurítico).[1][65]
Otros tratamientos
No administre corticosteroides de forma rutinaria a pacientes con NAC de cualquier gravedad.[1][63][65]
Comente con un colega veterano pacientes con comorbilidades para las que están indicados los corticosteroides.[63]
Falta de mejora
Discuta con un colega veterano cualquier paciente que no mejore como se esperaba.[1][65]
Considere la posibilidad de repetir la radiografía de tórax, la proteína C reactiva, el recuento de leucocitos y otras muestras para microbiología en pacientes que no progresan satisfactoriamente después de 3 días de tratamiento.[1][65]
Pronóstico
Para los pacientes hospitalizados, la tasa de mortalidad oscila entre el 5% y el 15%, pero aumenta entre el 20% y el 50% en los pacientes que requieren ingreso en la UCI.[6][118] Los pacientes tratados en el entorno comunitario generalmente presentan un buen pronóstico.[1]
Determine la gravedad de la enfermedad en pacientes con un diagnóstico práctico de NAC, ya que la neumonía grave se asocia con un alto riesgo de complicaciones y muerte.[64]
Estratifique a los pacientes en aquellos con enfermedad de gravedad baja, moderada o alta (ver más abajo).[1][63][65]
La identificación temprana de la gravedad permite iniciar una antibioticoterapia adecuada, así como confirmar si el paciente puede reciba el manejo en el entorno comunitario o si necesita el ingreso en el hospital donde puede ser necesaria la ventilación asistida en un entorno de cuidados intensivos.[1][63][65]
Practical tip
Piense en "¿Podría ser sepsis?" basado en el deterioro agudo en un paciente adulto en el que hay evidencia clínica o una fuerte sospecha de infección.[66][67][68] Ver Sepsis en adultos.
El paciente puede presentar síntomas inespecíficos o no localizados (p. ej., malestar agudo con temperatura normal) o puede haber signos graves con evidencia de disfunción multiorgánica y shock.[66][67][68]
Recuerde que la sepsis representa el final grave y potencialmente mortal de la infección.[79]
La neumonía es una de las principales fuentes de sepsis.[80]
Utilice un enfoque sistemático (p. ej., Puntuación Nacional de Alerta Temprana 2 [NEWS2]), junto con su juicio clínico, para evaluar el riesgo de deterioro debido a la sepsis.[66][68][69][81] Consulte las guías de práctica clínica locales para conocer el enfoque recomendado en su institución.
Organice una revisión urgente por parte de un responsable de la toma de decisiones clínicas de alto nivel (por ejemplo, un médico de nivel ST4 en el Reino Unido) si sospecha sepsis:[70]
En un plazo de 30 minutos para un paciente que está gravemente enfermo (p. ej., puntaje NEWS2 de 7 o más, evidencia de shock séptico u otras preocupaciones clínicas significativas).
En un plazo de 1 hora para un paciente que está gravemente enfermo (p. ej., puntaje NEWS2 de 5 o 6).
Siga su protocolo local para la prueba diagnóstica y el tratamiento de todos los pacientes con sospecha de sepsis o aquellos en riesgo. Comience el tratamiento de inmediato. Determine la urgencia del tratamiento de acuerdo con la probabilidad de infección y la gravedad de la enfermedad, o de acuerdo con su protocolo local.[70][81]
En el entorno comunitario: derivar para atención médica de emergencia en el hospital (generalmente en ambulancia de luz azul en el Reino Unido) a cualquier paciente que esté gravemente enfermo con una sospecha de infección y que:[67]
Se considera que tiene un alto riesgo de deterioro debido a la disfunción orgánica (medido por la estratificación del riesgo)
Riesgo de sepsis neutropénica.
Utilice su juicio clínico junto con un sistema de puntuación:[1][63][65]
CURB-65 en el hospital [ Índice de gravedad de la neumonía CURB-65 Opens in new window ]
CRB-65 en la comunidad.
Debate: La importancia del juicio clínico
Su juicio clínico es fundamental al evaluar la gravedad de la NAC utilizando un sistema de puntuación.
Por ejemplo, considere a una persona joven con una presión arterial y un nivel de urea normales, pero una baja saturación de oxígeno a pesar de la oxigenoterapia. Esta persona podría tener neumonía grave, pero podría pasar por alto esto si solo usa un sistema de puntuación en su evaluación.[64]
Debe utilizar herramientas de pronóstico de mortalidad como CURB-65 y CRB-65 para complementar, en lugar de reemplazar, el juicio clínico al evaluar la gravedad de la NAC.
Consulte con un colega veterano sobre la decisión de comenzar a tomar antibióticos lo antes posible.[1]
En el hospital
Evalúe la gravedad utilizando la puntuación CURB-65 y su juicio clínico para identificar a los pacientes con sospecha de NAC con alto riesgo de muerte para que pueda priorizar el tratamiento inmediato y considerar si el paciente debe recibir el ingrese.[1][63][65]
Evalúe la gravedad regularmente en todos los pacientes con NAC después del ingreso hospitalario.[1][65]
Una oportunidad temprana para esto es la de un colega veterano y el equipo médico durante la ronda de la sala después del ingreso.[1]
Puntuación CURB-65: entorno hospitalario |
|---|
Puntúe 1 punto por cada característica presente:
|
|
Comente con los pacientes con una puntuación CURB-65 de 3 o más con un colega veterano lo antes posible y maneje la neumonía de alta gravedad (ver más abajo).[1][63][65]
Organice la evaluación de urgencia de pacientes con una puntuación CURB-65 de 4 o 5 por parte de un especialista en cuidados intensivos.[1][65]
Evaluación de riesgos y manejo de la NAC en las primeras 4 horas: ámbito hospitalario[Figure caption and citation for the preceding image starts]: Evaluación de riesgos y manejo de la NAC en las primeras 4 horas: ámbito hospitalarioAdaptado de Lim WS, et al. Thorax. Octubre de 2009; 64 (Supl 3): iii1-55 [Citation ends].
Siga su protocolo local cuando recete antibióticos.Las recomendaciones dadas aquí se basan en las guías de práctica clínica de la Sociedad Torácica Británica (BTS).[1][65] Consulte nuestra sección Manejo en el hospital a continuación para obtener más detalles sobre los regímenes de antibióticos.
Evidencia: efectividad de la puntuación de riesgo de mortalidad CURB-65
CURB-65 es una herramienta de pronóstico precisa para pronosticar la mortalidad en pacientes con NAC, y es recomendada por la Sociedad Torácica Británica (BTS) y el National Institute for Health and Care Excellence (NICE) junto con el juicio clínico.[1][63][65]
Se desarrolló a partir de tres estudios prospectivos en el Reino Unido, Nueva Zelanda y los Países Bajos que incluyeron a más de 1000 pacientes con NAC.[115]
Se han realizado estudios de validación en varios países (incluyendo más de 3000 pacientes en total). Han demostrado un aumento de la mortalidad con el aumento de las puntuaciones CURB-65, que van del 0% al 1.1% (puntuación CURB-65 = 0) al 17% al 60% (puntuación CURB-65 = 5),[119][120][121][122] y aumento de la necesidad de ventilación mecánica con el aumento de las puntuaciones CURB-65, que oscilan entre el 0% (puntuación CURB-65 = 0) y el 11% (puntuación CURB-65 = 5).[122]
En un estudio que comparó CURB-65 con el índice de gravedad de la neumonía (PSI), CURB-65 mostró la misma sensibilidad y una mayor especificidad (74.6% CURB-65 vs. 52.2% PSI) en la predicción de la mortalidad por NAC.[119]
Otro estudio sugiere que la PSI puede ser más precisa que CURB-65 (y CRB-65) para pronosticar la mortalidad a 30 días en pacientes con NAC.[123]
A pesar de la evidencia emergente de algunos beneficios de la PSI, tanto el NICE como la BTS consideran que la simplicidad del cálculo de la puntuación CURB-65 es una ventaja sobre la PSI.[1][63][65]
En el entorno comunitario
Evalúe la gravedad utilizando la puntuación CRB-65 junto con su juicio clínico para decidir si tratar a los pacientes con sospecha de NAC en casa o derivarlos al hospital para su evaluación o ingreso hospitalario.[1][63][65]
Puntuación CRB-65: entorno comunitario |
|---|
Puntúe 1 punto por cada característica presente:
|
*Use la prueba mental abreviada para evaluar la confusión. Abbreviated Mental Test Score Opens in new window
|
Evaluación y manejo de riesgos de la NAC: entorno comunitario[Figure caption and citation for the preceding image starts]: Evaluación de riesgos y manejo de la NAC en las primeras 4 horas: entorno comunitario. *Tenga en cuenta las circunstancias sociales, las comorbilidades inestables, la capacidad de tomar el tratamiento oral de manera segura y confiable, y los deseos del paciente al decidir si tratar a los pacientes en casa. **La mayoría de los pacientes con NAC de gravedad moderada deben ser derivados al hospital. Sin embargo, debe considerar las circunstancias sociales, la capacidad de tomar el tratamiento oral de manera segura, las comorbilidades inestables y los deseos del paciente al decidir sobre el tratamiento en el hogarAdaptado de Lim WS, et al. Thorax. Octubre de 2009; 64 (Supl 3): iii1-55 [Citation ends].
Siga su protocolo local cuando recete antibióticos.Las recomendaciones dadas aquí se basan en las guías de práctica clínica del NICE y la BTS.[1][65][117] Consulte nuestra sección Manejo en el entorno comunitario a continuación para obtener más detalles sobre los regímenes de antibióticos.
Antibióticos
Administre antibióticos empíricos a todos los pacientes con NAC confirmada por radiografía de tórax inmediatamente después del diagnóstico y dentro de las 4 horas posteriores a la presentación en el hospital.[1][65][117]
Trate de administrar antibióticos a todos los pacientes con NAC confirmada antes de que abandonen el área de evaluación inicial.[1][65]
Administre antibióticos empíricos a pacientes con enfermedades potencialmente mortales en función de un diagnóstico clínico presuntivo de NAC, y después solicite una radiografía de tórax inmediata para confirmar el diagnóstico.[1][65]
Para estos pacientes, siga su protocolo local para la prueba diagnóstica y el tratamiento de todos los pacientes con sospecha de sepsis o aquellos en riesgo. Comience el tratamiento de inmediato. Determine la urgencia del tratamiento de acuerdo con la probabilidad de infección y la gravedad de la enfermedad, o de acuerdo con su protocolo local.[70][81] Ver Sepsis en adultos.
La neumonía es una de las principales fuentes de sepsis.[80]
Es importante hacer un diagnóstico temprano y preciso de la infección y usar antibióticos de manera adecuada.
Consulte con un colega veterano sobre su decisión de comenzar a tomar antibióticos lo antes posible.[1][65]
Documente claramente la indicación de prescribir antibióticos en las notas médicas.[1]
Reduzca el tratamiento tan pronto como sea adecuado, incluido el cambio de antibioticoterapia intravenosa a oral.[1] Al tomar esta decisión, tenga en cuenta la respuesta al tratamiento (consulte el consejo práctico), el cambio en la gravedad de la enfermedad y las contraindicaciones para la administración oral, tales como:[1][65]
El paciente no puede tragar (p. ej., deterioro del reflejo de deglución, deterioro de la conciencia)
Malabsorción gastrointestinal por razones funcionales o anatómicas.
Revise la vía de administración inicialmente en la ronda de la planta después del ingreso y posteriormente, a diario.[1][65]
Practical tip
Indicadores para la mejora clínica
Las siguientes características clínicas deberían llevarlo a considerar cambiar de antibioticoterapia intravenosa a oral:[1][65]
Frecuencia del pulso <100 latidos/minuto
Resolución de la taquipnea
Clínicamente hidratado y tomando líquidos orales
Resolución de la fiebre durante >24 horas
Resolución de la hipotensión
Ausencia de hipoxia
Mejorar el recuento de glóbulos blancos
Infección no bacteriémica
No hay evidencia microbiológica de infección por legionela, estafilocóccicos o bacilos entéricos gramnegativos
No hay preocupaciones sobre la absorción gastrointestinal.
Considere la posibilidad de reducir el espectro de antibióticos o cambiar a antibióticos dirigidos a patógenos una vez que se identifique un patógeno causal.[1][65]
Antibióticos empíricos
Trate a la mayoría de los pacientes empíricamente ya que el patógeno causante rara vez se identifica en la evaluación inicial.[1][65]
Prescriba un régimen de antibióticos adecuado de acuerdo con su protocolo local para ayudar a reducir el desarrollo de resistencia a los antibióticos y la infección por Clostridium difficile.[1][65] Para ayudar a la administración de antibióticos, la Sociedad Torácica Británica (BTS) recomienda:[1][65]
Administrar antibióticos intravenosos empíricos de amplio espectro solo a pacientes con NAC de alta gravedad y reducir la escala a antibióticos de espectro estrecho tan pronto como sea clínicamente adecuado, según los resultados de las primeras pruebas diagnósticas microbiológicas.[1][65]
Este grupo comprende aproximadamente un tercio de todos los pacientes ingresados en el hospital con NAC confirmada.[1]
Administre antibióticos empíricos a todos los demás pacientes y cambie a antibióticos dirigidos a patógenos tan pronto como se identifiquen patógenos específicos.
Consulte con un microbiólogo sobre la antibioticoterapia adecuada.[1][65]
Consulte los protocolos locales de antibióticos para determinar la opción más adecuada en función de la prevalencia local de patógenos y los patrones de resistencia a los antibióticos.
Considere si se ha realizado un diagnóstico correcto de NAC si un pacienteno responde a los antibióticos empíricos iniciales.[1][65]
Considere la revisión clínica y radiográfica para buscar diagnósticos secundarios o complicaciones de la NAC, como derrame pleural/empiema, absceso pulmonar o empeoramiento del ensombrecimiento neumónico.[1]
Considere la posibilidad de cambiar los antibióticos empíricos iniciales, pero antes considere el cumplimiento y la absorción adecuada de un régimen oral.[1]
Las siguientes recomendaciones se basan en las guía de práctica clínica de la BTS y el National Institute for Health and Care Excellence (NICE).[1][65][117]
NAC de alta gravedad (puntuación CURB-65: 3 o más)
Maneje siempre a los pacientes con NAC de alta gravedad en el hospital.[1]
Administre antibióticos intravenosos empíricos de amplio espectro inmediatamente después del diagnóstico y dentro de las 4 horas posteriores a la presentación al hospital.[1][65][117]
Evidencia: plazo hasta el primer antibiótico dentro de las 4 horas posteriores a la presentación
El estudio del paquete de atención BTS CAP se llevó a cabo en 2013 en 16 centros hospitalarios del Reino Unido.
El paquete de atención de NAC constaba de cuatro elementos:
Una radiografía de tórax obtenida dentro de las 4 horas posteriores al ingreso hospitalario en todos los adultos con sospecha de NAC
Evaluación y prescripción de oxígeno de acuerdo con la guía de práctica clínica de oxígeno de la BTS[71]
Evaluación de la gravedad respaldada por la puntuación CURB-65
Antibióticos oportunos y dirigidos administrados de acuerdo con la gravedad de la NAC dentro de las 4 horas posteriores al ingreso.
El estudio comparó a los pacientes con NAC que recibían el paquete de atención NAC con los que recibían atención estándar. El análisis de los datos de 2118 adultos (mediana de edad 75.3 años) mostró que un número significativamente mayor de pacientes en el grupo del paquete de atención NAC recibió antibióticos dentro de las 4 horas posteriores al ingreso (odds ratio [OR] ajustado 1.52; IC del 95%: 1.08 a 2.14; p = 0.016) y que la mortalidad hospitalaria a los 30 días fue menor en este grupo (8.8% vs. 13.6%; odds ratio [OR] ajustado 0.59; IC del 95%: 0.37 a 0.95; p = 0.03).[124]
Administre una penicilina resistente a la betalactamasa de amplio espectro (p. ej., amoxicilina/clavulanato) más un macrólido(p. ej., claritromicina).[1][65]
La guía de práctica clínica de la BTS recomienda agregar una fluoroquinolona al régimen empírico existente (es decir, terapia triple) si el paciente no responde o si se sospecha fuertemente una neumonía por legionela.[1][65] Sin embargo, en la práctica existen preocupaciones sobre el riesgo de usar un macrólido y fluoroquinolona juntos, ya que ambos pueden prolongar el intervalo QT. Por lo tanto, algunos médicos reemplazan el macrólido en el régimen empírico original con una fluoroquinolona en su lugar (es decir, terapia dual). Considere los problemas de seguridad asociados con el uso de fluoroquinolonas. Consulte con un microbiólogo y un colega veterano antes de tratar a estos pacientes.
Las guías de práctica clínica más recientes (2019) del NICE sobre la prescripción de antimicrobianos en adultos también recomiendan amoxicilina/clavulanato más claritromicina (o eritromicina) como primera línea en personas con NAC de alta gravedad. Estas recomendaciones se basan principalmente en la opinión de los expertos, ya que la evidencia es limitada.[117]
Para los pacientes que son alérgicos a la penicilina, administre una cefalosporina de segunda generación (p. ej., cefuroxima) o una cefalosporina de tercera generación (p. ej., cefotaxima o ceftriaxona) más un macrólido (p. ej., claritromicina).[1][65]
Un pequeño número de pacientes son alérgicos tanto a las penicilinas como a las cefalosporinas; consulte a un especialista de enfermedades infecciosas para la selección de antibióticos adecuados en estos pacientes.
Las guías de práctica clínica del NICE sobre la prescripción de antimicrobianos en adultos recomiendan levofloxacina (después de considerar los problemas de seguridad asociados con el uso de fluoroquinolonas) como un antibiótico alternativo para pacientes con NAC de alta gravedad que son alérgicos a la penicilina.[117]
Revise la necesidad de antibióticos intravenosos inicialmente durante la ronda de planta después del ingreso y a continuación, a diario.[1][65]
Las guías de práctica clínica del NICE sobre la prescripción de antimicrobianos en adultos recomiendan revisar los antibióticos intravenosos a las 48 horas y considerar el cambio a tratamiento oral si es posible.[117] La mejor práctica es revisar los antibióticos intravenosos todos los días; la mayoría de los antibióticos intravenosos se pueden suspender y cambiar al tratamiento oral en el plazo de 24 horas.
Cambie a antibióticos orales tan pronto como se produzca una mejoría clínica (consulte el consejo práctico anterior para obtener indicaciones sobre la mejoría clínica) y siempre que no existan contraindicaciones para la administración oral, tales como:[1][65]
El paciente no puede tragar (p. ej., deterioro del reflejo de deglución, deterioro de la conciencia)
Malabsorción gastrointestinal por razones funcionales o anatómicas.
Administre antibioticoterapia durante 5 días.[117][125] El NICE recomienda:[117]
Prescribir el ciclo más corto que pueda ser eficaz para reducir el riesgo de resistencia a los antimicrobianos y minimizar el riesgo de efectos adversos[117]
Suspenda el tratamiento después de 5 días a menos que los resultados microbiológicos sugieran un curso más prolongado o que el paciente no esté clínicamente estable.Esto debe basarse en su juicio clínico y en los siguientes criterios:[117][126]
Fiebre en las últimas 48 horas, o más de un signo de inestabilidad clínica:
Presión arterial sistólica <90 mmHg
Frecuencia cardíaca >100/minuto
Frecuencia respiratoria >24/minuto
Saturación arterial de oxígeno <90% o PaO 2 <60 mmHg en aire ambiente.
En algunas personas, es posible que se necesiten cursos más largos debido a circunstancias individuales. En el Reino Unido, algunos hospitales requieren una consulta con el equipo de microbiología si consideran la opción de ampliar la duración del tratamiento con antibióticos más allá de 5 días en NAC de alta gravedad.Siga su protocolo local.
Las guías de práctica clínica del NICE no proporcionan un límite superior en la duración del ciclo de antibióticos. Esto se determinará en circunstancias individuales, en función del tiempo necesario para alcanzar la estabilidad clínica.[117]
NAC de gravedad moderada (puntuación CURB-65: 2)
Administre antibióticos lo antes posible después del diagnóstico y dentro de las 4 horas posteriores a la presentación en el hospital.[1][65][117]
Considere a los pacientes con NAC de gravedad moderada para el tratamiento hospitalario de corta estancia o el tratamiento ambulatorio supervisado por el hospital.[1][65]
Evidencia: plazo hasta el primer antibiótico dentro de las 4 horas posteriores a la presentación
El estudio del paquete de atención BTS CAP se llevó a cabo en 2013 en 16 centros hospitalarios del Reino Unido.
El paquete de atención de NAC constaba de cuatro elementos:
Una radiografía de tórax obtenida dentro de las 4 horas posteriores al ingreso hospitalario en todos los adultos con sospecha de NAC.
Evaluación y prescripción de oxígeno de acuerdo con la guía de práctica clínica de oxígeno de la BTS[71]
Evaluación de la gravedad respaldada por la puntuación CURB-65
Antibióticos oportunos y dirigidos administrados de acuerdo con la gravedad de la NAC dentro de las 4 horas posteriores al ingreso.
El estudio comparó a los pacientes con NAC que recibían el paquete de atención NAC con los que recibían atención estándar. El análisis de los datos de 2118 adultos (mediana de edad 75.3 años) mostró que un número significativamente mayor de pacientes en el grupo del paquete de atención NAC recibió antibióticos ≤4 horas después del ingreso (OR ajustado 1.52; IC del 95%: 1.08 a 2.14; p = 0.016) y que la mortalidad hospitalaria a los 30 días fue menor en este grupo (8.8% vs. 13.6%; OR ajustado 0.59; IC del 95%: 0.37 a 0.95; p = 0.03).[124]
La mayoría de los pacientes con NAC de gravedad moderada pueden tratarse con antibioticoterapia oral doble. La opción de preferencia es amoxicilina más un macrólido (p. ej., claritromicina).[1][65]
Las guías de práctica clínica del NICE sobre la prescripción de antimicrobianos en adultos recomiendan la monoterapia con amoxicilina en personas con NAC de gravedad moderada, con la adición de claritromicina (o eritromicina) solo si se sospecha un patógeno atípico. Estas recomendaciones se basan principalmente en la opinión de los expertos, ya que la evidencia es limitada.[117]
Considere el uso de la monoterapia con un macrólido para pacientes que han sido tratados en el entorno comunitario y que no han respondido a un ciclo adecuado de amoxicilina antes del ingreso hospitalario.[1][65]
Decida si el curso de amoxicilina fue adecuado es complicado e implica juicio clínico. Consulte a un médico veterano antes de prescribir monoterapia dentro de las primeras 24 horas del ingreso.[1][65]
Si los antibióticos orales están contraindicados (p. ej., el paciente no puede deglutir o tiene malabsorción gastrointestinal por razones funcionales o anatómicas), administre amoxicilina o bencilpenicilina intravenosa, más claritromicina.[1][65]
Para los pacientes que son alérgicos a la penicilina o a los macrólidos, considere el uso de la doxiciclina oral.[1][65] Las opciones alternativas incluyen levofloxacina oral o moxifloxacina (después de considerar los problemas de seguridad asociados con el uso de fluoroquinolonas).[1][65]
Las guías de práctica clínica del NICE sobre la prescripción de antimicrobianos en adultos con NAC recomiendan doxiciclina o claritromicina en personas alérgicas a la penicilina.[117]
Para los pacientes alérgicos a la penicilina en los que los antibióticos orales están contraindicados, administre una cefalosporina de segunda generación (p. ej., cefuroxima) o una cefalosporina de tercera generación (p. ej., cefotaxima o ceftriaxona) más claritromicina o levofloxacina intravenosa como monoterapia.[1][65]
Si el paciente no responde a una combinación de amoxicilina más claritromicina, considere la posibilidad de cambiar el tratamiento a doxiciclina o una fluoroquinolona con cobertura neumocócica efectiva.[1][65]
Más información: restricciones de la EMA y la MHRA sobre el uso de antibióticos fluoroquinolonas
En noviembre de 2018, la Agencia Europea de Medicamentos (EMA) completó una revisión de los efectos adversos graves, incapacitantes y potencialmente irreversibles asociados a la administración de fluoroquinolonas por vía sistémica e inhalada. Estos efectos adversos incluyen tendinitis, ruptura de tendones, artralgia, neuropatías y otros efectos musculoesqueléticos o del sistema nervioso.
Como consecuencia de esta revisión, la EMA ahora recomienda que los antibióticos de fluoroquinolonas se restrinjan para su uso solo en infecciones bacterianas graves y potencialmente mortales. Además, recomiendan que las fluoroquinolonas no se usen para infecciones leves a moderadas a menos que no se puedan usar otros antibióticos adecuados para la infección específica, y no deben usarse en infecciones no graves, no bacterianas o autolimitadas. Los pacientes de edad avanzada, que presentan insuficiencia renal o que han tenido un trasplante de órganos sólidos, y los que están recibiendo tratamiento con corticosteroides presentan un mayor riesgo de sufrir daños en los tendones. Se debe evitar la administración conjunta de una fluoroquinolona y un corticosteroide.[127] La Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA), con sede en el Reino Unido, respalda estas recomendaciones.[128]
Por esta razón, las fluoroquinolonas solo deben considerarse en NAC de gravedad moderada cuando se considera inadecuado el uso de otros antibióticos que se recomiendan comúnmente para el tratamiento de la NAC.Consulte con un microbiólogo sobre si una fluoroquinolona es una opción adecuada para su paciente.
Revise la necesidad de antibióticos intravenosos inicialmente en la ronda de planta después del ingreso y a continuación, a a diario.[1][65]
Las guías de práctica clínica del NICE sobre la prescripción de antimicrobianos en adultos recomiendan revisar los antibióticos intravenosos a las 48 horas y considerar el cambio a tratamiento oral si es posible.[117] La mejor práctica es revisar los antibióticos intravenosos todos los días; la mayoría de los antibióticos intravenosos se pueden suspender y cambiar al tratamiento oral en el plazo de 24 horas.
Cambie a antibióticos orales tan pronto como se produzca una mejoría clínica (véase consejo práctico), y siempre que no existan contraindicaciones para la administración oral como:[1][65]
El paciente no puede tragar (p. ej., deterioro del reflejo de deglución, deterioro de la conciencia)
Malabsorción gastrointestinal por razones funcionales o anatómicas.
Practical tip
Indicadores para la mejora clínica
Las siguientes características clínicas deberían llevarlo a considerar cambiar de antibioticoterapia intravenosa a oral:[1][65]
Frecuencia del pulso <100 latidos/minuto
Resolución de la taquipnea
Clínicamente hidratado y tomando líquidos orales
Resolución de la fiebre durante >24 horas
Resolución de la hipotensión
Ausencia de hipoxia
Mejorar el recuento de glóbulos blancos
Infección no bacteriémica
No hay evidencia microbiológica de infección por legionela, estafilocóccicos o bacilos entéricos gramnegativos
No hay preocupaciones sobre la absorción gastrointestinal.
Administre antibioticoterapia durante 5 días.[117][125] El NICE recomienda:[117]
Prescribir el ciclo más corto que pueda ser eficaz para reducir el riesgo de resistencia a los antimicrobianos y minimizar el riesgo de efectos adversos
Suspenda el tratamiento después de 5 días a menos que los resultados microbiológicos sugieran un curso más prolongado o que el paciente no esté clínicamente estable. Esto debe basarse en su juicio clínico y en los siguientes criterios:[117][126]
Fiebre en las últimas 48 horas, o más de un signo de inestabilidad clínica:
Presión arterial sistólica <90 mmHg
Frecuencia cardíaca >100/minuto
Frecuencia respiratoria >24/minuto
Saturación arterial de oxígeno <90% o PaO 2 <60 mmHg en aire ambiente.
Un EAC encontró que en los pacientes con NAC moderadamente grave que cumplían los criterios de estabilidad clínica, la interrupción del tratamiento con betalactámicos después de 3 días no era inferior a 8 días de tratamiento, lo que sugiere que 3 días de antibióticos pueden ser suficientes en los pacientes inmunocompetentes y no gravemente enfermos que mejoran clínicamente al tercer día.[129]
En algunas personas, es posible que se necesiten cursos más largos debido a circunstancias individuales. En el Reino Unido, algunos hospitales requieren una consulta con el equipo de microbiología si consideran la opción de ampliar la duración del tratamiento con antibióticos más allá de los 5 días en NAC de gravedad moderada.Siga su protocolo local.
Las guías de práctica clínica del NICE no proporcionan un límite superior en la duración del ciclo de antibióticos. Esto se determinará en circunstancias individuales, en función del tiempo necesario para alcanzar la estabilidad clínica.[117]
NAC de baja gravedad (puntuación CURB-65: 0-1)
Administre antibióticos lo antes posible y dentro de las 4 horas posteriores a la presentación en el hospital.[1][65][117]
Evidencia: plazo hasta el primer antibiótico dentro de las 4 horas posteriores a la presentación
El estudio del paquete de atención BTS CAP se llevó a cabo en 2013 en 16 centros hospitalarios del Reino Unido.
El paquete de atención de NAC constaba de cuatro elementos:
Una radiografía de tórax obtenida dentro de las 4 horas posteriores al ingreso hospitalario en todos los adultos con sospecha de NAC
Evaluación y prescripción de oxígeno de acuerdo con la guía de práctica clínica de oxígeno de la BTS[71]
Evaluación de la gravedad respaldada por la puntuación CURB-65
Antibióticos oportunos y dirigidos administrados de acuerdo con la gravedad de la NAC dentro de las 4 horas posteriores al ingreso.
El estudio comparó a los pacientes con NAC que recibían el paquete de atención NAC con los que recibían atención estándar. El análisis de los datos de 2118 adultos (mediana de edad 75.3 años) mostró que un número significativamente mayor de pacientes en el grupo del paquete de atención NAC recibió antibióticos ≤4 horas después del ingreso (OR ajustado 1.52; IC del 95%: 1.08 a 2.14; p = 0.016) y que la mortalidad hospitalaria a los 30 días fue menor en este grupo (8.8% vs. 13.6%; OR ajustado 0.59; IC del 95%: 0.37 a 0.95; p = 0.03).[124]
La mayoría de los pacientes con NAC de baja gravedad que reciben tratamiento en el hospital pueden recibir tratamiento con antibióticos orales.[1][65] La opción preferida es la amoxicilina.[1][65] Considere un macrólido (p. ej., claritromicina) o una tetraciclina (p. ej., doxiciclina) para pacientes que son alérgicos a la penicilina.[1][65]
El NICE recomienda la claritromicina (o eritromicina) o la doxiciclina como alternativas a la amoxicilina para los pacientes alérgicos a la penicilina y para los pacientes en los que la amoxicilina no es adecuada (p. ej., si se sospecha una neumonía atípica). Las recomendaciones de NICE se basan principalmente en la opinión de expertos, ya que la evidencia es limitada.[117]
Si la vía oral está contraindicada (p. ej., deterioro del reflejo de deglución, alteración de la conciencia, malabsorción gastrointestinal), considere la amoxicilina, la bencilpenicilina o la claritromicina intravenosas.[1][65]
Revise la necesidad de antibióticos intravenosos inicialmente durante la ronda de la sala después del ingreso y después todos los días después.[1][65] Las guías de práctica clínica del NICE sobre la prescripción de antimicrobianos en adultos recomiendan revisar los antibióticos intravenosos a las 48 horas y considerar el cambio a tratamiento oral si es posible.[117] La mejor práctica es revisar los antibióticos intravenosos todos los días; la mayoría de los antibióticos intravenosos se pueden suspender y cambiar al tratamiento oral en el plazo de 24 horas.
Cambie a antibióticos orales tan pronto como se produzca una mejoría clínica (véase consejo práctico) y siempre que no existen contraindicaciones para la administración oral.[1][117][65]
Practical tip
Indicadores para la mejora clínica
Las siguientes características clínicas deberían llevarlo a considerar cambiar de antibioticoterapia intravenosa a oral:[1][65]
Frecuencia del pulso <100 latidos/minuto
Resolución de la taquipnea
Clínicamente hidratado y tomando líquidos orales
Resolución de la fiebre durante >24 horas
Resolución de la hipotensión
Ausencia de hipoxia
Mejorar el recuento de glóbulos blancos
Infección no bacteriémica
No hay evidencia microbiológica de infección por legionela, estafilocóccicos o bacilos entéricos gramnegativos
No hay preocupaciones sobre la absorción gastrointestinal.
Si el paciente no respondea la monoterapia con amoxicilina, considere la posibilidad de cambiar o agregar un macrólido (p. ej., claritromicina).[1][65]
Administre antibioticoterapia durante 5 días.[117][125] El NICE recomienda:[117]
Prescribir el ciclo más corto que pueda ser eficaz para reducir el riesgo de resistencia a los antimicrobianos y minimizar el riesgo de efectos adversos
Suspenda el tratamiento después de 5 días a menos que los resultados microbiológicos sugieran un curso más prolongado o que el paciente no esté clínicamente estable.Esto debe basarse en su juicio clínico y en los siguientes criterios:[117][126]
Fiebre en las últimas 48 horas, o más de un signo de inestabilidad clínica:
Presión arterial sistólica <90 mmHg
Frecuencia cardíaca >100/minuto
Saturación arterial de oxígeno <90% o PaO 2 <60 mmHg en aire ambiente.
Tratamiento antibiótico dirigido a patógenos
Cambie de antibióticos empíricos a antibióticos dirigidos a patógenos tan pronto como se identifiquen patógenos específicos (a menos que existan preocupaciones legítimas sobre la infección por patógenos duales).[1][65]
Consulte con un microbiólogo sobre la antibioticoterapia adecuada.[1][65]
Solo alrededor de un tercio a un cuarto de los pacientes con NAC ingresados en el hospital tendrán su neumonía definida microbiológicamente.[1] Entre estos pacientes:
Alrededor del 14% tiene un patógeno atípico, de los cuales:[21]
El 7% tiene Mycoplasma pneumoniae
El 4% tiene Chlamydophila pneumoniae
El 3% tiene Legionella pneumophila
Aquellos con infecciones debidas a organismos como Mycoplasma, Chlamydophila y Coxiella burnetii serán diagnosticados tarde en la enfermedad sobre la base de la seroconversión, lo que reduce la oportunidad de una terapia dirigida temprana.[1] Entre los pacientes tratados en el entorno comunitario, muy pocos se definirán microbiológicamente.[1]
Considere la posibilidad de cambiar de tratamiento una vez que los resultados de las pruebas de sensibilidad estén disponibles o después de consultar con un microbiólogo, intensivista o médico respiratorio.[1]
Recomendaciones de la BTS para los antibióticos dirigidos a patógenos[1][65]
Patógeno | Antibiótico de preferencia | Antibiótico alternativo |
|---|---|---|
Mycoplasma pneumoniae Chlamydophila pneumoniae | Claritromicina (por vía oral o intravenosa) | Doxiciclina (por vía oral) o una fluoroquinolona (por vía oral o intravenosa) |
Especies de Legionella | Fluoroquinolona (por vía oral o intravenosa) | Claritromicina (por vía oral o intravenosa) o azitromicina (en países donde se usa para controlar la neumonía) |
Streptococcus pneumoniae | Amoxicilina (por vía oral) o bencilpenicilina (por vía intravenosa) | Claritromicina (por vía oral) o cefuroxima o cefotaxima o ceftriaxona (por vía intravenosa) |
Chlamydia psittaci Coxiella burnetii | Doxiciclina (por vía oral) | Claritromicina (por vía oral o intravenosa) |
Haemophilus influenzae | No productoras de betalactamasas: amoxicilina (por vía oral o intravenosa) Productoras de betalactamasas: amoxicilina/ácido clavulánico (por vía oral o intravenosa) | Cefuroxima o cefotaxima o ceftriaxona (por vía intravenosa) o una fluoroquinolona (por vía oral o intravenosa) |
Bacilos entéricos gramnegativos | Cefuroxima o cefotaxima o ceftriaxona (por vía intravenosa) | Fluoroquinolona (por vía intravenosa) o imipenem/cilastatina (por vía intravenosa) o meropenem (por vía intravenosa) |
Pseudomonas aeruginosa | Ceftazidima (por vía intravenosa) más Gentamicina o tobramicina (se requiere control de dosis) | Ciprofloxacino (por vía intravenosa) o piperacilina/tazobactam (por vía intravenosa) más Gentamicina o tobramicina (se requiere control de dosis) |
Staphylococcus aureus: no MRSA | Flucloxacilina (por vía intravenosa) con o sin Rifampicina (por vía oral o intravenosa) | |
Staphylococcus aureus: SARM | Vancomicina (por vía intravenosa; se requiere control de la dosis) o linezolid (por vía intravenosa) o teicoplanina (por vía intravenosa) con o sin Rifampicina (por vía oral o intravenosa) |
Cuidados de soporte
Brindar atención de apoyo a los pacientes tratados en el hospital.Esto puede incluir las siguientes medidas.[1][65]
Oxígeno
Evaluar la saturación de oxígeno en todos los pacientes mediante oximetría de pulso (preferiblemente mientras respiran aire).
Administre oxígeno si la saturación de oxígeno <94% y manténgala en el rango objetivo.[1][65] En pacientes con riesgo de retención de CO2 , administre oxígeno si la saturación de oxígeno <88%. La evaluación temprana del oxígeno se asocia con un mejor pronóstico.[71]
Monitorear la oxigenoterapia controlada. Un límite superior de SpO2 del 96% es razonable cuando se administra oxigenoterapia a la mayoría de los pacientes con enfermedad aguda queno están en riesgo de hipercapnia.
La evidencia indica que el uso liberal de oxigenoterapia (objetivo SpO2 >96%) en adultos gravemente enfermos se asocia con una mayor mortalidad que la oxigenoterapia más conservadora.[72]
Un objetivo más bajo de SpO2 del 88% al 92% es adecuado si el paciente está en riesgo de insuficiencia respiratoria hipercápnica.[71]
Evidencia: saturación de oxígeno objetivo en adultos gravemente enfermos
Demasiada oxigenoterapia aumenta la mortalidad.
La evidencia de una revisión sistemática grande y un metanálisis apoya la oxigenoterapia conservadora/controlada frente a la oxigenoterapia liberal en adultos gravemente enfermos que no están en riesgo de hipercapnia.
Las guías de práctica clínica difieren en sus recomendaciones sobre la saturación de oxígeno objetivo en adultos gravemente enfermos que reciben oxigenoterapia.
La guía de práctica clínica de la British Thoracic Society (BTS) del 2017 recomienda un rango objetivo de SpO2 del 94% al 98% para pacientes que no tienen riesgo de hipercapnia, mientras que la guía de la Thoracic Society of Australia and New Zealand (TSANZ) de 2022 recomienda del 92% al 96%.[71][130]
La guía de práctica clínica de la Global Initiative For Asthma (GINA) de 2022 recomienda un rango objetivo de SpO2 del 93% al 96% en el contexto de las exacerbaciones agudas del asma.[131]
Una revisión sistemática que incluyó un metanálisis de datos de 25 ensayos aleatorizados controlados publicados en 2018 encontró que en adultos con enfermedad aguda, la oxigenoterapia liberal (ampliamente equivalente a una saturación objetivo >96%) se asocia con una mayor mortalidad que la oxigenoterapia conservadora (ampliamente equivalente a una saturación objetivo ≤96%).[72] La mortalidad hospitalaria fue 11 por 1000 más alta para el grupo de oxigenoterapia liberal frente al grupo de terapia conservadora (IC del 95%: 2 a 22 por 1000 más). La mortalidad a los 30 días también fue mayor en el grupo que había recibido oxígeno liberal (CR 1,14; IC del 95%: 1,01 a 1,29). Los ensayos incluyeron adultos con sepsis, enfermedad crítica, accidente cerebrovascular, traumatismo, infarto de miocardio, paro cardíaco y pacientes sometidos a cirugía de emergencia. Se excluyeron de la revisión los estudios que se limitaron a pacientes con enfermedades respiratorias crónicas o psiquiátricas, o pacientes con soporte vital extracorpóreo, que recibían oxigenoterapia hiperbárica o que se sometían a cirugía electiva.
Por lo tanto, un límite superior de SpO2 del 96% es razonable cuando se administra oxigenoterapia a pacientes con enfermedades agudas que no están en riesgo de hipercapnia. Sin embargo, un objetivo más alto puede ser adecuado para algunas afecciones específicas (p. ej., neumotórax, intoxicación por monóxido de carbono, cefalea en racimos y crisis de células falciformes).[132]
En 2019, el BTS revisó su guía de orientación en respuesta a esta revisión sistemática y metanálisis y decidió que no se requería una actualización provisional.[113]
El comité señaló que la revisión sistemática respaldaba el uso de oxigenoterapia controlada para un objetivo.
Si bien la revisión sistemática mostró una asociación entre mayores saturaciones de oxígeno y mayor mortalidad, el comité de BTS consideró que la revisión no era definitiva sobre cuál debería ser el rango objetivo óptimo. El rango sugerido del 94% al 96% en la revisión se basó en el intervalo de confianza más bajo del 95% y la mediana de SpO2 basal de los grupos de terapia liberal de oxígeno, junto con la recomendación anterior de la guía TSANZ de 2015.
Posteriormente, la experiencia durante la pandemia de COVID-19 también ha favorecido que los médicos sean más conscientes de la viabilidad de la hipoxemia permisiva.[133]
El manejo de la oxigenoterapia en pacientes en cuidados intensivos es especializado e informado por evidencia adicional que es más específica para este contexto.[134][135][136]
Medir la gasometría arterial en aquellos con SpO2 <94%, aquellos con riesgo de insuficiencia ventilatoria hipercápnica (retención de CO2 ) y todos los pacientes con NAC de alta gravedad.[1][65]
Practical tip
Registre siempre claramente la concentración de oxígeno inspirado, ya que es esencial para interpretar los resultados de los gases en sangre.
Cuidados de apoyo estándar de la unidad de cuidados intensivos (UCI)
Organizar que los pacientes con puntajes CURB-65 de 4 y 5 y una indicación para el ingreso en la UCI sean transferidos a la UCI y manejados por especialistas de la UCI junto con médicos respiratorios.[1][65]
Los pacientes con insuficiencia respiratoria a pesar de la oxigenoterapia adecuada requieren un manejo urgente de las vías respiratorias y una posible intubación.
No administre de forma rutinaria soporte de ventilación no invasiva (VNI) o presión positiva continua en las vías respiratorias (CPAP)en pacientes con insuficiencia respiratoria debido a NAC.[1][65]
Si está indicado, debe realizar un ensayo de soporte no invasivo solo en un área de cuidados intensivos donde se disponga de experiencia inmediata para permitir una transición rápida a la ventilación invasiva.[1][65]
Vasopresores
Iniciar vasopresores si el paciente está hipotenso durante o después de la reanimación con líquidos para mantener el nivel medio de presión arterial ≥65 mmHg.[137]
Fluidoterapia intravenosa
Evalúe a todos los pacientes para detectar hipovolemia y administre fluidoterapia intravenosa si es necesario.[1][65]
profilaxis de tromboembolia venosa (TEV)
Considere la profilaxis para el TEV con heparina de bajo peso molecular para todos los pacientes que no tienen movilidad completa.[1][65]
Apoyo nutricional
Organizar el apoyo nutricional(ya sea enteral, parenteral o mediante alimentación nasogástrica) para pacientes con NAC grave que requieren una estancia hospitalaria prolongada.[1][65]
despeje de las vías respiratorias
No trate a las personas con neumonía sin complicaciones con técnicas tradicionales de depuración de las vías respiratorias de forma rutinaria. Si es necesario, ofrezca a estos pacientes consejos sobre la expectoración del esputo.[1][65]
Considere técnicas de depuración de las vías respiratorias si el paciente tiene dificultad para expectorar el esputo o si tiene una afección pulmonar preexistente.[1][65]
Analgesia
Administre analgesia simple (p. ej., paracetamol) según corresponda (p. ej., para el dolor pleurítico).[1][65]
Practical tip
Anime a los pacientes con NAC no complicada (es decir, no complicada por la presencia de derrame paraneumónico, empiema, absceso, neumotórax, neumonía necrotizante o fístula broncopleural), cuya condición médica les permita, a sentarse fuera de la cama. Inicialmente, trate de realizar al menos 20 minutos en las primeras 24 horas y luego aumente la movilidad cada día posterior de hospitalización.
Otros tratamientos
Corticosteroides
No administre corticosteroides de forma rutinaria a pacientes con NAC de cualquier gravedad.[1][63][65]
Hable con un colega sénior sobre pacientes con comorbilidades para las que están indicados los corticosteroides.[63]
Debate: Tratamiento con corticoides en la NAC
La evidencia más reciente indica que los corticosteroides administrados como complemento del tratamiento con antibióticos mejoran los resultados en adultos con NAC, pero aumentan el riesgo de hiperglucemia. La recomendación del NICE de no administrar corticosteroides de forma sistemática sigue siendo válida hasta que se disponga de más evidencia.
Una revisión de la Cochrane que incluyó 17 estudios evaluó la seguridad y la eficacia de los corticosteroides administrados como complemento del tratamiento con antibióticos para adultos y niños con neumonía (NAC, neumonía adquirida en el hospital y neumonía asociada al ventilador). La intervención incluyó prednisolona oral en 3 ensayos y dexametasona, hidrocortisona o metilprednisolona intravenosa en 13 ensayos. Los hallazgos sugieren que los corticosteroides redujeron significativamente la mortalidad y la morbilidad en pacientes con NAC de alta gravedad. También redujeron la morbilidad, aunque no la mortalidad, en pacientes con NAC de gravedad moderada o baja. La hiperglucemia fue el evento adverso más frecuente en adultos tratados con corticosteroides; sin embargo, los autores concluyeron que, en general, los beneficios superan a los daños.[138]
Dos revisiones sistemáticas (publicadas antes de la revisión de la Cochrane) también consideraron la seguridad y la eficacia de los glucocorticoides adyuvantes para los pacientes con NAC.[139][140] No mostraron diferencias significativas en la mortalidad por cualquier causa e informaron reducciones significativas en la duración de la estancia en la UCI.[139] duración de la estancia hospitalaria,[139][140] y el tiempo hasta la estabilidad clínica en los grupos de corticosteroides.[139][140] Una de las revisiones informó un mayor riesgo de hiperglucemia en pacientes tratados con corticosteroides.[140]
El NICE debe revisar esta área cuando se hayan publicado los resultados de dos ensayos en curso. Por ahora, la recomendación de no administrar corticosteroides de forma rutinaria sigue siendo válida.[63]
Monitorización
Mida las observaciones inicialmente al menos dos veces al día y con mayor frecuencia (p. ej., cada hora) en aquellos ingresados en una unidad de cuidados intensivos (unidad de alta dependencia o UCI).[1][65] Monitorizar:
Pulso
Presión arterial
Frecuencia respiratoria
Temperatura
Saturación de oxígeno (con un registro de la saturación de oxígeno inspirada al mismo tiempo)
Estado mental.
Considere medir una concentración inicial de proteína C reactiva en pacientes con NAC al ingreso en el hospital, y repita la prueba si el progreso clínico es incierto después de 48 a 72 horas.[1][63][65]
Revise a todos los pacientes con NAC de gravedad alta al menos cada 12 horas hasta que se produzca una mejoría clínica.[1][65] Esto debe ser hecho por un colega veterano y el equipo médico.[1][65]
Practical tip
Indicadores para la mejora clínica
Las siguientes características clínicas deberían llevarlo a considerar cambiar de antibioticoterapia intravenosa a oral:[1][65]
Frecuencia del pulso <100 latidos/minuto
Resolución de la taquipnea
Clínicamente hidratado y tomando líquidos orales
Resolución de la fiebre durante >24 horas
Resolución de la hipotensión
Ausencia de hipoxia
Mejorar el recuento de glóbulos blancos
Infección no bacteriémica
No hay evidencia microbiológica de infección por legionela, estafilocóccicos o bacilos entéricos gramnegativos
No hay preocupaciones sobre la absorción gastrointestinal.
Evaluar la gravedad regularmente en todos los pacientes con NAC después del ingreso hospitalario.[1][65] Una oportunidad temprana para esto es la ronda de sala después de la admisión por un colega sénior y el equipo médico.[1][65]
Para obtener más información sobre las complicaciones relacionadas con la NAC, consulte nuestra sección separada de Complicaciones .
Falta de mejora
Hable con un colega sénior sobre cualquier paciente que no mejore como se esperaba.[1][65]
Considere repetir la radiografía de tórax, la proteína C reactiva, el recuento de leucocitos y otras muestras para la microbiología en pacientes que no progresan satisfactoriamente después de 3 días de tratamiento.[1][65]
Practical tip
Las principales razones por las que los pacientes no mejoran como se esperaba incluyen:[1][65]
Diagnóstico incorrecto o afección con complicaciones (p. ej., embolia pulmonar, carcinoma bronquial, bronquiectasias)
Patógeno inesperado o patógenos no cubiertos por la elección de antibióticos (p. ej., patógenos "atípicos", patógenos resistentes a antibióticos de uso común, como Haemophilus influenzae resistente a la ampicilina)
Antibiótico ineficaz o que causa una reacción alérgica (p. ej., mala absorción de antibióticos orales, dosis inadecuada, hipersensibilidad a los antibióticos)
Deterioro de las defensas locales (p. ej., bronquiectasias, obstrucción endobronquial, aspiración) o sistémicas (p. ej., infección por VIH, mieloma)
Complicaciones locales (p. ej., derrame paraneumónico, empiema, absceso pulmonar) o a distancia (p. ej., infección metastásica, septicemia, flebitis en el sitio de la cánula intravenosa) de la NAC
Infección abrumadora
Se espera una mejoría demasiado pronto (por ejemplo, en pacientes mayores).
Alta hospitalaria
No dé de alta a los pacientes de forma rutinaria si han tenido 2* o más de los siguientes hallazgos presentes en las últimas 24 horas:[63]
Temperatura >37,5 °C (>99.5 °F)
Frecuencia cardíaca >100/minuto
Frecuencia respiratoria ≥24/minuto
Presión arterial sistólica ≤90 mmHg
Saturación de oxígeno <90% en el aire ambiente
Incapacidad para mantener la ingesta oral
Estado mental anormal.
(*El BTS recomienda basar su decisión de dar de alta a los pacientes con NAC en 1 o más de los hallazgos enumerados [a menos que representen el estado inicial habitual para ese paciente] y utiliza un umbral de temperatura de 37.8 °C [100.04 °F]. Ver +Debate a continuación.[1][65])
Considere retrasar el alta de los pacientes con NAC si su temperatura es superior a 37.5 °C (99.5 °F).[63]
Debate: Temperatura de corte para un alta hospitalaria segura
El BTS considera una temperatura >37.8°C (>100.04 °F), en lugar de los >37.5 °C (>99.5 °F) recomendado por NICE, como un hallazgo que debería llevarlo a considerar retrasar el alta en un paciente con NAC.[1][65]
El >37.5°C (>99.5 °F) El umbral recomendado por NICE se basa en las conclusiones de un estudio de cohorte prospectivo que analizó el valor de las variables clínicas simples para predecir los resultados a corto plazo en pacientes con neumonía.[63][141]
Encontró que un límite de 37.5 °C (99.5 °F) estaba fuertemente asociado con el riesgo de mortalidad a los 30 días.
Por esta razón, hemos basado nuestra recomendación en la orientación del NICE.
Al alta o en el seguimiento, ofrezca a los pacientes acceso a información sobre CAP, como un folleto de información para el paciente.[1][65]
Organice una visita de seguimiento alrededor de las 6 semanas, ya sea con el médico de cabecera del paciente o en una clínica hospitalaria.[1][65]
Seguimiento después del alta
Solicite una radiografía de tórax repetida durante la recuperación después de aproximadamente 6 semanas para los pacientes (independientemente de si han sido ingresados en el hospital):[1][65]
Consíntomas persistentes o signos físicos
Que tienen un mayor riesgo de neoplasia maligna subyacente (especialmente los fumadores y las personas de >50 años).
Considere la broncoscopia durante la recuperación en pacientes con signos, síntomas y alteraciones radiológicas persistentes alrededor de 6 semanas después de completar el tratamiento.[1][65]
Utilice la herramienta de riesgo de mortalidad CRB-65 y su juicio clínico para determinar qué pacientes son adecuados para el tratamiento en la comunidad (consulte nuestra sección anterior sobre Estratificación del riesgo).
Considere el tratamiento en el hogar para pacientes con una puntuación CRB-65 de 0 (gravedad baja) o una puntuación CRB-65 de 1 o 2 (gravedad media) si desean ser tratados en casa y cumplen con todos los siguientes criterios:[1][63][65]
Pueden recibir medicamentos orales de manera segura y confiable
Sus circunstancias sociales los hacen aptos para el tratamiento en el hogar
No presentan comorbilidades inestables.
Sin embargo, adopte un enfoque cauteloso al decidir si es seguro tratar a cualquier paciente con NAC de gravedad moderada (puntuación CRB-65 de 1 o 2) en el entorno comunitario. Estos pacientes tienen un mayor riesgo de muerte, particularmente aquellos con una puntuación CRB-65 de 2.Debe derivar a la mayoría para el tratamiento en el hospital.[1][63][65]
Si decide tratar al paciente en el entorno comunitario, siga las mismas recomendaciones de tratamiento que se indican a continuación para los pacientes con sospecha de NAC que se presentan en el entorno comunitario (gravedad baja).
Remitir a cualquier paciente que se presente en el entorno comunitario con una puntuación CRB-65 de 3 o más para su ingreso hospitalario inmediato (generalmente en ambulancia de luz azul en el Reino Unido).[1][63][65]
Practical tip
Si necesita derivar a un paciente para atención médica de emergencia en el hospital, es importante informar al equipo clínico del hospital que el paciente está en camino. Esto permitirá al hospital iniciar el tratamiento adecuado tan pronto como llegue el paciente.
Antibióticos
Las siguientes recomendaciones se basan en las guías de práctica British Thoracic Society (BTS) y el National Institute for Health and Care Excellence (NICE).[1][65][117]
Administrar antibióticos antes del traslado al hospital
NAC de gravedad alta (puntuación CRB-65 3 o 4)
Administrar antibióticos empíricos antes del traslado al hospital (generalmente en ambulancia de luz azul en el Reino Unido) a pacientes con sospecha de NAC considerada potencialmente mortal.[1][65] Se deben seguir los protocolos locales.
La primera opción es la bencilpenicilina intravenosa o la amoxicilina oral. La claritromicina es una alternativa para las personas alérgicas a la penicilina.[1]
Las guías de práctica clínica más recientes (2019) del NICE sobre la prescripción de antimicrobianos en adultos recomiendan amoxicilina/clavulanato más claritromicina (o eritromicina) de primera línea en personas con NAC de alta gravedad. Estas recomendaciones se basan principalmente en la opinión de los expertos, ya que la evidencia es limitada.[117]
Considere la posibilidad de administrar antibióticos antes del traslado hospitalario a pacientes con sospecha de NAC de alta gravedad, donde es probable que haya retrasos de más de 6 horas en el ingreso hospitalario y el tratamiento.[1][65]
Los antibióticos previos a la admisión pueden influir negativamente en los resultados de las pruebas diagnósticas microbiológicas posteriores, pero esto no se considera una razón para retener los antibióticos si un médico de medicina general lo considera indicado.[1]
NAC de gravedad moderada (puntuación CRB-65 1 o 2) y NAC de gravedad baja (puntuación CRB-65 0)
No administre antibióticos a pacientes con NAC de gravedad moderada o NAC de baja gravedad antes de la derivación al hospital.[1][65]
Antibióticos empíricos para el tratamiento domiciliario
Administrar antibióticos orales empíricos a pacientes tratados en el entorno comunitario.
Las opciones alternativas para los pacientes que son alérgicos a la penicilina son un macrólido (por ejemplo, claritromicina) o una tetraciclina (por ejemplo, doxiciclina).[1][65]
El NICE recomienda la claritromicina (o eritromicina) o la doxiciclina como alternativas a la amoxicilina para los pacientes alérgicos a la penicilina y para los pacientes en los que la amoxicilina no es adecuada (p. ej., si se sospecha una neumonía atípica). Las recomendaciones de NICE se basan principalmente en la opinión de expertos, ya que la evidencia es limitada.[117]
Considere agregar o cambiar a un macrólido si el paciente no responde a la amoxicilina.[1][65]
Considere si se ha realizado un diagnóstico correcto de NAC si un paciente no responde a los antibióticos empíricos iniciales.[1]
Considere la revisión clínica y radiográfica para buscar diagnósticos secundarios o complicaciones de la NAC, como derrame pleural/empiema, absceso pulmonar o empeoramiento del ensombrecimiento neumónico.[1]
Considere la posibilidad de cambiar los antibióticos empíricos iniciales, pero antes considere el cumplimiento y la absorción adecuada de un régimen oral.[1]
Administre antibioticoterapia durante 5 días.[117][125] El NICE recomienda:[117]
Prescribir el ciclo más corto que pueda ser eficaz para reducir el riesgo de resistencia a los antimicrobianos y minimizar el riesgo de efectos adversos
Suspenda el tratamiento después de 5 días a menos que los resultados microbiológicos sugieran un curso más prolongado o que el paciente no esté clínicamente estable. Esto debe basarse en su juicio clínico y en los siguientes criterios:[117][126]
Fiebre en las últimas 48 horas, o más de un signo de inestabilidad clínica:
Presión arterial sistólica <90 mmHg
Frecuencia cardíaca >100/minuto
Frecuencia respiratoria >24/minuto
Saturación arterial de oxígeno <90% o PaO 2 <60 mmHg en aire ambiente.
Manejo general
Aconseje a los pacientes que descansen, beban muchos líquidos y no fumen.[1]
Falta de respuesta
Aconsejar a los pacientes (y a sus cuidadores) que busquen asesoramiento médico si:[117]
Los síntomas empeoran de forma rápida o significativa
Los síntomas no comienzan a mejorar en 3 días
El paciente presenta un deterioro sistémico muy grave.
Alrededor del 10% de los pacientes atendidos en el entorno comunitario no responden al tratamiento con antibióticos y requieren hospitalización.[142]
Ingresar urgentemente en el hospital a cualquier paciente en tratamiento antibiótico con características de infección de gravedad moderada o alta.[1][65]
Solicitar una radiografía de tórax durante la recuperación después de aproximadamente 6 semanaspara los pacientes (independientemente de si los pacientes han sido ingresados en el hospital):[1][65]
Consíntomas persistentes o signos físicos
Que presentan un mayor riesgo de neoplasia maligna subyacente (especialmente las personas que fuman y las personas de >50 años).
Considere la broncoscopia durante la recuperación en pacientes con signos, síntomas y alteraciones radiológicas persistentes alrededor de 6 semanas después de completar el tratamiento.[1][65]
Para los pacientes ingresados en el hospital, la tasa de mortalidad oscila entre el 5% y el 15%, pero aumenta entre el 20% y el 50% en los pacientes que requieren ingreso en la unidad de cuidados intensivos (UCI).[6][118]
Los factores de riesgo asociados con el aumento de la mortalidad a los 30 días incluyen bacteriemia, ingreso en la UCI, comorbilidades (especialmente enfermedades neurológicas) e infección por un agente patógeno potencialmente resistente a múltiples fármacos (p. ej., Staphylococcus aureus, Pseudomonas aeruginosa, Enterobacteriaceae).[34][143][144][145]
Los pacientes tratados en el entorno comunitario generalmente tienen un buen pronóstico.[1][65]
El uso de este contenido está sujeto a nuestra cláusula de exención de responsabilidad
