Recomendações
Urgente
Suspeita de PAC em pacientes com sintomas e sinais de infecção aguda do trato respiratório inferior e, em ambiente hospitalar, com nova sombra radiográfica (consolidação) para a qual não há outra explicação.[1][63][64][65]
Durante a pandemia de COVID-19, considere que todos os pacientes com tosse, febre ou outros sintomas sugestivos têm COVID-19 até prova em contrário. Para pacientes com suspeita ou confirmação de pneumonia por COVID-19, consulte nosso tópico Coronavirus disease 2019 (COVID-19) Opens in new windowresistente.
A pneumonia devida à COVID-19 não é abordada neste tópico.
Pense: “ Isso poderia ser sepse? com base na deterioração aguda em um paciente adulto no qual há evidência clínica ou forte suspeita de infecção.[66][67]
Use uma abordagem sistemática, juntamente com seu julgamento clínico, para avaliação; consulte urgentemente um tomador de decisão clínica sênior (por exemplo, médico de nível ST4 no Reino Unido) se suspeitar de sepse.[67][68][69][70]
Consulte as diretrizes locais para a abordagem recomendada em sua instituição para avaliação e tratamento do paciente com suspeita de sepse. Veja Sepse em adultos.
Urgente: no hospital
Priorize uma radiografia torácica para todos os pacientes com suspeita de PAC dentro de 4 horas após a apresentação ao hospital.[1][63][65]
Solicite exames de sangue, incluindo:[1][65]
Saturações de oxigênio para orientar o tratamento de suporte
Gasometria arterial em pacientes com SpO 2 < 94%, aqueles com risco de insuficiência ventilatória hipercápnica (retenção de CO 2) e todos os pacientes com PAC de alta gravidade (consulte nossa seção Manejo- recomendações para obter mais detalhes sobre a avaliação da gravidade)
Ureia e eletrólitos para informar a gravidade
Hemograma completo, testes da função hepática e proteína C-reativa para auxiliar no diagnóstico e nas medições basais.
Avalie as necessidades de oxigênio. Prescreva oxigênio se a saturação de oxigênio for < 94% e mantenha-se na faixa alvo.[1][65] Em pacientes com risco de retenção de CO 2, prescreva oxigênio se saturação de oxigênio < 88%.[71]
Monitore a oxigenoterapia controlada. Um limite superior de SpO 2 de 96% é razoável quando se administra oxigênio suplementar à maioria dos pacientes com doenças agudas que não correm risco de hipercapnia.
As evidências sugerem que o uso liberal de oxigênio suplementar (SpO 2 > 96% alvo) em adultos com doenças agudas está associado a maior mortalidade do que a oxigenoterapia mais conservadora.[72]
Uma meta de SpO 2 mais baixa de 88% a 92% é apropriada se o paciente estiver em risco de insuficiência respiratória hipercápnica.[71]
Avalie o risco de mortalidade usando a pontuação CURB-65 e seu julgamento clínico para todos os pacientes com pneumonia confirmada por radiografia torácica (consulte nossa seção Manejo- recomendações completas para obter mais informações). [ Escore CURB-65 de gravidade de uma pneumonia. Opens in new window ] [1][63][65]
Pontuação 3-5: alta gravidade.
Pontuação 2: trate como pneumonia de gravidade moderada.[1][63][65]
Pontuação 0 ou 1: trate como pneumonia de baixa gravidade.[1][63][65]
Envie amostras de escarro e sangue para cultura de pessoas com PAC de gravidade moderada ou alta, de preferência antes de iniciar os antibióticos.[1][65] Considere o teste de antígeno urinário de legionela e pneumocócico.[63]
Meça as observações inicialmente pelo menos duas vezes ao dia e com mais frequência (por exemplo, a cada hora) em pessoas internadas em uma unidade de cuidados intensivos (unidade de alta dependência de cuidados ou unidade de terapia intensiva).[1][65]
Urgente: na comunidade
Faça uma radiografia torácica SOMENTE se não tiver certeza do diagnóstico e a radiografia o ajudará a controlar a doença aguda.[1][63][65]
Use a oximetria de pulso como parte de sua avaliação da gravidade da doença e para determinar a necessidade de oxigênio.[71]
Avalie o risco de mortalidade usando a pontuação CRB-65 (consulte Manejo - recomendações completas) e seu julgamento clínico para informar a gravidade.[1][63][65]
Principais recomendações
Apresentação
Pacientes com PAC geralmente apresentam sintomas e sinais consistentes com uma infecção do trato respiratório inferior (ou seja, tosse, dispneia, dor torácica pleurítica, escarro mucopurulento, mialgia, febre) e nenhuma outra explicação para a doença (por exemplo, sinusite ou asma).[63]
Lembre-se de considerar apresentações atípicas (sem sinais torácicos óbvios). Por exemplo:
A pneumonia por micoplasma em adultos jovens pode se manifestar como dor de garganta, dor de cabeça, náuseas, dor abdominal e diarreia[73]
A pneumonia por Legionella pode se apresentar como transtorno constitucional, diarreia e confusão[73]
A pneumonia por Pneumocystis em pessoas imunossuprimidas pode se manifestar apenas como tosse, dispneia e hipóxia acentuada[73]
Os idosos frequentemente apresentam sintomas inespecíficos (especialmente confusão) e piora de condições pré-existentes e sem sinais torácicos ou febre[1][65]
Algumas pessoas apresentam estados confusionais agudos.[73]
Não use apenas as características clínicas para prever o agente causador ou influenciar sua escolha inicial de antibiótico.[1][65][74]
Estratificação de risco
Determine se o paciente deve ser tratado no hospital ou em casa usando a pontuação de risco de mortalidade CURB-65 (ambiente hospitalar) ou a pontuação CRB-65 (ambiente comunitário) (consulte nossa seção Manejo - recomendações para obter mais detalhes sobre estratificação de risco). [ Escore CURB-65 de gravidade de uma pneumonia. Opens in new window ] [1][63][65]
Estratificação de risco no hospital*
Gravidade da PAC | Índice CURB-65 | Decisão de manejo |
|---|---|---|
Alto | 4 ou 5 | Providencie uma avaliação de emergência por um especialista em cuidados intensivos[1][63][65] |
3 | Discuta com um colega sênior na primeira oportunidade e trate como uma pneumonia de alta gravidade[1][63][65] | |
Moderado | 2 | Considere o tratamento hospitalar de curta duração ou o tratamento ambulatorial supervisionado por um hospital[1][63][65] |
Baixo | 0 ou 1 | |
*Todos os pacientes com PAC confirmados por radiografia torácica. | ||
Estratificação de risco na comunidade
Gravidade da PAC | CRB-65 | Decisão de manejo |
|---|---|---|
Alto | 3 ou mais | |
Moderado | 1 ou 2 | Considere o encaminhamento hospitalar para avaliação e tratamento*[1][63][65] |
Baixo | 0 |
Exames por imagem
Confirme o diagnóstico por radiografia torácica em todos os pacientes que se apresentam ao hospital com suspeita de PAC.[1][63][65]
O diagnóstico definitivo de PAC requer evidências de consolidação na radiografia torácica.[75]
Em ambientes comunitários, baseie o diagnóstico em sinais e sintomas de infecção do trato respiratório inferior, sinais torácicos focais e gravidade da doença.[1][63][65]
Investigações adicionais
Discuta com um colega sênior qualquer paciente que não melhore conforme o esperado.[1][65]
Considere repetir a radiografia torácica, proteína C-reativa, contagem de leucócitos e outras amostras para microbiologia em pacientes que não evoluem satisfatoriamente após 3 dias de tratamento.[1][65]
Em pacientes com PAC de alta gravidade que não respondem aos antibióticos betalactâmicos ou nos quais você suspeita de um patógeno atípico ou viral solicite a reação em cadeia da polimerase (ou outro teste de detecção de antígeno) do escarro ou de outra amostra do trato respiratório.[1][65]
Na comunidade, avalie a oxigenação por meio da oximetria de pulso.[71]
A saturação de oxigênio < 94% é um fator prognóstico adverso na PAC e também geralmente uma indicação para oxigenoterapia.[76]
Considere o encaminhamento hospitalar urgente desses pacientes.[1][65]
Investigações gerais não são necessárias na maioria dos pacientes presentes na comunidade, mas você deve considerar um teste de proteína C-reativa no local de atendimento se não conseguir fazer um diagnóstico de PAC a partir da avaliação clínica e não tiver certeza se os antibióticos são indicados.[1][63][65]
Durante a pandemia de COVID-19, solicite um teste de amplificação de ácido nucleico, como PCR em tempo real, para SARS-CoV-2 em qualquer paciente com suspeita de infecção sempre que possível.[77][78] Veja nosso tópico Coronavirus disease 2019 (COVID-19) Opens in new windowresistente.
Nenhuma constelação de sinais e sintomas é preditiva de PAC. No entanto, os pacientes geralmente apresentam:[1][63][64][65]
Sintomas e sinais consistentes com uma infecção do trato respiratório inferior:
Tosse e pelo menos um outro sintoma do trato respiratório:
Pelo menos uma característica sistêmica:
Calafrios ou sudorese noturna – geralmente presentes, mas menos comuns em pacientes idosos[1]
Febre (> 38ºC [> 100ºF]) –pacientes idosos podem estar afebris[1]
Sintomas inespecíficos – podem incluir mialgia, letargia, mal-estar, anorexia. A confusão é frequentemente observada empacientes mais velhos[1]
Novos sinais torácicos focais no exame, como estertores ou sopro tubário
Nenhuma outra explicação para a doença.
Lembre-se de considerar apresentações atípicas da PAC (ou seja, sem sinais torácicos óbvios). Por exemplo:
A pneumonia por micoplasma em adultos jovens pode se manifestar como dor de garganta, dor de cabeça, náuseas, dor abdominal e diarreia[73]
A pneumonia por Legionella pode se apresentar como transtorno constitucional, diarreia e confusão[73]
A pneumonia por Pneumocystis nos imunossuprimidos pode se manifestar apenas com tosse, dispneia e hipóxia acentuada[73]
Os idosos frequentemente apresentam sintomas inespecíficos (por exemplo, letargia, mal-estar, anorexia, confusão) e piora de condições pré-existentes e sem sinais torácicos ou febre[1]
Algumas pessoas apresentam estados confusionais agudos.[73]
Considere a velocidade do início dos sintomas em seu diagnóstico diferencial:
Os sintomas que se desenvolvem em minutos podem ser sugestivos de embolia pulmonar, pneumotórax ou etiologia cardíaca.
Practical tip
Pense: “ Isso poderia ser sepse?" com base na deterioração aguda em um paciente adulto no qual há evidência clínica ou forte suspeita de infecção.[66][67][68] Consulte Sepse em adultos .
O paciente pode apresentar sintomas inespecíficos ou não localizados (por exemplo, mal-estar agudo com temperatura normal) ou pode haver sinais graves com evidência de disfunção em múltiplos órgãos e choque.[66][67][68]
Lembre-se de que a sepse representa o fim grave e potencialmente fatal da infecção.[79]
A pneumonia é uma das principais fontes de sepse.[80]
Use uma abordagem sistemática (por exemplo, National Early Warning Score 2 [NEWS2]), juntamente com seu julgamento clínico, para avaliar o risco de deterioração devido à sepse.[66][68][69][81] Consulte as diretrizes locais para obter a abordagem recomendada em sua instituição.
Organize uma revisão urgente por um tomador de decisão clínica sênior (por exemplo, médico de nível ST4 no Reino Unido) se você suspeitar de sepse:[70]
Dentro de 30 minutos para um paciente que está gravemente doente (por exemplo, pontuação NEWS2 de 7 ou mais, evidência de choque séptico ou outros problemas clínicos significativos).
Dentro de 1 hora para um paciente gravemente doente (por exemplo, pontuação NEWS2 de 5 ou 6).
Siga seu protocolo local para investigação e tratamento de todos os pacientes com suspeita de sepse ou aqueles em risco. Inicie o tratamento imediatamente. Determine a urgência do tratamento de acordo com a probabilidade de infecção e a gravidade da doença, ou de acordo com seu protocolo local.[70][81]
Na comunidade: encaminhe para atendimento médico de emergência no hospital (geralmente por ambulância de luz azul no Reino Unido) qualquer paciente que esteja gravemente doente com suspeita de infecção e seja:[67]
Considerado de alto risco de deterioração devido à disfunção orgânica (conforme medido pela estratificação de risco)
Com risco de sepse neutropênica.
Alguns sintomas e sinais são mais comuns com patógenos específicos.[1]
No entanto, não use apenas as características clínicas para prever o agente causador ou para influenciar sua escolha inicial de antibiótico.[1][65][74]
Patógenos típicos que causam PAC em adultos no Reino Unido e suas características mais comumente associadas[1]
Patógenos | Características clínicas mais comumente associadas | Outras características |
|---|---|---|
Streptococcus pneumoniae | Início agudo, febre alta e dor torácica pleurítica | Patógeno geral mais comum Mais provável na presença de comorbidade cardiovascular, aumento da idade A bactéria S pneumoniae é mais provável em:
|
Haemophilus influenzae | Sem características definidoras específicas | Mais provável em pessoas idosas e com DPOC |
Legionella pneumophila | Diarreia, encefalopatia e outros sintomas neurológicos, maior probabilidade de infecção grave e evidência de envolvimento multissistêmico (por exemplo, testes anormais da função hepática, elevação da creatina quinase sérica) | Mais provável em pacientes jovens sem comorbidades, fumantes, pessoas imunocomprometidas, pessoas expostas a sistemas de água artificial contaminados (por exemplo, aparelhos de ar condicionado, spas, fontes, reparo de sistemas de encanamento doméstico) Maior frequência em doenças graves (pacientes na unidade de terapia intensiva) Informe-se sobre viagens ao exterior |
Staphylococcus aureus | Sem características definidoras específicas | Mais provável se houver infecção por influenza anterior ou simultânea Maior frequência em doenças graves (pacientes na unidade de terapia intensiva) Informe-se sobre os sintomas da influenza, pois eles têm valor preditivo. A infecção pelo vírus influenza pode ser complicada pela infecção co-/secundária com S. aureus |
Patógenos atípicos que causam PAC em adultos no Reino Unido e suas características mais comumente associadas[1]
Patógenos | Características clínicas mais comumente associadas | Outras características |
|---|---|---|
Pneumonia por micoplasma | Em adultos jovens pode se manifestar como faringite, cefaleia, náuseas, dor abdominal e diarreia[73] | Mais provável em pacientes mais jovens As epidemias ocorrem em ciclos de aproximadamente 4 anos |
Chlamydophila pneumoniae | Sem características definidoras específicas | Nenhum |
Coxiella burnetii | História de tosse seca e febre alta | Mais provável em homens A exposição a fontes animais infectadas (especialmente durante o parto) é o principal elo epidemiológico[82] |
Klebsiella pneumoniae | Sem características definidoras específicas | Pessoas com dependência de álcool correm maior risco de pneumonia bacteriêmica e fatal por Klebsiella |
Seu histórico deve abranger os fatores de risco para ajudá-lo a avaliar se o paciente tem PAC, uma infecção do trato respiratório inferior ou um diagnóstico alternativo. Você também deve identificar os fatores que podem influenciar o plano de manejo se a PAC for diagnosticada.
Esteja ciente de que você não pode fazer um diagnóstico definitivo de PAC apenas com base na história.
História médica
(*Denota um forte fator de risco para a PAC.)
Doenças crônicas respiratórias:
Outras comorbidades crônicas:
Practical tip
Considere pneumonite/pneumonia por aspiração em pacientes com alto risco de aspiração, como aqueles com dificuldades crônicas de deglutição, aqueles com condições neurológicas orgânicas (por exemplo, doença de Parkinson, AVC, demência) ou aqueles que não conseguem proteger suas vias aéreas facilmente.[1]
História social
Idade ≥65 anos*
A incidência de PAC aumenta significativamente com a idade. A idade avançada está associada a uma maior mortalidade por PAC.[10]
Residência em um lar de idosos*
Contato com crianças*
O contato regular com crianças está associado a um aumento do risco de PAC.[49]
A PAC é mais grave em homens que em mulheres, o que leva à maior mortalidade em homens em geral e, especialmente, naqueles com idade avançada.[86]
História do estilo de vida
Uso/uso indevido de álcool*
As pessoas que consomem álcool ou em quantidades maiores têm um risco 83% maior de PAC em comparação com as pessoas que não consomem álcool ou consomem quantidades menores (risco relativo de 1.83).[43] Para cada 10 a 20 g a mais de ingestão de álcool por dia, há um aumento de 8% no risco de PAC.[43]
Tabagismo*
Higiene bucal ineficiente
A má higiene bucal (particularmente a disestesia dentária e o uso de próteses dentárias) pode contribuir para um maior risco de PAC em adultos.[87]
História de medicamentos
Inibidores da bomba de prótons, antagonistas H2 e opioides prescritos (particularmente opioides imunossupressores) estão associados à PAC.[59]
Realize um exame completo, particularmente do sistema cardiorrespiratório, para identificar características consistentes com PAC.
Verifique se:
Febre (> 38ºC [> 100ºF])
Frequência respiratória elevada
Taquicardia
Sinais torácicos focais – nenhum, alguns ou todos podem estar presentes:
Estertores
sopro tubário
Expansão torácica reduzida
Macicez à percussão (sugere consolidação e/ou derrame pleural)
Diminuição da entrada de ar.
Além disso, concentre-se em outras áreas (por exemplo, garganta, pernas) se a apresentação sugerir um diagnóstico alternativo, como infecção do trato respiratório superior, trombose venosa profunda ou embolia pulmonar.
no hospital
Todos os pacientes na apresentação
Envie todos os pacientes atendidos no hospital com suspeita de PAC para uma radiografia torácica o mais rápido possível para confirmar o diagnóstico e dentro de 4 horas após a apresentação ao hospital.[1][63][65]
Nova sombra (consolidação) na radiografia torácica confirma o diagnóstico de PAC[1][63][65]
Reavalie o paciente se a radiografia torácica não mostrar consolidação.[1][Figure caption and citation for the preceding image starts]: Radiografia de tórax posteroanterior mostrando consolidação do lobo superior direito em um paciente com pneumonia adquirida na comunidadeDurrington HJ, et al. Recent changes in the management of community acquired pneumonia in adults. BMJ 2008;336:1429. [Citation ends].
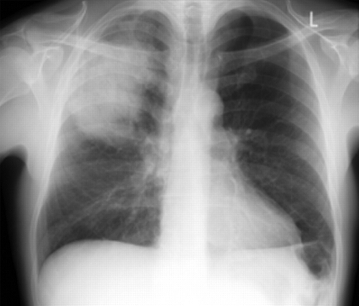
Practical tip
Uma radiografia torácica de alta qualidade é importante para garantir um diagnóstico preciso e evitar a prescrição inadequada de antibióticos. Um estudo relatou que 29% dos pacientes hospitalizados tratados por PAC não tinham anormalidades radiográficas.[88]
Lembre-se de que é mais difícil obter uma imagem de alta resolução de uma pessoa com obesidade classe III (índice de massa corporal ≥40).
Reservado para circunstâncias específicas
Considere uma tomografia computadorizada (TC) de tórax se a radiografia for de baixa qualidade ou se houver uma consolidação mal definida.[1]
Considere uma tomografia computadorizada de tórax ou outras investigações de imagem para pneumonia “complicada” ou alterações atípicas em uma radiografia torácica, como cavitação, padrão de consolidação multifocal ou derrame pleural.[89][Figure caption and citation for the preceding image starts]: Radiografia de tórax mostrando pneumonia cavitando no lobo superior esquerdoDa coleção do Dr. Jonathan Bennett. Usado com permissão [Citation ends].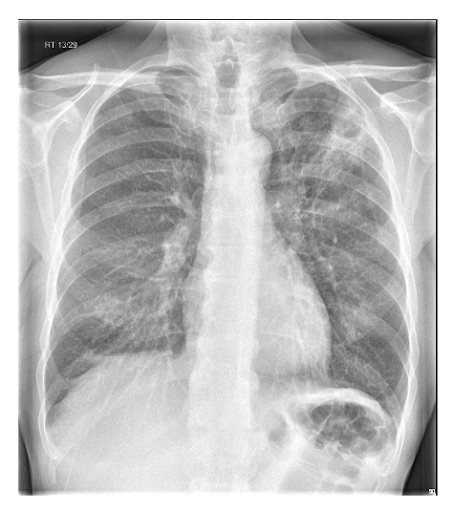
[Figure caption and citation for the preceding image starts]: Derrame pleural no lado esquerdoDa coleção do Dr. R Light. Usado com permissão [Citation ends].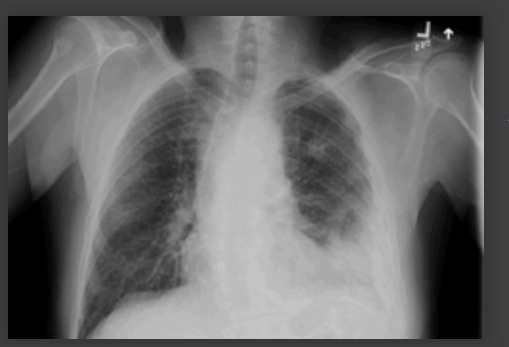
[Figure caption and citation for the preceding image starts]: Opacificação aumentada da região peri-hilar direita e do segmento superior dos lobos inferior e superior direitos, compatível com agravamento da pneumonia por aspiraçãoDa coleção do Dr. Roy Hammond. Usado com permissão [Citation ends].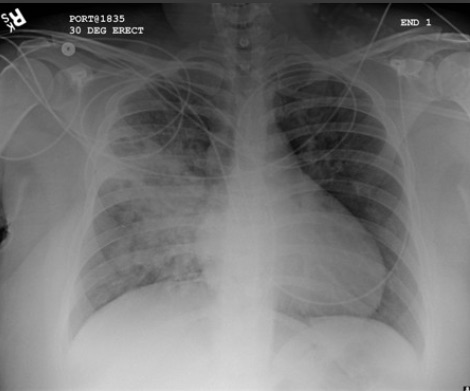
Achados radiográficos | Exames de imagem adicionais | Considere um diagnóstico alternativo |
|---|---|---|
Cavitação | Tomografia de tórax |
|
Consolidação multifocal (observe que é a natureza multifocal, não a consolidação, que é a característica distintiva) | Tomografia de tórax |
|
Derrame pleural | Ecografia de tórax +/- aspiração guiada +/- tomografia computadorizada de tórax |
|
Practical tip
Pneumonia “complicada” refere-se à pneumonia com presença de derrame parapneumônico (um derrame pleural exsudativo associado à infecção pulmonar), empiema (pus no espaço pleural), abscesso, pneumotórax, pneumonia necrosante ou fístula broncopleural.
Cerca de 40% das pessoas hospitalizadas por pneumonia desenvolvem derrame parapneumônico.[90] O empiema é um tipo de derrame pleural difícil de distinguir de um derrame parapneumônico na radiografia torácica.
Os achados de uma tomografia computadorizada sugestiva de derrame parapneumônico (em oposição ao empiema) incluem:[91]
Volume geralmente pequeno
Sinal normal do menisco
dependente
Sem loculação.
O “sinal de pleura dividida” não é típico e é mais específico para o empiema.
Considere a angiografia pulmonar por TC (APTC) para descartar embolia pulmonar se os sintomas surgirem rapidamente (em minutos) ou se a dor e a dispneia precederem os sintomas infecciosos.[92]
Na comunidade
Não solicite uma radiografia torácica para pacientes com suspeita de PAC vistos na comunidade, a menos que:[1][63][65]
Hádúvida diagnóstica
O paciente é considerado em risco de patologia pulmonar subjacente (por exemplo, ele tem fatores de risco para câncer de pulmão)
O progresso após o tratamento não é satisfatório na revisão.
Em cenários comunitários, baseie o diagnóstico em sinais e sintomas de infecção do trato respiratório inferior, sinais torácicos focais e gravidade da doença.[1][63][65]
Debate: a ultrassonografia no diagnóstico da PAC
Embora uma radiografia torácica mostrando um novo sombreamento que não possa ser atribuído a nenhuma outra causa seja o “padrão ouro” para o diagnóstico de pneumonia, ela nem sempre é viável em um cenário comunitário e envolve exposição à radiação.
Novas evidências mostraram que a ultrassonografia pulmonar é um possível teste diagnóstico preciso para pessoas com PAC. No entanto, os benefícios de seu uso na prática em relação à radiografia torácica ainda não estão claros.
Uma metanálise de 12 estudos que analisaram a precisão diagnóstica da ultrassonografia pulmonar em pessoas com PAC encontrou uma sensibilidade e especificidade de 0.88 e 0.86, respectivamente.[93] No entanto, houve limitações, como a grande variabilidade nos achados e a falta de heterogeneidade dos estudos revisados.
Mais evidências são necessárias antes que as recomendações possam ser feitas.
Investigações gerais
Em um ambiente hospitalar
Realize os seguintes testes para todos os pacientes internados no hospital.
Comece com saturações de oxigênio e ureia (e eletrólitos), pois elas informarão o tratamento de suporte e a gravidade, respectivamente:[1][65]
Oximetria de pulso (preferencialmente ao respirar ar) para avaliar as saturações de oxigenação.
A saturação de oxigênio < 94% é um fator prognóstico adverso em pacientes com PAC e pode ser uma indicação para oxigenoterapia.[76]
Medições da gasometria arterial (ABG) em pacientes recebendo oxigenoterapia.[71]
Meça o ABG em pacientes com SpO 2 <94% , aqueles com risco de insuficiência ventilatória hipercápnica (retenção de CO 2) e todos os pacientes com PAC de alta gravidade.[1]
Ureia (e eletrólitos) para informar a gravidade da doença.
Practical tip
Sempre registre claramente a concentração de oxigênio inspirado, pois isso é essencial para interpretar os resultados da gasometria.
Solicite hemograma completo, proteína C reativa e teste da função hepática para ajudar a identificar a patologia subjacente ou associada e para medições basais.[1][65]
Hemograma completo . A leucocitose é frequentemente observada em pessoas com PAC:
Uma contagem de leucócitos de >15 x 10 9/L indica uma etiologia bacteriana (particularmente pneumocócica).[1]
Proteína C reativa (PCR) para ajudar a descartar outras doenças respiratórias agudas e como medida inicial:
Um nível >100 mg/L torna provável a pneumonia[94]
Altos níveis de proteína C-reativa não indicam necessariamente que a pneumonia seja bacteriana ou SARS-CoV-2, mas níveis baixos de PCR tornam menos provável uma infecção bacteriana secundária.[95]
Um nível <20 mg/L com sintomas por mais de 24 horas torna a presença de pneumonia altamente improvável[94]
A falha na proteína C-reativa de 50% ou mais no dia 4 está associada ao aumento do risco de mortalidade em 30 dias, necessidade de ventilação mecânica e/ou suporte inotrópico e complicações.[96]
Testes da função hepática para avaliar a função hepática:
Considere solicitar a procalcitonina sérica. A procalcitonina basal é cada vez mais usada em ambientes de cuidados intensivos e no pronto-socorro para orientar as decisões sobre o tratamento com antibióticos em pacientes com alta suspeita de sepse e naqueles com suspeita de infecção bacteriana.[81][97][98][99][100]
Valores aumentados de procalcitonina estão correlacionados com pneumonia bacteriana, enquanto valores mais baixos estão correlacionados com pneumonia viral e atípica. A procalcitonina é especialmente elevada em casos de pneumonia pneumocócica.[101][102]
A procalcitonina é um peptídeo precursor da calcitonina, responsável pela homeostase do cálcio. Atualmente, está excluído das principais diretrizes, mas é cada vez mais usado na prática.
Realize toracocentese precoce em todos os pacientes com derrame pleural, pois isso pode revelar um espaço pleural infectado consistente com um derrame parapneumônico ou empiema.[1][65]
Drene o líquido pleural em pacientes com empiema ou líquido pleural claro com pH <7.2.[1]
Monitoramento
Meça as observações inicialmente pelo menos duas vezes ao dia e com mais frequência (por exemplo, a cada hora) em pacientes internados em uma unidade de cuidados intensivos (unidade de alta dependência ou unidade de terapia intensiva).[1][65]
Pulso
Pressão arterial
Frequência respiratória
Temperatura
Pressão arterial
Saturação de oxigênio (com um registro da saturação de oxigênio inspirado ao mesmo tempo)
Estado mental.
Todos os pacientes com PAC de alta gravidade (alto risco de morte) devem ser revisados pelo menos a cada 12 horas até a melhora.[1][65] Isso deve ser feito por um colega sênior e pela equipe médica.[1][65]
Na comunidade
Investigações gerais não são necessárias para a maioria dos pacientes com PAC que são tratados na comunidade.[1][65] No entanto, você deve considerar uma proteína C reativa (PCR) no local de atendimento se não conseguir fazer um diagnóstico de PAC a partir da avaliação clínica e não estiver claro se os antibióticos devem ser prescritos.[63]
Avalie a oxigenação por meio da oximetria de pulso.[71]
A saturação de oxigênio <94% é um fator prognóstico adverso na PAC e também pode ser uma indicação para oxigenoterapia.[76]
Investigações microbiológicas
Esteja ciente de que a extensão dos testes microbiológicos em um paciente individual é guiada pela gravidade, presença de fatores de risco (por exemplo, DPOC) e surtos de doenças (por exemplo, pneumonia por legionella).[1][65]
no hospital
Não realize testes microbiológicos rotineiramente em pacientes com PAC de baixa gravidade presentes no hospital.[1][65] A antibioticoterapia empírica está associada a um bom prognóstico nesses pacientes.[1]
Hemoculturas
Solicite hemoculturas, de preferência antes da administração de antibióticos, em todos os pacientes com PAC de gravidade moderada ou alta (conforme determinado pelo escore CURB-65 — consulte nossa seção de recomendações de tratamento).[1][63][65]
O isolamento de bactérias pode ser altamente específico na determinação da etiologia microbiana em pessoas com PAC moderada ou grave.[1][63][65]
A bacteriemia também é um marcador da gravidade da doença. No entanto, muitos pacientes com PAC não têm bacteremia associada.[1] As causas microbianas da PAC que podem ser associadas à bacteremia incluem:[1]
Não solicite hemoculturas em pacientes com PAC confirmada que tenham doença de baixa gravidade e sem comorbidades.[1][65]
Debate: hemoculturas
Há um debate sobre a praticidade de solicitar hemoculturas de rotina em pacientes hospitalizados com PAC. Isso se deve principalmente à baixa sensibilidade, ao custo e ao fato de que os resultados raramente influenciam o manejo antimicrobiano.
Em um estudo com 355 pacientes internados no hospital por PAC, a proporção de hemoculturas falso-positivas foi de 10% e a proporção de verdadeiros positivos foi de 9% (IC de 95%, 3.3% a 5.5%).[104]
A antibioticoterapia foi alterada com base nos resultados da hemocultura em apenas 5% dos pacientes (IC de 95%, 3% a 8%).[104]
No entanto, apesar dessas limitações, a maioria dos especialistas ainda recomenda hemoculturas em pacientes com PAC de alta gravidade.[1]
Culturas de escarro
Envie culturas de escarro em:
Todos os pacientes com PAC de gravidade moderada ou alta (conforme determinado pelo escore CURB-65).[63] A British Thoracic Society recomenda culturas de escarro em pacientes comPAC de gravidade moderada somente se eles não tiverem recebido antibioticoterapia prévia[1][65]
Pacientes que não melhoram independentemente da gravidade da doença (escarro ou outras amostras respiratórias).[1][65]
Coloração de Gram de culturas de escarro
Solicite a coloração de Gram de culturas de escarro em pacientes com PAC de alta gravidade ou complicações, se disponível em seu laboratório local.[1][65]
A coloração de Gram é um indicador imediato do provável patógeno e pode ajudar na interpretação dos resultados da cultura.[1][65]
Evidência: coloração de Gram no escarro
Um estudo prospectivo de 1390 pacientes com PAC bacterêmica encontrou uma sensibilidade à coloração de Gram no escarro de:[105]
82% para pneumonia pneumocócica
79% para pneumonia por H influenzae
76% para pneumonia estafilocócica.
As especificidades variaram de 93% a 96%.
Practical tip
A realização de colorações de Gram de escarro de rotina para todos os pacientes é desnecessária.[1] O teste tem baixa sensibilidade e especificidade e, muitas vezes, não contribui para o manejo inicial. Os problemas incluem:[1]
Os pacientes podem não ser capazes de produzir boas amostras
Exposição prévia a antibióticos
Atrasos no transporte e processamento de amostras, o que reduz o rendimento de patógenos bacterianos
Dificuldade em interpretar os resultados devido à contaminação da amostra pela flora do trato respiratório superior, que pode incluir patógenos potenciais, como S. pneumoniae e 'coliformes' (especialmente em pacientes que já receberam antibióticos).
Teste de antígeno urinário
Considere os testes de antígeno urinário pneumocócico para pessoas com PAC de gravidade moderada ou alta.[63]
O teste de antígeno urinário é útil para diagnosticar pneumonia pneumocócica em adultos e é menos afetado do que as culturas de sangue/escarro pela antibioticoterapia prévia.[1][65]
Evidência: teste de antígeno urinário para pneumonia pneumocócica
Estudos mostraram taxas de sensibilidade significativamente maiores para o teste de antígeno urinário pneumocócico do que para culturas de sangue ou escarro de rotina.[106]
Os resultados permanecem positivos em 80% a 90% dos pacientes por até 7 dias após o início do tratamento antimicrobiano.[106]
Debate: grupos de pacientes para testes pneumocócicos
As diretrizes da British Thoracic Society (BTS) e do National Institute for Health and Care Excellence (NICE) diferem em suas recomendações sobre quem deve ser testado para pneumonia pneumocócica usando antígeno urinário.
O BTS recomenda testar todos os pacientes com PAC de alta gravidade,[1] enquanto o NICE recomenda considerar o teste em pacientes com PAC de gravidade moderada ou alta.[63][65]
Uma comparação posterior feita pela BTS das principais recomendações das duas diretrizes (BTS publicada em 2009 e NICE em 2014) concluiu que não havia grandes diferenças entre elas e, onde houvesse diferenças, os médicos deveriam seguir a diretriz do NICE em vez da diretriz do BTS.[107]
Solicite testes de antígeno urinário de legionella em todos os pacientes com fatores de risco específicos e para todos os pacientes com PAC durante surtos.[1][65] Considere testar também para pessoas com PAC de gravidade moderada ou alta.[63]
É importante que a pneumonia por legionella seja diagnosticada imediatamente, pois está associada a uma mortalidade significativa e tem importância para a saúde pública.[1][65]
A detecção do antígeno urinário de Legionella pneumophila por imunoensaio enzimático permite resultados rápidos no início da doença.[1][65]
O teste do antígeno de Legionella por imunoensaio enzimático é altamente específico (>95%) e sensível (80%) para detectar o sorogrupo 1 de L pneumophila, que é a causa mais comum de PAC e PAC esporádica devido a viagens ao exterior no Reino Unido.[108]
Debate: grupos de pacientes para testes de legionella
As diretrizes da British Thoracic Society (BTS) e do National Institute for Health and Care Excellence (NICE) diferem em suas recomendações em relação aos grupos de pacientes que devem ser testados para pneumonia por legionella usando antígeno urinário.
A BTS recomenda testar apenas pacientes com PAC de alta gravidade, pacientes com fatores de risco e todos os pacientes com PAC durante surtos,[1] enquanto o NICE recomenda que os médicos considerem fazer testes em pessoas com PAC de gravidade moderada ou alta.[63][65]
Uma comparação posterior feita pela BTS das principais recomendações das duas diretrizes (BTS publicada em 2009 e NICE em 2014) concluiu que não havia grandes diferenças entre elas e, onde houvesse diferenças, os médicos deveriam seguir a diretriz do NICE em vez da diretriz do BTS.[107]
Na comparação, a BTS também afirmou que sua recomendação de testar a legionela em pacientes com fatores de risco e em todos os pacientes com PAC durante surtos permanece válida, pois não foi examinada pelo NICE.[107]
Se o teste de antígeno urinário de legionella for positivo lembre-se de solicitar culturas de escarro de amostras respiratórias (por exemplo, obtidas por broncoscopia) para espécies de Legionella. Isso é para ajudar na investigação de surtos e fontes para evitar novos casos.[1][65]
Reação em cadeia da polimerase (PCR) e testes sorológicos
Use reação em cadeia da polimerase de escarro ou outras amostras do trato respiratório para vírus respiratórios (influenza A e B, parainfluenza 1-3, adenovírus, vírus sincicial respiratório) e patógenos atípicos (Mycoplasma pneumoniae, Chlamydophila pneumoniae, Chlamydophila psittaci, Coxiella burnetii e Pneumocystis jirovecii [se houver risco]) em pacientes com PAC de alta gravidade:[1][65]
Se não responder aos antibióticos betalactâmicos
Se houver uma forte suspeita de um patógeno “atípico”.
Durante a pandemia de COVID-19, solicite um teste de amplificação de ácido nucleico, como PCR em tempo real, para SARS-CoV-2 em qualquer paciente com suspeita de infecção sempre que possível.[77][78] Veja nosso tópico Coronavirus disease 2019 (COVID-19) Opens in new window
Geralmente, não é possível diferenciar a pneumonia bacteriana adquirida na comunidade da COVID-19 a partir de sinais e sintomas. No entanto, os pacientes com pneumonia bacteriana têm maior probabilidade de desenvolver rapidamente sintomas e escarro purulento. Eles são menos propensos a ter mialgia, anosmia ou dor pleurítica.[109]
Considere o antígeno urinário a reação em cadeia da polimerase de amostras do trato respiratório superior (por exemplo, esfregaços de nariz e garganta) ou inferior (por exemplo, escarro) ou investigações sorológicas em pacientes com PAC de gravidade moderada ou baixa:[1]
Durante surtos (por exemplo, doença do legionário)
Durante epidemias de micoplasma, ou
Quando há uma razão clínica ou epidemiológica específica
Se disponível, a reação em cadeia da polimerase é preferível às investigações sorológicas.
Na comunidade
Não solicite exames microbiológicos rotineiramente em pacientes que apresentam PAC na comunidade, pois:[1][63][65]
Esses pacientes geralmente não estão gravemente doentes e têm baixo risco de morte[1]
Atrasos no transporte de amostras para o laboratório reduzem a produção de patógenos bacterianos (especialmente S pneumoniae) nas culturas de escarro, e os resultados geralmente são recebidos tarde demais pelo clínico geral para ter qualquer impacto no manejo inicial.[1]
Só considere solicitar testes microbiológicos na comunidade se:[1][65]
Os sintomas do paciente não melhoram com a antibioticoterapia empírica
Considere o exame de escarro
O paciente tem uma tosse produtiva persistente, especialmente se também apresentar mal-estar, perda de peso, sudorese noturna ou fatores de risco para tuberculose (por exemplo, origem étnica, privação social, pacientes idosos, história prévia de tuberculose, histórico de contato com tuberculose)
Considere o exame de escarro para Mycobacterium tuberculosis
Há uma razão clínica ou epidemiológica, como umsurto (por exemplo, doença do legionário) ou durante epidemias de micoplasma
Considere o antígeno urinário, a reação em cadeia da polimerase de amostras do trato respiratório superior (por exemplo, esfregaços do nariz e garganta) ou inferior (por exemplo, escarro) ou investigações sorológicas. Se disponível, a reação em cadeia da polimerase é preferível às investigações sorológicas.[1][65]
Durante a pandemia de COVID-19, solicite um teste de amplificação de ácido nucleico, como PCR em tempo real, para SARS-CoV-2 em qualquer paciente com suspeita de infecção sempre que possível.[77][78] Veja nosso tópico Coronavirus disease 2019 (COVID-19) Opens in new window
Resumo das recomendações para investigações microbiológicas da British Thoracic Society (BTS) e do National Institute for Health and Care Excellence (NICE)[1][63][65]
Gravidade da PAC e local de tratamento | Testes microbiológicos preferidos |
|---|---|
Alta severidade (CURB-65 = 3-5; CRB-65 = 3-4): tratamento no hospital |
|
Gravidade moderada (CURB-65 = 2; CRB-65 = 1-2): tratamento no hospital |
|
Baixa gravidade (CURB-65 = 0-1; CRB-65 = 0): tratar em casa ou no hospital |
|
*Se disponível, a reação em cadeia da polimerase é preferível às investigações sorológicas.[1][65] | |
Practical tip
Na prática clínica de rotina, os patógenos são identificados apenas em cerca de um terço a um quarto dos pacientes com PAC internados no hospital.[1] Apesar disso, identificar o organismo causador da PAC e os padrões de sensibilidade é importante porque:[1]
Permite a seleção adequada de esquemas de antibioticoterapia. A mudança para antibioticoterapia direcionada e de espectro estreito é recomendada assim que o patógeno for identificado, a menos que haja preocupações de infecção dupla
Detecta certos patógenos com importância para a saúde pública e/ou aqueles que causam doenças graves que requerem tratamento diferente dos antibióticos empíricos padrão. Eles incluem:
Espécies de Legionella
Influenza A e B, incluindo influenza aviária A H5N1 e influenza aviária A H7N9
Coronavírus da síndrome respiratória do Oriente Médio (MERS-CoV) e coronavírus da síndrome respiratória aguda grave (SARS-CoV)
S aureus resistente à meticilina associado à comunidade (CA-MRSA)
Agentes do bioterrorismo
Outros patógenos novos
Permite o monitoramento do espectro de organismos que causam PAC ao longo do tempo. Isso é importante para estabelecer padrões de sensibilidade.
no hospital
Discuta com um colega sênior qualquer paciente que não melhore conforme o esperado.[1]
Considere repetir a radiografia de tórax, proteína C reativa (PCR), contagem de leucócitos e outras amostras para microbiologia em pacientes que não progridem satisfatoriamente após 3 dias de tratamento.[1][65]
A falha na proteína C-reativa de 50% ou mais no dia 4 está associada ao aumento do risco de mortalidade em 30 dias, necessidade de ventilação mecânica e/ou suporte inotrópico e complicações.[96]
Practical tip
Indicadores para a melhora clínica:[1][65]
Resolução da febre por >24 horas
Frequência de pulso <100 batimentos/minuto
Resolução da taquipneia
Clinicamente hidratado e tomando fluidos orais
Resolução da hipotensão
Ausência de hipóxia
Melhorando a contagem de leucócitos
Infecção não bacteriêmica
Nenhuma evidência microbiológica de infecção por legionela, estafilococos ou bacilos entéricos gram-negativos
Nenhuma preocupação com a absorção gastrointestinal.
Considere o encaminhamento a um médico respiratório.[1][65]
Em pacientes com PAC de alta gravidade que não respondem aos antibióticos betalactâmicos ou para os quais há suspeita de um patógeno atípico ou viral, solicite reação em cadeia da polimerase (ou outro teste de detecção de antígeno) do escarro ou de outra amostra do trato respiratório.[1][65]
Na comunidade
Avalie a oxigenação por meio da oximetria de pulso.[71]
Não solicite uma radiografia de tórax repetida antes da alta hospitalar em pacientes que se recuperaram satisfatoriamente da PAC.[1][65]
Solicite uma radiografia torácica repetida durante a recuperação após cerca de 6 semanas para os pacientes (independentemente de terem sido internados no hospital):[1][65]
Comsintomas persistentes ou sinais físicos
Que correm maior risco de malignidade subjacente (especialmente pessoas que fumam e pessoas com idade >50 anos).
Practical tip
A resolução das alterações radiográficas ocorre de forma relativamente lenta após a PAC e fica aquém da recuperação clínica.[1]
Considere a broncoscopia em pacientes com sinais, sintomas e anormalidades radiológicas persistentes por volta de 6 semanas após o término do tratamento.[1][65]
O uso deste conteúdo está sujeito ao nosso aviso legal
